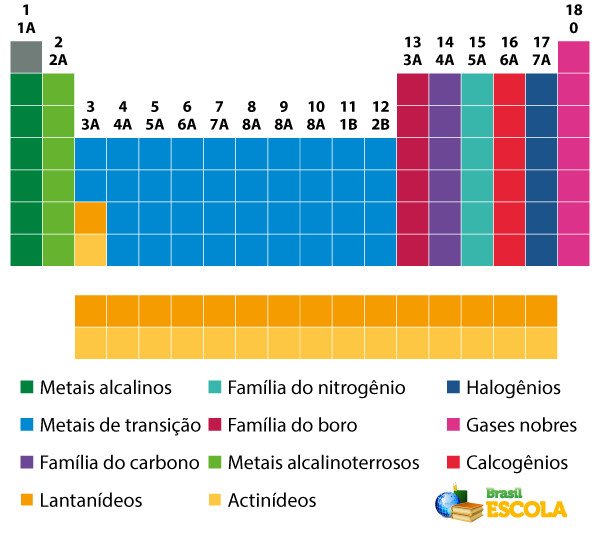
As famílias da Tabela Periódica são as sequências verticais da tabela e reúnem elementos químicos com propriedades químicas similares. Tais similaridades se devem à presença de iguais quantidades de elétrons de valência para os elementos agrupados em uma mesma família. As famílias acomodam os elementos representativos nos grupos 1 e 2, de 13 a 18 e os elementos de transição dos grupos 1 a 12.
Leia também: Elementos transurânicos — os elementos químicos artificiais que vêm depois do urânio na Tabela Periódica
Tópicos deste artigo
- 1 - Resumo sobre famílias da Tabela Periódica
- 2 - Organização das famílias da Tabela Periódica
- 3 - Nomenclatura das famílias da Tabela Periódica
- 4 - Elementos químicos das famílias da Tabela Periódica
- 5 - Principais características das famílias da Tabela Periódica
- → Grupo 1 ou família dos metais alcalinos
- → Grupo 2 ou família dos metais alcalinoterrosos
- → Grupos 3 a 12 ou família dos metais de transição
- → Grupo 13 ou família do boro
- → Grupo 14 ou família do carbono
- → Grupo 15 ou família do nitrogênio
- → Grupo 16 ou família do oxigênio (calcogênios)
- → Grupo 17 ou família dos halogênios
- → Grupo 18 ou família dos gases nobres
- 6 - Tabela Periódica e distribuição eletrônica
- 7 - Exercícios resolvidos sobre as famílias da Tabela Periódica
Resumo sobre famílias da Tabela Periódica
-
As famílias correspondem às linhas verticais da Tabela Periódica.
-
Também conhecidas como grupos, as famílias da Tabela Periódica são numeradas de 1 a 18.
-
Os elementos químicos de uma mesma família possuem propriedades químicas similares.
-
A familiaridade de um conjunto de elementos se explica por possuírem iguais quantidades de elétrons de valência.
-
Os elementos representativos se dividem nos grupos 1, 2, 13, 14, 15, 16, 17 e 18. Cada uma dessas famílias possui nomes específicos.
-
Os elementos de transição formam uma única família que se divide entre os grupos 3, 4, 5, 6, 7, 8, 9, 10, 11 e 12.
Anuncie aqui
Organização das famílias da Tabela Periódica
As famílias na Tabela Periódica são as sequências verticais da tabela, ou seja, as colunas. Também conhecidas como grupos, as famílias da Tabela Periódica são numeradas de 1 a 18, da esquerda para a direita.
Elementos químicos que ocupam a mesma coluna são considerados da mesma família, em razão da similaridade entre suas propriedades químicas, que se deve ao fato de possuírem o mesmo número de elétrons na camada de valência. Por exemplo, todos os elementos químicos da família 18 possuem oito elétrons na camada de valência (camada completa) e raramente participam de ligações químicas.
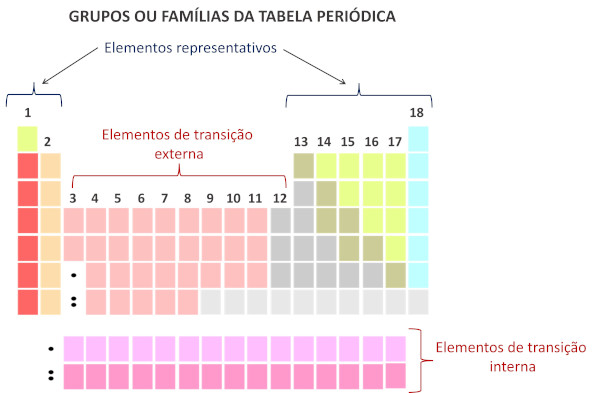
De acordo com o sistema moderno da International Union of Pure and Applied Chemistry (Iupac), cada grupo ou família é identificado por uma numeração de 1 a 18, iniciando da esquerda para a direita na Tabela Periódica.
É importante destacar que o sistema antigo da Iupac adotava um sistema alfanumérico, com as letras A e B para se referenciar aos elementos representativos e de transição, respectivamente. Atualmente, esse tipo de nomenclatura está deixando de ser empregada.
Nomenclatura das famílias da Tabela Periódica
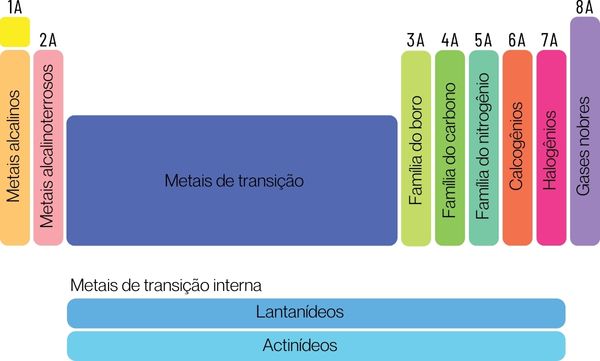
Os elementos químicos podem ser classificados em duas grandes famílias: os elementos representativos e os elementos de transição.
→ Elementos representativos da Tabela Periódica
Os elementos representativos se dividem nos grupos 1, 2, 13, 14, 15, 16, 17 e 18. Cada um desses grupos possui um nome específico, pelo qual também pode ser conhecido. Veja:
-
Grupo 1: família dos metais alcalinos.
-
Grupo 2: família dos metais alcalinoterrosos.
-
Grupo 13: família do boro ou dos metais terrosos.
-
Grupo 14: família do carbono.
-
Grupo 15: família do nitrogênio ou pnicogênios.
-
Grupo 16: família do oxigênio ou calcogênios.
Anuncie aqui -
Grupo 17: família dos halogênios.
-
Grupo 18: família dos gases nobres.
→ Elementos de transição da Tabela Periódica
Os elementos de transição formam uma única família que se divide entre os grupos 3, 4, 5, 6, 7, 8, 9, 10, 11 e 12. A série dos lantanídeos e dos actinídeos também faz parte dos elementos de transição.
Os elementos de transição são todos metálicos e possuem propriedades químicas similares, mesmo possuindo diferentes elétrons na camada de valência e, por isso, formariam uma única e grande família dos metais de transição.
Elementos químicos das famílias da Tabela Periódica
Cada família ou grupo é composto por um conjunto de elementos químicos. Veja a descrição dos elementos químicos que compõem cada família:
-
Grupo 1: lítio, sódio, potássio, rubídio, césio, frâncio.
Anuncie aqui -
Grupo 2: berílio, magnésio, cálcio, estrôncio, bário, rádio.
-
Grupo 3: escândio, ítrio, série dos lantanídeos e série dos actinídeos.
-
Grupo 4: titânio, zircônio, háfnio e rutherfórdio.
-
Grupo 6: cromo, molibdênio, tungstênio e seabórgio.
-
Grupo 7: manganês, tecnécio, rênio e bóhrio.
Anuncie aqui -
Grupo 9: cobalto, ródio, irídio e meitnério.
-
Grupo 13: boro, alumínio, gálio, índio e tálio.
Anuncie aqui -
Grupo 14: carbono, silício, germânio, estanho, chumbo e fleróvio.
-
Grupo 15: nitrogênio, fósforo, arsênio, antimônio e bismuto.
-
Grupo 16: oxigênio, enxofre, selênio, telúrio, polônio e livermório.
-
Grupo 18: hélio, neônio, argônio, criptônio, xenônio e radônio.
Importante: O elemento químico hidrogênio é um caso particular, pois apesar de estar localizado junto ao grupo 1, não faz parte da família dos metais alcalinos, por não compartilhar de propriedades químicas similares.
Saiba mais: Quais são os elementos radioativos da Tabela Periódica?
Principais características das famílias da Tabela Periódica
→ Grupo 1 ou família dos metais alcalinos
-
São sólidos metálicos, brilhantes e macios.
-
Apresentam alta condutividade térmica e alta condutividade elétrica.
-
Possuem temperaturas de fusão relativamente baixas.
-
São altamente reativos com água.
-
Tendência em formar cátions monovalentes (carga +1).
Anuncie aqui
→ Grupo 2 ou família dos metais alcalinoterrosos
-
São sólidos metálicos, brilhantes e mais duros em comparação aos metais alcalinos.
-
Oxidam com facilidade.
-
Apresentam alta condutividade térmica e alta condutividade elétrica.
-
Possuem temperaturas de fusão um pouco mais elevadas em comparação aos metais alcalinos.
-
São reativos com água.
-
Tendência em formar cátions divalentes (carga +2).
Anuncie aqui
→ Grupos 3 a 12 ou família dos metais de transição
-
São a maior família da Tabela Periódica.
-
Sólidos metálicos duros e brilhantes.
-
Apresentam alta condutividade térmica e alta condutividade elétrica.
-
Densos.
-
Elevadas temperaturas de fusão.
-
Podem apresentar diferentes estados de oxidação.
Anuncie aqui
→ Grupo 13 ou família do boro
-
Possuem propriedades intermediárias entre as propriedades dos metais e de não metais.
-
São sólidos em condições ambientes.
-
Tendência em formar cátions trivalentes (carga +3).
→ Grupo 14 ou família do carbono
-
Possuem propriedades intermediárias entre as propriedades dos metais e de não metais.
-
São sólidos em condições ambientes.
-
Tendência em formar quatro ligações.
Anuncie aqui -
São sólidos em condições ambientes.
-
Carbono e silício conseguem formar ligações em cadeia.
→ Grupo 15 ou família do nitrogênio
-
Possuem propriedades intermediárias entre as propriedades de metais e de não metais.
-
Sólidos em condições ambientes, com exceção do nitrogênio, que é um gás.
-
Nitrogênio e fósforo são fundamentais em organismos vivos.
-
Arsênio é altamente tóxico.
Anuncie aqui
→ Grupo 16 ou família do oxigênio (calcogênios)
-
Possuem propriedades diversas, mudando de elemento não metálico para metálico conforme se desce na família.
-
Sólidos em condições ambientes, com exceção do oxigênio, que é um gás.
-
Tendência em formar ânions divalentes (carga -2).
→ Grupo 17 ou família dos halogênios
-
São não metais.
-
Bastante reativos.
-
Maus condutores térmicos e elétricos.
Anuncie aqui -
Sob condições ambientes, flúor e cloro existem como gases, bromo é líquido e iodo é sólido.
-
Tendência em formar ânions monovalentes (carga -1).
→ Grupo 18 ou família dos gases nobres
-
São não metais.
-
Muito pouco reativos, por isso podem ser chamados de gases inertes.
-
Existem sob a forma de gases.
-
Não possuem tendência a formar íons.
Anuncie aqui
Tabela Periódica e distribuição eletrônica
Os elementos químicos pertencentes a uma mesma família ou grupo possuem propriedades químicas similares em razão de possuírem igual quantidade de elétrons na camada de valência.
O número de elétrons na camada de valência é relevante, pois determina a tendência para formação de cátions ou ânions, o tipo de ligação química a ser formada, a energia envolvida em reações químicas, entre outras características. Para encontrar o número de elétrons de valência, é necessário conhecer o número atômico do elemento e realizar a sua distribuição eletrônica.
→ Distribuição eletrônica dos elementos representativos
Os elementos representativos possuem seus elétrons mais energéticos em subníveis s e p da camada eletrônica (n). A tabela a seguir reúne as configurações eletrônicas associadas a cada família dos elementos representativos. O termo n varia de 1 a 7 e representa o nível de energia ocupado pelos elétrons de valência, equivalendo ao período (linha horizontal) da Tabela Periódica em que o elemento se encontra.
|
Distribuição eletrônica dos elementos representativos |
||
|
Família ou grupo |
Distribuição eletrônica |
Exemplo |
|
1 |
ns1 |
Li (Z=3): 1s2 2s1 |
|
2 |
ns2 |
Be (Z=4): 1s2 2s2 |
|
13 |
ns2 np1 |
B (Z=5): 1s2 2s22p1 |
|
14 |
ns2 np2 |
C (Z=6): 1s2 2s22p2 |
|
15 |
ns2 np3 |
N (Z=7): 1s2 2s22p3 |
|
16 |
ns2 np4 |
O (Z=8): 1s2 2s22p4 |
|
17 |
ns2 np5 |
F (Z=9): 1s2 2s22p5 |
|
18 |
ns2 np6 |
Ne (Z=10): 1s2 2s22p6 |
→ Distribuição eletrônica dos elementos de transição
Os elementos de transição estão distribuídos entre os grupos 3 e 12 e possuem os subníveis d e f ocupados pelos elétrons de valência:
-
Elementos de transição externa: mantêm os elétrons de valência no subnível d, mantendo configuração eletrônica igual a ns2 (n-1)d(1 a 8). Por exemplo, o elemento níquel (Z = 28) pertence ao grupo 10, e sua configuração é 1s2 2s2 2p6 3s2 3p6 4s2 3d8.
Anuncie aqui -
Elementos de transição interna: fazem parte do grupo 3, mas ficam “internos” à Tabela Periódica, sendo expandidos abaixo dela, nos períodos 6 (lantanídeos) e 7 (actinídeos). Esses elementos possuem os elétrons de valência ocupando o subnível f e configuração eletrônica geral de ns2 (n-2)f(1 a 13). Por exemplo, o elemento lantânio (Z = 57) é o primeiro elemento da série dos lantanídeos, e sua distribuição eletrônica é 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f1.
Saiba também: Qual é a origem da Tabela Periódica?
Exercícios resolvidos sobre as famílias da Tabela Periódica
Questão 1
(UFC — adaptada) Com relação à classificação periódica moderna dos elementos, assinale a afirmação verdadeira:
A) Na Tabela Periódica, as famílias ou grupos correspondem às linhas horizontais.
B) Em uma família, os elementos apresentam propriedades químicas bem distintas.
C) Em uma família, os elementos apresentam geralmente o mesmo número de elétrons na última camada.
D) Em um período, os elementos apresentam propriedades químicas semelhantes.
E) Os elementos representativos estão distribuídos nos grupos 3 a 12.
Resolução:
Alternativa C
Item A incorreto: as famílias ou grupos são as colunas (linhas verticais) da Tabela Periódica.
Item B e D incorretos: Em uma família, os elementos apresentam propriedades químicas similares. Nos períodos, os elementos possuem a mesma camada eletrônica ocupada pelos elétrons de valência.
Item C correto: Em uma família, os elementos apresentam o mesmo número de elétrons na última camada.
Item E incorreto: os elementos representativos são os grupos 1, 2, 13, 14, 15, 16, 17 e 18. Os elementos de transição estão distribuídos nos grupos 3 a 12.
Questão 2
(EAM) Os elementos A, B e C têm as seguintes configurações eletrônicas em suas camadas de valência:
A: 3s1
B: 4s2 4p4
C: 3s2
Com base nessas informações, assinale a opção correta.
A) O elemento A é um metal alcalino.
B) O elemento B é um halogênio.
C) O elemento C é um calcogênio.
D) Os elementos A e B pertencem ao terceiro período da Tabela Periódica.
E) Os três elementos pertencem ao mesmo grupo da Tabela Periódica.
Resolução:
Alternativa A
Item A correto: o elemento A possui distribuição eletrônica contendo apenas um elétron de valência, logo pertence ao grupo 1 da Tabela Periódica.
Item B incorreto: o elemento B possui configuração eletrônica 4s2 4p4, indicando que há 6 elétrons na última camada e que esse elemento pertence ao grupo 16 (calcogênios).
Item C incorreto: o elemento C possui configuração eletrônica com 2 elétrons na última camada, logo é um elemento do grupo 2 da tabela.
Item D incorreto: o elemento A pertence terceiro período (n = 3), e o elemento B pertence ao quarto período (n = 4).
Item E incorreto: os três elementos possuem diferentes quantidades de elétrons na última camada, logo não podem fazer parte da mesma família.
Por Ana Luiza Lorenzen Lima
Professora de Química