Como o próprio nome diz, os elementos transurânicos são aqueles que possuem o número atômico superior ao número atômico do urânio, isto é, maior que 92 e, que, portanto, vêm após esse elemento na Tabela Periódica.
A obtenção e a descoberta desses elementos em laboratório se devem às experiências realizadas com o bombardeamento com partículas de núcleos atômicos estáveis, de elementos que não são naturalmente radioativos. Assim, eles sofrem transmutação e se transformam em outros elementos.
As primeiras tentativas de produção de elementos além do urânio foram feitas por Fermi, Segrè e colaboradores em 1934, baseando-se nos trabalhos de Irene Curie e Frederic Joliot sobre a radioatividade artificial por meio do bombardeamento de núcleos.
No entanto, apenas em 1940 é que isso foi realizado pela primeira vez, por Edwin M. McMillan e Philip H. Abelson. Eles bombardearam o núcleo do urânio-238 com um feixe de nêutrons; e o resultado foi a obtenção do primeiro elemento transurânico, o netúnio (Np), com número atômico 93:
92238U + 01n → 93239Np + -10β
Nesse caso, os nêutrons não possuem carga, portanto seu bombardeamento ocorre com maior facilidade, não sofrendo repulsão por parte do núcleo, que é carregado positivamente. No entanto, como as pesquisas para obtenção de elementos transurânicos foram se aprofundando, outras partículas (como as partículas alfa, os dêuterons e os prótons) passaram a ser usados como projéteis nesses bombardeamentos. Mas como elas possuem carga positiva, é necessário o uso de um acelerador de partícula, que aumenta as suas velocidades a fim de romper as forças de repulsão com o núcleo.
Assim, com o auxílio dos aceleradores de partículas, possibilitou-se a produção de vários elementos artificiais com números atômicos mais elevados. No mesmo ano de 1940 foi produzido outro elemento transurânico, o plutônio (Pu), com número atômico 94, conforme as reações a seguir:
12H + 92238U → 93239Np + 2 01n
93239Np → 94238Pu + -10β
Os demais elementos transurânicos descobertos foram: o amerício (Am), o cúrio (Cm), o berquélio (Bk), o califórnio (Cf), o einstênio (Es) e o férmio (Fm). E com o tempo houve outros. Na tabela a seguir são mostrados seus números atômicos e as reações de suas obtenções:

No entanto, a determinação das propriedades desses elementos é muito difícil, pois eles são conseguidos em pequenas quantidades e também apresentam grande instabilidade nuclear, decaindo rapidamente quanto maior for seu número atômico.
Um cientista que se destacou nesse campo foi Glenn T. Seaborg, que chefiou a seção que trabalhava com elementos transurânicos dentro do Projeto Manhattan (responsável pelo desenvolvimento da bomba atômica). Foi ele quem isolou e descobriu o plutônio, juntamente com E. M. McMillan, J. W. Kennedy e A. C. Wahl. Depois, ele também descobriu mais quatro elementos transurânicos e, ainda, esteve envolvido na descoberta de mais cinco.
Glenn Seaborg, em 1944, propôs a hipótese de que os elementos de número atômico acima do actínio (Z = 89) formavam uma nova série semelhante aos lantanídeos.Isso permitiu a explicação das propriedades químicas tanto de elementos já identificados quanto dos ainda não identificados. Assim, em 1945, ele publicou a primeira Tabela Periódica que continha os novos elementos descobertos.
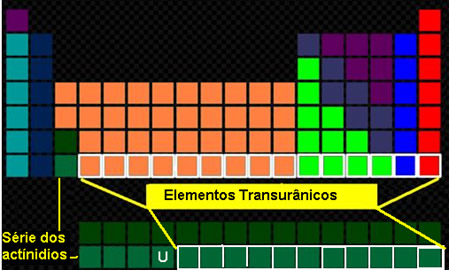
Localização dos elementos transurânicos na Tabela Periódica
Por seus trabalhos nessa área ele recebeu o Prêmio Nobel de Química, em 1951, juntamente com o físico Edwin M. McMillan, já citado. Em sua homenagem, no ano de 1997, o elemento artificial de número atômico 106 foi denominado seabórgio.
Por Jennifer Fogaça
Graduada em Química



