O chumbo é um metal muito versátil pela sua maleabilidade, ductilidade, dureza e resistência à oxidação; é, no entanto, um metal tóxico e bioacumulativo, considerado um contaminante ambiental, além de ser ofensivo à saúde humana. Atualmente se usa o chumbo na fabricação de baterias, mantas de blindagem, cabos, aditivo de gasolina, entre outros.
Leia também: Carbono – elemento químico que pode ser encontrado de diferentes formas na natureza
Tópicos deste artigo
- 1 - Propriedades do chumbo
- 2 - Características do chumbo
- 3 - Aplicações do chumbo
- 4 - Intoxicação por chumbo
- 5 - História do chumbo
- 6 - Obtenção do chumbo
- 7 - Exercícios resolvidos
Propriedades do chumbo
-
Símbolo: Pb
-
Massa atômica: 207,2 u
-
Número atômico: 82
-
Eletronegatividade: 2,33 (Pauling)
-
Configuração eletrônica: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 5d10 4f14 6p2
-
Série química: metal representativo
Anuncie aqui -
Ponto de fusão: 327,46 °C
-
Ponto de ebulição: 1748,85 °C
-
Densidade: 11.340 kg/m3
-
Dureza: 1,5 (escala de Mohs)
-
Solubilidade em água (25 °C): 9580 mg/L

Características do chumbo
O chumbo é um metal pesado, com baixa dureza, por isso, sendo fácil de ser manipulado (maleável), não é um bom condutor de eletricidade. É um elemento anfótero, ou seja, reage em meio ácido e básico, possui resistência à corrosão dos ácidos clorídrico e sulfúrico diluídos, mas se dissolve em ácido nítrico, e, ainda, reage com o ácido acético, não sendo, portanto, indicado para fabricação de utensílios de uso culinário.
Em condições normais de temperatura e pressão, o chumbo possui aspecto sólido, de cor cinza azulado. O chumbo é também um metal tóxico e bioacumulativo, podendo provocar mudanças bioquímicas e funcionais nos organismos vivos.
Aplicações do chumbo
O chumbo é muito aplicado como ligas metálicas, que, misturadas a elementos como estanho, cobre, antimônio, arsênio, bismuto, cadmio e sódio, formam materiais com diversas aplicações. Utiliza-se também sais orgânicos, silicatos e carbonatos de chumbo como reagentes em processos químicos e aditivos:
-
Baterias chumbo-ácido;
-
Fabricação de forros para cabos de energia;
-
Materiais utilizados na construção civil;
-
Aditivo de gasolina (chumbo tetraetila – Pb(C2H5)4);
Anuncie aqui -
Formulação de pigmentos para navios (inibe a fixação de crustáceos);
-
Manta de blindagem contra radiação;
-
Aditivos estabilizantes contra calor e luz, aplicados na fabricação de plásticos;
-
Nitreto de chumbo Pb(N3)2, aplicado na fabricação de detonadores de explosivos.

Intoxicação por chumbo
Os efeitos do chumbo no organismo independem da rota de absorção, mas os principais são inalação, especialmente no caso de exposição ocupacional, e ingestão de água e alimentos contaminados. O sistema nervoso é o mais afetado pela presença do metal no organismo, podendo causar encefalopatia, deficit cognitivo e danos nas funções motoras.
O chumbo pode interferir no sistema sanguíneo, na síntese de células responsáveis pelo transporte de oxigênio e em funções endócrinas; pode causar problemas renais; e diminuir a fertilidade masculina. Em caso de intoxicação severa, causa danos gastrointestinais, podendo ocasionar prisão de ventre, diarreia e gastrite.
Veja também: Nióbio – metal com várias aplicações industriais e comerciais
História do chumbo
A palavra chumbo provém do latim, plumbum, o que explica o símbolo do átomo de chumbo ser Pb. Há hipóteses de que o chumbo esteja sendo usado há 7000 mil anos, isso devido à facilidade de sua extração, maleabilidade e ductilidade do metal. No Tora, ou na Bíblia hebraica, o livro do Êxodo faz menção ao elemento, citando-o como algo denso:
“Sopraste com o teu vento, o mar os cobriu; afundaram-se como chumbo em veementes águas.”
Êxodo 15:10
No Museu Britânico, em Londres, está guardada a peça mais antiga de chumbo descoberta até então, data que tenha sido criada em 3800 a.C. Há registros de que os chineses extraíam e manipulavam o chumbo em 3000 a.C.; os fenícios, em 2000 a.C., exploravam o metal.
Atualmente, em Roma, encontra-se encanamentos de chumbo com as insígnias de imperadores que reinaram em 300 a.C., sendo eles, inclusive, um dos possíveis causadores de demência de muitos governantes e seus familiares, pois, além do chumbo que contaminava a água através dos tubos, os romanos faziam uso do acetato de chumbo para adoçar vinhos, além dos compostos de chumbo que eram aplicados na formulação de cosméticos e tintas. A durabilidade do metal foi aplicada pelos egípcios na fabricação de armas, adornos e utensílios.
Obtenção do chumbo
O chumbo é obtido, principalmente, do sulfeto de chumbo II, encontrado no mineral galena, que possui cerca de 87% de chumbo em sua composição. Para extração do chumbo, faz-se a ustulação, que é o aquecimento do sulfeto na presença de gás oxigênio, obtendo-se como produto o óxido de chumbo, conforme a reação:
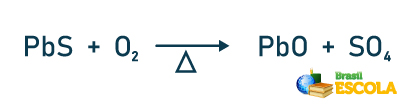
O óxido de chumbo obtido é levado a um forno com agentes redutores. O chumbo é separado por destilação e flotação, e o resultado desse processo é o chumbo metálico, com pureza de 99,99%.
Acesse também: Quais são os nomes dos novos elementos químicos?
Exercícios resolvidos
Questão 1 – (Instituto AOCP) Para o perito criminal, ter conhecimento sobre a tabela periódica é fundamental porque ela permite identificar um elemento químico. Diante disso, assinale a alternativa correta sobre a localização do chumbo e o respectivo comportamento do átomo.
A) O chumbo é um elemento químico de símbolo Pb, número atómico 82 (82 prótons e 82 elétrons), com massa atómica igual a 207,2 u, pertencente ao grupo 14 ou IVA da classificação periódica dos elementos químicos. À temperatura ambiente, o chumbo encontra-se no estado sólido.
B) O chumbo é um elemento químico de símbolo Pb, número atómico 82 (82 prótons e 82 elétrons), com massa atómica igual a 207,2 u, pertencente ao grupo 12 ou IVA da classificação periódica dos elementos químicos. À temperatura ambiente, o chumbo encontra-se no estado sólido.
C) O chumbo é um elemento químico de símbolo Pb, número atómico 22 (82 prótons e 82 elétrons), com massa atómica igual a 207,2 u, pertencente ao grupo 11 ou IVA da classificação periódica dos elementos químicos. À temperatura ambiente, o chumbo encontra-se no estado sólido.
D) O chumbo é um elemento químico de símbolo Pb, número atómico 82 (82 prótons e 82 elétrons), com massa atómica igual a 107,2 u, pertencente ao grupo 12 ou IVA da classificação periódica dos elementos químicos. À temperatura ambiente, o chumbo encontra-se no estado sólido.
E) O chumbo é um elemento químico de símbolo Pb, número atómico 82 (82 prótons e 82 elétrons), com massa atómica igual a 227,2 u, pertencente ao grupo 13 ou IVA da classificação periódica dos elementos químicos. À temperatura ambiente, o chumbo encontra-se no estado sólido.
Resolução
Alternativa A.
B – Incorreta: O chumbo não pertence ao grupo 12 da tabela, e sim ao 14.
C – Incorreta: O número atômico do chumbo não é 22, e sim 82, e seu grupo também não é o 11.
D – Incorreta: A massa atômica do chumbo não é 107,2 u, e sim 207,2u, e ele não pertence ao grupo 12, mas ao 14.
E – Incorreta: O chumbo não tem massa atômica de 227,2 u, mas sim de 207,2u, e seu grupo também não é o 13, mas o 14.
Questão 2 – Sobre o metal chumbo, é incorreto afirmar que:
A) É um metal maleável, dúctil, de coloração cinza azulado.
B) É um metal maleável, condutor de eletricidade, utilizado na fabricação de fios.
C) É um metal de fácil obtenção, com uma infinita versatilidade de uso, principalmente na construção civil.
D) O chumbo foi um dos primeiros metais a ser manipulado pelo ser humano, o metal foi usado como referência de um elemento denso em inscrições bíblicas.
E) O chumbo, apesar de sua versatilidade, é um metal tóxico que pode causar problemas nos sistemas nervoso, gástrico e nos rins.
Resolução
Alternativa B. O chumbo é um metal maleável e é sim utilizado na fabricação de fios, mas para encapar os fios condutores. O chumbo, em si, não é um bom condutor de energia.
Por Laysa Bernardes Marques de Araújo
Professora de Química



