Os gases nobres são os sete elementos contidos no grupo 18 da Tabela Periódica, que vai desde o hélio, He, até o oganessônio, Og. São conhecidos por sua baixíssima reatividade química, consequência direta da sua configuração eletrônica, que proporciona uma alta energia de ionização e baixa afinidade eletrônica.
Leia também: Quais são as famílias da Tabela Periódica?
Tópicos deste artigo
- 1 - Resumo sobre os gases nobres
- 2 - O que são gases nobres?
- 3 - Quais são os gases nobres?
- 4 - Características dos gases nobres
- 5 - Gases nobres na Tabela Periódica
- 6 - Por que os gases nobres são estáveis?
- 7 - Como os gases nobres são obtidos?
- 8 - Para que servem os gases nobres?
- 9 - Exercícios resolvidos sobre os gases nobres
Resumo sobre os gases nobres
- Os gases nobres são os sete elementos presentes no grupo 18 da Tabela Periódica.
- Atualmente, são considerados como gases nobres o hélio, o neônio, o argônio, o criptônio, o xenônio, o radônio e o oganessônio.
- Destacam-se por sua baixa reatividade química, consequência direta da sua configuração eletrônica.
- Contudo, desde a década de 1960, já se conhecem compostos de gases nobres, principalmente do xenônio.
- Os gases nobres conseguem existir na natureza na forma de gases monoatômicos.
- Boa parte dos gases nobres está localizada no ar atmosférico.
O que são gases nobres?
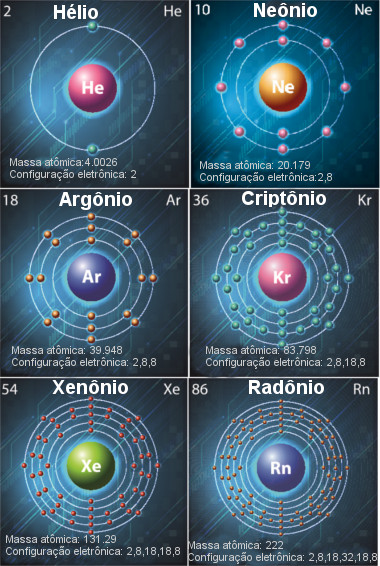
Os gases nobres são um conjunto de elementos representativos localizados no grupo 18 da Tabela Periódica. Sendo assim, são considerados como gases nobres os elementos:
Eles são assim chamados por conta de sua baixa reatividade química, assim como os metais nobres (como ouro, prata e os metais do grupo da platina). Contudo, tal característica é consequência da sua configuração eletrônica, com a camada de valência completa, o que resulta em uma baixa afinidade eletrônica e uma alta energia de ionização, fazendo com que eles sejam inertes quimicamente ou muito pouco reativos.
A nomenclatura “gás nobre” é creditada ao cientista alemão Hugo Erdmann, que utilizou o termo pela primeira vez no ano de 1898, referindo-se a tais elementos como “edelgas” (que, em alemão, significa gás nobre).
Quais são os gases nobres?
Segundo a União Internacional de Química Pura e Aplicada, a IUPAC, são considerados como gases nobres todos os elementos do grupo 18 da Tabela Periódica. Assim sendo, atualmente, são gases nobres os elementos:
- Hélio, He, Z = 2;
- Neônio, Ne, Z = 10;
- Argônio, Ar, Z = 18;
- Criptônio, Kr, Z = 36;
- Xenônio, Xe, Z = 54;
- Radônio, Rn, Z = 86;
- Oganessônio, Og, Z = 118.
Características dos gases nobres
Todas as características mais comuns dos gases nobres derivam da sua configuração eletrônica, em que todos os elementos apresentam a camada de valência totalmente completa, sendo 1s2 para o hélio e ns2 np6 para os demais elementos (em que n indica o período em que tal elemento se encontra na Tabela Periódica).
Tal configuração eletrônica permite que eles possuam uma alta energia de ionização e uma baixa afinidade eletrônica. Consequentemente, tais elementos foram, por muito tempo, considerados quimicamente inertes. A baixa reatividade dos gases nobres é tanta, que lhes permite existirem como compostos gasosos monoatômicos, algo exclusivo desse grupo.
|
Gás Nobre |
Ponto de fusão (°C) |
Ponto de ebulição (°C) |
Primeira energia de ionização (kJ/mol) |
|
He |
- |
-268,93 |
2372 |
|
Ne |
-248,61 |
-246,06 |
2081 |
|
Ar |
-189,37 |
-185,86 |
1521 |
|
Kr |
-157,20 |
-153,35 |
1351 |
|
Xe |
-111,80 |
-108,13 |
1170 |
|
Rn |
-71 |
-62 |
1037 |
O hélio é o elemento que possui a menor temperatura de ebulição conhecida, com poucos graus acima do conhecido zero absoluto. Esse elemento, aliás, não pode ser congelado na pressão de 1 atm.
Os gases nobres são todos incolores, inodoros e insípidos.

Antigamente, era comum a ideia de que os gases nobres fossem chamados de raros, mas isso logo cai por terra, ao se perceber que o hélio é o segundo elemento mais abundante do universo, ficando atrás, apenas, do hidrogênio. O argônio está presente numa concentração de, aproximadamente, 0,92% em volume na atmosfera terrestre, sendo o terceiro componente mais abundante do ar seco e, aproximadamente, 24 vezes mais abundante em volume que o dióxido de carbono, CO2.
Essa percepção de inércia química absoluta para os gases nobres mudou em 1962, quando Neil Bartlett, ao perceber a semelhança entre as energias de ionização entre xenônio e O2, conseguiu reagir o Xe com PtF6. Isso desencadeou a caracterização dos primeiros fluoretos de xenônio, como XeF2, XeF4 e XeF6, os quais podem ser produzidos mediante reação entre o Xe e o F2, em condições que envolvem utilização de raios ultravioleta, descargas elétricas ou passando os gases por um tubo de níquel.
Hoje, compostos de xenônio são os mais diversos dentro dos gases nobres, sendo possível observar o xenônio ligado não só ao flúor, mas também ao oxigênio, cloro, nitrogênio, carbono e, até mesmo, com metais de transição.
O criptônio, que também possui uma energia de ionização relativamente baixa, é capaz de formar o composto binário e estável KrF2. Os fluoretos de xenônio e criptônio, aliás, são excelentes agentes oxidantes e fluorinantes.
Possuindo um raio atômico maior e uma menor energia de ionização que o Xe, esperava-se uma maior gama de compostos de radônio. Embora seja conhecida a espécie RnF2, a alta radioatividade desse elemento, somada ao fato de seu isótopo mais estável (222Rn) possuir uma meia-vida de apenas 3,8 dias, torna os estudos com esse elemento muito complicados. Por isso, a compreensão das características químicas do Rn é muito limitada.
Assim sendo, pode-se considerar que, dado o tamanho do raio atômico e a energia de ionização, apenas hélio e neônio são, de fato, gases nobres inertes quimicamente, tendo apenas algumas espécies transitórias com esses elementos sido observadas em espectrometria de massa. No ano 2000, relatou-se o primeiro composto de argônio, o HArF. Tal substância é relativamente estável em uma baixa temperatura, mas se decompõe em temperatura ambiente.
O oganessônio foi o último elemento a ser colocado nesse grupo, com sua descoberta tendo sido realizada no ano de 2015 e confirmada no ano seguinte pela IUPAC. É um elemento radioativo e seu isótopo mais estável, o 294Og, possui uma meia-vida muito pequena (na faixa de 7 x 10−4 s) e, assim sendo, não há ainda dados suficientes para descrever as propriedades desse elemento.
Gases nobres na Tabela Periódica
Os gases nobres começaram a ser isolados no fim do século XIX, por meio dos trabalhos de Lord Rayleigh e William Ramsay. O primeiro a ser isolado foi o argônio, cujo nome vem do grego e significa “inativo”. Os demais gases nobres foram sendo descobertos nos anos seguintes, por meio dos trabalhos de Ramsay e seu assistente, Morris Travers, utilizando destilação do ar liquefeito em baixa temperatura. O radônio veio a ser isolado em 1902, como um produto de decaimento nuclear, e o oganessônio, apenas em 2015, por meio de reações nucleares.
Foi Ramsay o responsável por sugerir que os gases nobres fossem alocados em um novo grupo da Tabela Periódica, embora Mendeleev, o criador da Tabela Periódica, discordasse de início.
Inicialmente conhecido como Grupo 0, os gases nobres hoje figuram no grupo 18 da Tabela Periódica, ficando na última coluna. São considerados como elementos representativos e se iniciam no primeiro período, com o hélio (He), e finalizam no sétimo período, com o oganessônio (Og).
Por que os gases nobres são estáveis?
A estabilidade dos gases nobres é decorrente da sua configuração eletrônica. À exceção do He, todos possuem oito elétrons na camada de valência (configuração do tipo ns2 np6). Essa configuração permite que os gases nobres combinem uma alta energia de ionização e uma baixa afinidade eletrônica, o que dificulta a ocorrência de processos reacionais. Contudo, à luz dos conhecimentos atuais, nem todos os gases nobres são considerados inertes quimicamente.
Já existem, desde a década de 1960, conhecimento de compostos de xenônio, como o XeF2, o XeF4, o XeF6 e o XeO2. O criptônio também é capaz de formar um fluoreto, de fórmula KrF2. Até o próprio argônio chegou a ter um composto relatado, o HArF, o qual apresenta uma boa estabilidade em baixa temperatura, decompondo-se em temperaturas maiores.
Já o radônio (Rn) e o oganessônio (Og) são radioativos, ou seja, possuem um núcleo atômico estável, que lhes confere a propriedade de emitir partículas nucleares e, assim, transmutando-se em elementos mais leves.
De fato, observando-se os dados que se possuem atualmente, apenas o hélio e o neônio ainda não apresentam compostos estáveis, podendo serem, de fato, considerados inertes quimicamente. Diferentemente dos demais gases nobres, He e Ne possuem um pequeno tamanho, o que lhes confere um acréscimo na sua energia de ionização.
Como os gases nobres são obtidos?
Em termos comerciais, hélio e argônio são os gases nobres mais importantes. O hélio ocorre em depósitos de gás natural (em concentrações de até 7% em volume), além de ser continuamente produzido a partir de decaimentos radioativos, como urânio e tório, já que a partícula alfa é um núcleo de hélio.
Comercialmente, o hélio é obtido a partir do gás natural, uma vez que, por possuir o menor ponto de ebulição dentre os elementos existentes, pode ser obtido a partir da liquefação dos demais componentes gasosos.
|
Gás Nobre |
Abundância no ar seco (% em volume) |
|
He |
5,24 x 10-4 |
|
Ne |
1,82 x 10-3 |
|
Ar |
9,34 x 10-1 |
|
Kr |
1,14 x 10-4 |
|
Xe |
8,7 x 10-6 |
Os demais gases nobres, como neônio e argônio, são obtidos a partir da destilação fracionada do ar atmosférico liquefeito, o que ocorre em baixas temperaturas. O neônio, por exemplo, é obtido como subproduto, uma vez que, durante o processo de destilação, é o único gás remanescente.
Já o argônio, por ter praticamente o mesmo ponto de ebulição do gás O2, é separado deste por meio de um processo de fracionamento, em que gás hidrogênio é acionado e então uma ignição é forçada para remoção de O2 e H2O. Já os demais gases nobres, como criptônio e xenônio, são geralmente separados do gás oxigênio por meio de uma absorção seletiva em carvão.
Para que servem os gases nobres?
Hélio e argônio são comumente utilizados para criar atmosferas inertes, ou seja, um ambiente gasoso que não será capaz de interferir quimicamente no sistema. Isso é muito comum na soldagem a arco ou no crescimento de cristais de silício ou germânio. Nas lâmpadas de filamento (incandescentes), o argônio também foi utilizado para reduzir a evaporação do filamento metálico.
Sendo de baixíssima densidade e não inflamável, o gás hélio é utilizado para inflar pneus de grandes aeronaves e balões, como balões meteorológicos, para pesquisas espaciais e, até mesmo, para simples balões de festa. Possuindo o menor ponto de ebulição existente, o hélio é um importante líquido refrigerante, sendo usado em aparelhos como espetrômetros de ressonância magnética nuclear de alto campo, incluindo os utilizados para geração de imagens diagnósticas de exames médicos.
Mergulhadores que atingem altas profundidades acabam utilizando uma mistura de O2/He ao invés de O2/N2, uma vez que o hélio é bem menos solúvel no sangue que o gás nitrogênio, facilitando o processo de descompressão quando o mergulhador atinge a superfície. Ainda, o hélio é usado como trocador de calor em reatores nucleares resfriados a gás, pois não é corrosivo e não se torna radioativo mediante irradiação.
Os gases nobres neônio, criptônio e xenônio são utilizados em letreiros luminosos ou faróis de veículos.
Leia também: Halogênios — as características dos elementos do grupo 17 da tabela
Exercícios resolvidos sobre os gases nobres
Questão 1. (Enem 2019) Por terem camada de valência completa, alta energia de ionização e afinidade eletrônica praticamente nula, considerou-se por muito tempo que os gases nobres não formariam compostos químicos. Porém, em 1962, foi realizada com sucesso a reação entre o xenônio (camada de valência 5s25p6) e o hexafluoreto de platina e, desde então, mais compostos novos de gases nobres vêm sendo sintetizados. Tais compostos demonstram que não se pode aceitar acriticamente a regra do octeto, na qual se considera que, numa ligação química, os átomos tendem a adquirir estabilidade assumindo a configuração eletrônica de gás nobre. Dentre os compostos conhecidos, um dos mais estáveis é o difluoreto de xenônio, no qual dois átomos do halogênio flúor (camada de valência 2s22p5) se ligam covalentemente ao átomo de gás nobre para ficarem com oito elétrons de valência.
Ao se escrever a fórmula de Lewis do composto de xenônio citado, quantos elétrons na camada de valência haverá no átomo do gás nobre?
A) 6
B) 8
C) 10
D) 12
E) 14
Resposta: Letra C.
O difluoreto de xenônio, XeF2, é obtido por meio da ligação covalente entre o xenônio e dois átomos de flúor. Cada átomo de flúor só realiza uma única ligação covalente, compartilhando, portanto, apenas um elétron. Dessa forma, cada flúor contribui com um único elétron para a estrutura de Lewis e, dessa forma, o xenônio passa a ter 10 elétrons na sua camada de valência: 8 que já possuía, mais os 2 do compartilhamento com os átomos de flúor.
Questão 2. (UERJ/2024) Dentre os elementos químicos do quinto período da tabela de classificação periódica, sabe-se que apenas o xenônio é encontrado no estado gasoso sob condições ambientes. Isso se explica pela alta estabilidade desse elemento, o que resulta em fracas interações interatômicas.
A característica do xenônio que justifica essa estabilidade é:
A) maior raio atômico.
B) energia de ionização nula.
C) menor eletronegatividade.
D) camada de valência completa.
Resposta: Letra D.
A estabilidade dos gases nobres é fruto da sua configuração eletrônica, em que sua camada de valência é completa (dois elétrons para o hélio e oito elétrons para os demais).
Fontes
HOUSECROFT, C. E.; SHARPE, A. G. Inorganic Chemistry. 4. ed. Harlow (Inglaterra): Pearson Education Limited, 2012.
MIESSLER, G. L.; FISCHER, P. J.; TARR, D. A. Química Inorgânica. 5. ed. São Paulo: Pearson Education do Brasil, 2014.
HAYNES, W. M. (ed.) CRC Handbook of Chemistry and Physics. 95a ed. CRC Press: 2014.
ATWOOD, D. Noble Gases: Inorganic Chemistry. In: Encyclopedia of Inorganic Chemistry. 2. ed. Wiley: Nova Jersey, 2005.





