As ligações químicas são as interações que ocorrem entre átomos para se tornarem uma molécula ou substância básica de um composto. Existem três tipos de ligações: covalentes, metálicas e iônicas. Os átomos buscam, ao realizar uma ligação química, estabilizar-se eletronicamente. Esse processo é explicado pela teoria do octeto, que dita que cada átomo, para alcançar estabilidade, precisa ter em sua camada de valência oito elétrons.
Tópicos deste artigo
Ligações química e a regra do octeto
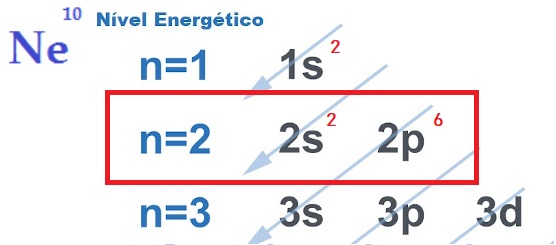
A busca por estabilidade eletrônica, que justifica a realização de ligações químicas entre os átomos, é explicada pela teoria do octeto. Proposta por Newton Lewis, essa teoria afirma que a interação atômica acontece para que cada elemento adquira a estabilidade de um gás nobre, ou seja, oito elétrons na camada de valência.
Para isso, o elemento doa, recebe ou compartilha elétrons da sua camada mais externa, realizando, portanto, ligações químicas de caráter iônico, covalente ou metálico. Os gases nobres são os únicos átomos que já possuem oito elétrons na sua camada mais externa e é por isso que pouco reagem com outros elementos.
Veja também: Regras de distribuição eletrônica: como fazer?
Tipos de ligações químicas
Para obter os oito elétrons na camada de valência como previsto na regra do octeto, os átomos estabelecem ligações entre si, que variam de acordo com a necessidade de doar, receber ou compartilhar elétrons e também com a natureza dos átomos ligantes.
-
Ligações iônicas
Também conhecidas com ligações eletrovalentes ou heteropolares, acontecem entre metais e elementos muito eletronegativos (ametais e hidrogênio). Nesse tipo de ligação, os metais tendem a perder elétrons, transformando-se em cátions (íons positivos), e os ametais e o hidrogênio ganham elétrons, tornando-se ânions (íons negativos).
Os compostos iônicos são duros e quebradiços, possuem alto ponto de ebulição e conduzem corrente elétrica quando estão no estado líquido ou diluídos em água.
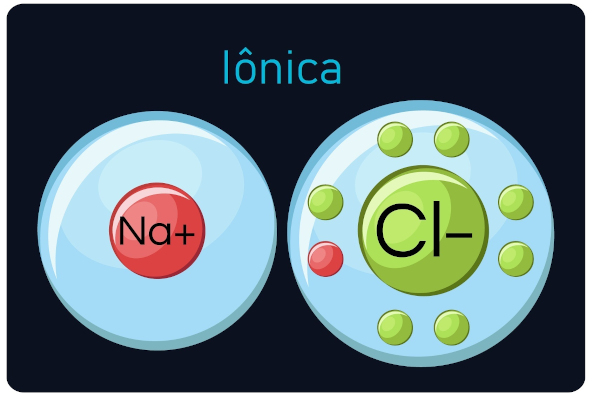
Observação: Fique atento ao fato de que o átomo que ganha elétrons vai se tornar um íon com sinal negativo e que o átomo que perde elétrons fica com sinal positivo.
Exemplos de substâncias iônicas:
- Bicarbonato (HCO3-);
- Amônio (NH4+);
- Sulfato (SO4-).
Para saber mais detalhes sobre esse tipo de ligação química, acesse o nosso texto: ligações iônicas.
-
Ligações covalentes
As ligações covalentes acontecem pelo compartilhamento de elétrons. Em virtude da baixa diferença de eletronegatividade entres os elementos ligantes, eles não doam ou recebem elétrons, mas compartilham pares eletrônicos para assim ficarem estáveis de acordo com a regra do octeto. Esse tipo de ligação é muito recorrente nos elementos simples, como Cl2, H2, O2, e também nas cadeias carbônicas. A diferença de eletronegatividade entre os ligantes determina se a ligação é polar ou apolar.
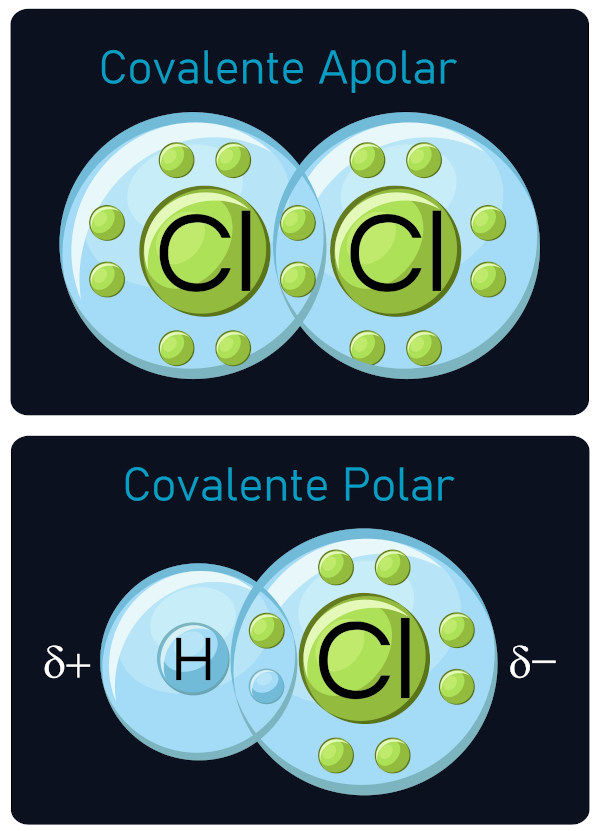
Leia também: Polaridade das móleculas: como identificar?
-
Ligação covalente dativa
Também chamada de ligação covalente coordenada, ligação semipolar, dativa ou coordenada, ela é muito semelhante à ligação covalente, o que difere as duas é que um dos átomos da ligação dativa é responsável por compartilhar dois elétrons. Nesse tipo de ligação, que ocorre artificialmente, a molécula adquire as mesmas características de uma molécula proveniente de uma ligação covalente espontânea.
-
Ligações metálicas
Esse tipo de ligação acontece entre metais, que englobam os elementos da família 1A (metais alcalinos), 2A (metais alcalinoterrosos) e os metais de transição (bloco B da tabela periódica – grupo 3 ao 12), formando o que chamamos de ligas metálicas. A característica diferencial em relação aos demais tipos de ligação é a movimentação dos elétrons, o que explica o fato de os materiais metálicos, no estado sólido, serem ótimos condutores elétricos e térmicos. Além disso, as ligas metálicas possuem alto ponto de fusão e ebulição, ductilidade, maleabilidade e brilho. São exemplos de ligas metálicas:
-
aço: ferro (Fe) e carbono C;
-
bronze: cobre (Cu) + estanho (Sn);
-
latão: cobre (Cu) + zinco (Zn);
-
ouro: ouro (Au) + cobre (Cu) ou prata (Ag).

Resumo
- Ligações químicas: interação entre átomos que buscam estabilidade eletrônica.
- Tipos de ligações: iônicas, covalentes e metálicas.
- Regra do octeto: define que, para o átomo ficar estável, ele deve ter em sua camada de valência oito elétrons.
Exercícios resolvidos
Questão 1 - (Mackenzie-SP) Para que átomos de enxofre e potássio adquiram configuração eletrônica igual à de um gás nobre, é necessário que:
(Dados: número atômico S = 16; K = 19).
a) o enxofre receba 2 elétrons e que o potássio receba 7 elétrons.
b) o enxofre ceda 6 elétrons e que o potássio receba 7 elétrons.
c) o enxofre ceda 2 elétrons e que o potássio ceda 1 elétron.
d) o enxofre receba 6 elétrons e que o potássio ceda 1 elétron.
e) o enxofre receba 2 elétrons e que o potássio ceda 1 elétron.
Resolução
Alternativa E. Visto que o enxofre se encontra na família 6A ou 16, obedecendo à regra do octeto, ele precisa adquirir 2 elétrons para ter assim 8 na sua camada de valência. Já o potássio, que pertence à primeira família da tabela periódica (1A ou família do hidrogênio), para ter em sua camada de valência a configuração de um gás nobre, precisa perder 1 elétron. Combinando 2 átomos de potássio com 1 átomo de enxofre, podemos estabelecer uma ligação iônica em que ambos os elementos encontram-se eletricamente estáveis.
Questão 2 - (UFF) O leite materno é um alimento rico em substâncias orgânicas, tais como proteínas, gorduras e açúcares, e substâncias minerais como, por exemplo, o fosfato de cálcio. Esses compostos orgânicos têm como característica principal as ligações covalentes na formação de suas moléculas, enquanto o mineral apresenta também ligação iônica. Assinale a alternativa que apresenta corretamente os conceitos de ligações covalente e iônica, respectivamente:
a) A ligação covalente só ocorre nos compostos orgânicos.
b) A ligação covalente se faz por transferência de elétrons, e a ligação iônica, pelo compartilhamento de elétrons com spins opostos.
c) A ligação covalente se faz por atração de cargas entre átomos, e a ligação iônica, por separação de cargas.
d) A ligação covalente se faz por união de átomos em moléculas, e a ligação iônica, por união de átomos em complexos químicos.
e) A ligação covalente se faz pelo compartilhamento de elétrons, e a ligação iônica, por transferência de elétrons.
Resolução
Alternativa E.
Vamos analisar as demais:
- Alternativa a: incorreta, pois as ligações covalentes ocorrem também em compostos inorgânicos, como CO2.
- Alternativa b: incorreta, pois as ligações covalentes ocorrem por compartilhamento, e as ligações iônicas, por transferência de elétrons.
- Alternativa c: tanto a ligação covalente quanto a ligação iônica ocorrem por meio da necessidade de perda ou ganho de elétrons, não por atração eletrostática entre os núcleos.
- Alternativa d: ambas as ligações, tanto covalente como iônica, ocorrem pela união de átomos em molécula.
Questão 3 - (PUC-MG) Analise a tabela, que mostra propriedades de três substâncias, X, Y e Z, em condições ambientes.
| Substância | Temperatura de fusão (c°) | Condutibilidade elétrica | Solubilidade na água |
| x | 146 |
nehuma |
solúvel |
| y | 1600 | elevada | insolúvel |
| z | 800 | só fundido ou dissolvido na água | solúvel |
Considerando-se essas informações, é CORRETO afirmar que as substâncias X, Y e Z são, respectivamente:
a) iônica, metálica, molecular.
b) molecular, iônica, metálica.
c) molecular, metálica, iônica.
d) iônica, molecular, metálica.
Resolução
Alternativa C.
A substância X é molecular, visto que as ligações moleculares, também chamadas de covalentes, possuem baixo ponto de ebulição, já que a diferença de eletronegatividade entre os ligantes não é muito alta. Geralmente compostos covalentes não possuem condutividade elétrica, e a solubilidade é variável.
Podemos reconhecer a substância Y como metálica, pois os metais possuem alto ponto de fusão, são ótimos condutores elétricos e insolúveis em água.
Por último, a substância Z é iônica, já que o ponto de fusão é relativamente alto para essa substância, o que é uma consequência do arranjo cristalino da molécula. Quando uma substância iônica está dissolvida em água ou no estado líquido, ela possui íons livres, o que a torna condutora de elétrons e solúvel em água.
Por Laysa Bernardes Marques
Professora de Química





