O bário, símbolo Ba, é um metal alcalinoterroso do sexto período da Tabela Periódica, com número atômico 56. Esse metal possui propriedades químicas semelhantes ao cálcio e ao estrôncio, os dois metais alcalinoterrosos anteriores, lembrando também o comportamento químico do metal alcalino sódio, sendo, porém, um pouco menos reativo.
Tem como principal fonte a barita, BaSO4, mas o elemento também pode ser extraído a partir de seus óxidos e cloretos. Compostos de bário são muito utilizados em fluidos para extração de petróleo e na fabricação de contraste de exames radiológicos. O bário é um elemento extremamente tóxico se estiver dissolvido em uma solução.
Veja também: Berílio — metal alcalinoterroso do segundo período da Tabela Periódica
Tópicos deste artigo
- 1 - Resumo sobre bário
- 2 - Propriedades do bário
- 3 - Características do bário
- 4 - Onde o bário é encontrado?
- 5 - Aplicações do bário
- 6 - Precauções com o bário
- 7 - História do bário
- 8 - Exercícios resolvidos sobre o bário
Resumo sobre bário
-
Bário é um metal alcalinoterroso do sexto período da Tabela Periódica.
-
Apresenta coloração prateada, sendo maleável, dúctil e bastante reativo com gases oxigênio e nitrogênio.
-
Sua principal fonte mineral é a barita, BaSO4.
-
Entre suas principais aplicações está a confecção de fluidos para exploração de petróleo e contraste para exames radiológicos.
-
É altamente tóxico quando dissolvido em meio aquoso.
Anuncie aqui
Propriedades do bário
-
Símbolo: Ba.
-
Massa atômica: 137,33 u.m.a.
-
Número atômico: 56.
-
Eletronegatividade: 0,89.
-
Configuração eletrônica: 6s2.
-
Ponto de fusão: 727 °C.
Anuncie aqui -
Ponto de ebulição: 1897 °C.
-
Série química: metal alcalinoterroso; grupo s; elemento representativo.
Características do bário
Assim como cálcio e estrôncio, o bário tem coloração prateada em sua forma metálica, sendo considerado um metal macio (ou seja, pode ser riscado com facilidade). Além disso, é também:
-
maleável;
-
dúctil;
-
frágil.
Anuncie aqui
Por causa da sua reatividade com o oxigênio e com o nitrogênio, o bário metálico, exposto ao ar, acaba criando manchas na sua superfície. Em termos de reatividade, comporta-se de maneira semelhante aos metais alcalinoterrosos anteriores — cálcio e estrôncio.
A atividade reacional desses metais alcalinoterrosos, em geral, relembra a do metal alcalino sódio, porém sendo um pouco menos reativa. Entre as principais semelhanças com o sódio, estão:
-
a reação com a água (formando gás hidrogênio);
-
a dissolução em amônia líquida (gerando uma solução azul).
Assim como todos os metais alcalinoterrosos, o bário é capaz de reagir, quando aquecido, com os gases oxigênio e nitrogênio, o enxofre e também halogênios.
-
2 Ba + O2 → 2 BaO
Anuncie aqui -
3 Ba + N2 → Ba3N2
-
8 Ba + S8 → 8 BaS
-
Ba + X2 → BaX2, com X= F, Cl, Br, I
Leia também: Quais metais possuem reatividade com água e bases?
Onde o bário é encontrado?
A abundância de bário é menor do que dos metais alcalinoterrosos mais comumente utilizados, que são o cálcio e o magnésio. Sua principal fonte mineral é a barita, BaSO4, com um teor médio de 58,8% do metal. Há também outro mineral de bário, chamado de witherita (Ba2CO3), contudo, por ser raro, não apresenta grande importância econômica.

O bário pode ser obtido em sua forma metálica por meio de processos eletrolíticos, como a eletrólise, não só a partir da barita, mas também advindo de outros compostos, como óxidos e cloretos. Contudo, o bário metálico não tem produção em larga escala, pois os mercados possuem, na verdade, grande demanda por barita. China, Índia e Marrocos lideram a produção mineral de barita, com mais de 60% da produção mundial.
Na natureza, sabe-se que as algas verdes (clorófitas) necessitam de bário para se desenvolver, embora ainda não se tenha clareza sobre o papel que esse elemento desempenha nelas.
As castanhas brasileiras, como a castanha-do-pará, costumam possuir cerca de 1% em massa de bário. Como o bário é extremamente tóxico, alguns especialistas chegaram a dizer que o consumo da castanha deveria ser controlado. Contudo, alguns estudos já conseguiram comprovar que o bário da castanha-do-pará se encontra em forma insolúvel, como sulfato de bário, ficando então indisponível ao organismo humano e, assim, não causando implicações negativas à saúde.
Aplicações do bário
O bário metálico não possui extensa utilização, entretanto, pode ser utilizado em ligas metálicas como agente de desoxidação, já que possui capacidade de formar óxidos estáveis e que podem ser formados antes da solidificação das ligas, diminuindo o teor de oxigênio nestas. Ainda no campo da metalurgia, o cloreto de bário, BaCl2 é amplamente utilizado para aumentar a dureza de ligas ferrosas e aços.
Majoritariamente, as aplicações do bário se dão por conta da barita, BaSO4. O principal uso da barita é na indústria petrolífera. Por conta de sua densidade elevada (na faixa de 4,5 g.cm-3), pouca abrasividade, inércia química e não susceptibilidade magnética, a barita é usada para controlar a densidade de fluidos de perfuração de poços de petróleo e gás.

Entre outros usos tecnológicos e industriais da barita, estão:
-
pigmento branco em papéis fotográficos;
Anuncie aqui -
composição de tintas, plásticos e revestimentos automotivos para proteção à corrosão;
-
formação de concreto de alta densidade e cimentos de proteção à radiação.
A barita ainda é utilizada como precursora de outros sais de bário, tais como:
-
hidróxidos;
-
Anuncie aqui
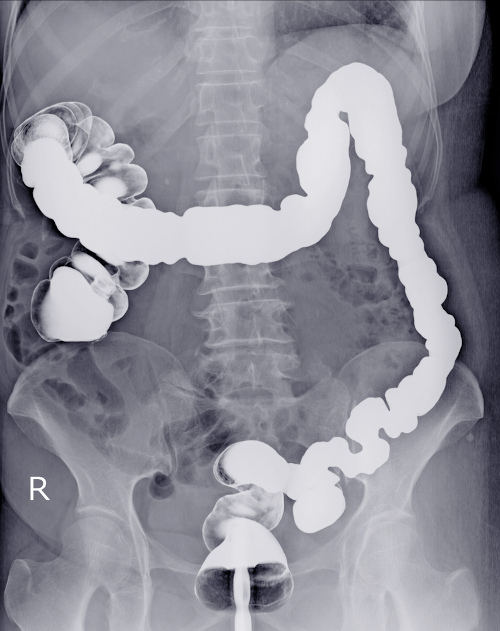
Por ser pouco solúvel em água em pH neutro, o sulfato de bário puro atua como contraste radiológico, uma vez que pode ser ingerido na forma de uma suspensão aquosa. Tal substância tem capacidade de absorver os raios X. Isso faz com que os órgãos internos preenchidos por esta apresentem-se com uma forte coloração branca no resultado do exame. A imagem realçada é melhor visualizada pelo médico e traz uma interpretação mais precisa do resultado.
Saiba mais: O que é ligação metálica?
Precauções com o bário
O bário é um elemento extremamente tóxico ao ser humano se estiver dissolvido. Um caso trágico em referência à toxicidade do bário ocorreu no ano de 2003, no Brasil, quando o contraste radiológico Celobar®, vendido como sulfato de bário, foi responsável pela morte de pelo menos 23 pessoas e de muitos casos de intoxicação.
Tudo começou quando o Laboratório Enila, responsável pela comercialização do produto, realizou, sem qualquer autorização da Agência Nacional de Vigilância Sanitária (Anvisa), experimentos para transformar o carbonato de bário em sulfato de bário.
O intuito desse laboratório era baratear os custos de produção, uma vez que o sulfato de bário era importado da Alemanha. Como consequência, o lote 3040068 apresentou contaminação de carbonato de bário.
Embora o carbonato de bário apresente característica necessária para ser utilizado como contraste, ou seja, ser pouco solúvel em água (17,8 mg.L-1) e assim não permitir a absorção do mesmo pelo organismo, o laboratório não se atentou a alguns fatos: o ânion carbonato é básico, e a baixa solubilidade em água ocorre apenas em pH neutro.
Em solução, o carbonato de sódio apresenta o seguinte equilíbrio, com concentrações bem pequenas de íons:
BaCO3 (s) ⇌ Ba2+ (aq) + CO32- (aq)
Ao adentrar no estômago e sofrer ação do ácido clorídrico, um ácido forte, os poucos mols de ânions carbonato presentes são protonados a ânions bicarbonato (HCO3-), que por sua vez são protonados ao H2CO3, o ácido carbônico. O ácido carbônico, instável, acaba se fragmentando em dióxido de carbono e água, como mostram as reações.
HCl (aq) → H+ (aq) + Cl- (aq)
CO32- (aq) + H+ (aq) ⇌ HCO3- (aq)
HCO3- (aq) + H+ (aq) ⇌ H2CO3 (aq)
H2CO3 (aq) → CO2 (g) + H2O (l)
A diminuição da concentração de ânions carbonato desloca o equilíbrio do BaCO3 para a direita, no sentido de repor a quantidade de carbonato retirada. Contudo, a reposição de ânions carbonato ocorre junto da formação de íons bário, solúveis.
Após a ação do ácido clorídrico, o único ânion disponível é o cloreto (Cl-), porém, este não forma um sal pouco solúvel com o bário, mantendo-o assim disponível para o organismo. O processo do Celobar® pode ser resumido pela seguinte reação:
BaCO3 (s) + 2 HCl (aq) → Ba2+ (aq) + 2 Cl- (aq) + CO2 (g) + H2O (l)
Como consequência do caso, em 2009, o presidente do Laboratório Enila e o chefe da Divisão Química foram condenados a 20 e 22 anos de prisão, respectivamente.
História do bário
O nome bário vem do grego barys, que significa pesado, em referência à alta densidade do elemento. Embora já se conhecesse a barita, a descoberta do bário ocorreu no ano de 1774, havendo, a partir disso, importantes acontecimentos:
-
em 1774, o químico sueco Carl Wilhelm Scheele detectou óxido de bário no gesso;
-
em 1808, Sir Humphrey Davy conseguiu isolar um pouco de bário metálico, embora impuro;
-
em 1855, o bário metálico foi obtido na forma pura, quando Robert Bunsen realizou a eletrólise ígnea de cloreto de bário fundido;
-
em 1905, foi em uma mistura com bário que Marie Curie descobriu o rádio;
Anuncie aqui -
em 1938, Otto Hahn e Fritz Strassmann detectaram bário entre os produtos do bombardeamento de nêutrons em urânio e, em conjunto com Lise Meitner, chegaram à conclusão de que o núcleo de urânio havia sofrido uma reação de fissão.
Exercícios resolvidos sobre o bário
Questão 1
O bário (Ba) é um metal utilizado para vários fins devido a suas características. Sobre esse elemento, assinale a alternativa que contém uma informação INCORRETA.
A) Tem altas temperaturas de fusão e ebulição.
B) Conduz corrente e calor, independentemente do estado em que se encontra (sólido ou fundido).
C) Tende a receber dois elétrons quando se liga ao oxigênio (O).
D) Ao ligar-se com o flúor (F), o composto resultante é do tipo iônico e de fórmula molecular BaF2.
Resolução:
Alternativa C
Como metal, o bário não tende a receber dois elétrons, mas sim a doar. É característica geral dos metais a baixa energia de ionização. Ao se ligar com o oxigênio, formando o BaO, o bário fica na forma do íon Ba2+.
Questão 2
(Enem 2016) Em meados de 2003, mais de 20 pessoas morreram no Brasil após terem ingerido uma suspensão de sulfato de bário utilizada como contraste em exames radiológicos. O sulfato de bário é um sólido pouquíssimo solúvel em água, que não se dissolve mesmo na presença de ácidos. As mortes ocorreram porque um laboratório farmacêutico forneceu o produto contaminado com carbonato de bário, que é solúvel em meio ácido. Um simples teste para verificar a existência de íons bário solúveis poderia ter evitado a tragédia. Esse teste consiste em tratar a amostra com solução aquosa de HCl e, após filtrar para separar os compostos insolúveis de bário, adiciona-se solução aquosa de H2SO4 sobre o filtrado e observa-se por 30 min.
TUBINO, M.; SIMONI, J. A. Refletindo sobre o caso Celobar®. Química Nova n. 2, 2007 (adaptado).
A presença de íons bário solúveis na amostra é indicada pela
A) liberação de calor.
B) alteração da cor para rosa.
C) precipitação de um sólido branco.
D) formação de gás hidrogênio.
E) volatilização de gás cloro.
Resolução:
Alternativa C
Como visto anteriormente no texto, ao tratar a amostra BaCO3 com HCl, podemos descrever a seguinte reação, a qual resume o processo:
BaCO3 (s) + 2 HCl (aq) → Ba2+ (aq) + 2 Cl- (aq) + CO2 (g) + H2O (l)
Ao adicionar uma solução aquosa de ácido sulfúrico, por esse ser um ácido forte, a ionização se dá por completo, representada pela seguinte reação:
H2SO4 (aq) → 2 H+ (aq) + SO42- (aq)
Os íons sulfato (SO42-) reagem com os íons bário (Ba2+), formando o sulfato de bário, muito pouco solúvel em água (2,45 mg.L-1):
Ba2+ (aq) + SO42- (aq) ⇌ BaSO4 (s)
O sulfato de bário é um sólido de coloração branca, portanto, o gabarito adequado é o da letra C, pois os íons bário seriam certificados pela presenta do precipitado branco.
Por Stéfano Araújo Novais
Professor de Química




