Denominam-se de elementos de transição interna todos os 28 elementos químicos localizados no 6º e 7º período do grupo 3 (ou família IIIB) da Tabela Periódica. Eles estão posicionados mais especificamente do lado de fora do corpo principal da Tabela.
São chamados de elementos de transição por não pertencerem às famílias A (elementos representativos), mas não podem ser confundidos com os elementos de transição externa (elementos pertencentes às famílias B e posicionados no corpo principal da Tabela Periódica).
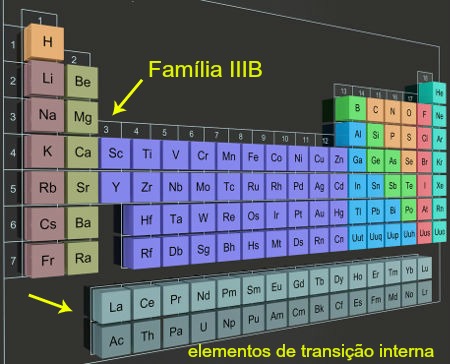
Elementos de transição interna nas colunas localizadas fora da Tabela Periódica
Os elementos de transição interna apresentam o subnível f como mais energético. Uma prova disso é que cada uma das colunas horizontais referentes a esses elementos apresenta apenas 14 elementos, sendo 14 o número máximo de elétrons suportados pelo subnível f.
a) Série dos lantanídeos
Os lantanídeos são todos os que pertencem exclusivamente ao 6º período da família IIIB, sendo chamados assim pelo fato de o primeiro elemento da série ser o lantânio (La). Veja o nome e a sigla de todos eles:
-
Lantânio (La)
-
Cério (Ce)
Anuncie aqui -
Praseodímio (Pr)
-
Neodímio (Nd)
-
Promécio (Pm)
-
Samário (Sm)
-
Európio (Eu)
-
Gadolínio (Gd)
Anuncie aqui -
Térbio (Tb)
-
Disprósio (Dy)
-
Hólmio (Ho)
-
Érbio (Er)
-
Túlio (Tm)
-
Itérbio (Yb)
Anuncie aqui
Todos os elementos de transição interna apresentam o subnível 4f como mais energético, ou seja, a distribuição eletrônica de todos eles termina nesse subnível, como podemos comprovar na distribuição de dois elementos pertencentes à série:
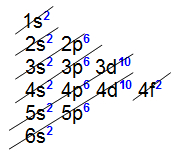
Distribuição eletrônica do elemento lantanídeo Cério

Distribuição eletrônica do elemento lantanídeo Hólmio
b) Série dos actinídeos
Os actinídeos são todos os que pertencem exclusivamente ao 7º período da família IIIB, sendo chamados assim pelo fato de o primeiro elemento da série ser o Actínio (Ac). Veja o nome e a sigla de todos eles:
-
Actínio (Ac)
Anuncie aqui -
Tório (Th)
-
Protactínio (Pa)
-
Urânio (U)
-
Netúnio (Np)
-
Plutônio (Pu)
-
Amerício (Am)
Anuncie aqui -
Cúrio (Cm)
-
Berquélio (Bk)
-
Califórnio (Cf)
-
Einstênio (Es)
-
Férmio (Fm)
-
Mendelévio (Md)
Anuncie aqui -
Nobélio (Nb)
Todos os elementos de transição interna apresentam o subnível 5f como mais energético, ou seja, a distribuição eletrônica de todos eles termina nesse subnível, como podemos comprovar na distribuição de dois elementos pertencentes à série:

Distribuição eletrônica do elemento actinídeo Urânio

Distribuição eletrônica do elemento actinídeo Califórnio
Por Me. Diogo Lopes Dias



