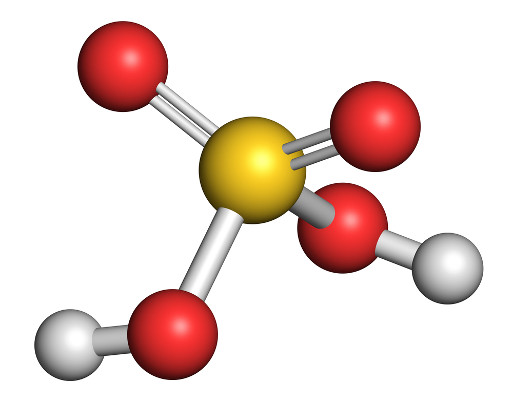
O ácido sulfúrico é um ácido forte e corrosivo, também chamado ácido de bateria ou óleo de vitriolo. É uma das substâncias mais usadas pela indústria e por isso é utilizado como indicador de potência industrial de um país.
Tópicos deste artigo
Características
Na temperatura ambiente, o ácido sulfúrico é líquido, com temperatura de fusão de 10,38 °C e temperatura de ebulição igual a 337 °C, viscoso, incolor, inodoro e corrosivo. Sua densidade é de 1,84 g/cm3 e é solúvel em solventes polares, sendo que com a água ocorre uma reação extremamente exotérmica.
Veja também: Processos endotérmicos e exotérmicos
Por isso, um dos cuidados que devem ser tomados ao misturar-se ácido sulfúrico e água é o de sempre adicionar o ácido na água, e nunca o contrário, pois, assim, a liberação de calor é minimizada.
O ácido sulfúrico possui um grau de ionização alto (α = 61%), ou seja, é um ácido forte. Além disso, possui um elevado poder oxidante e desidratante, e por essa razão, é tão perigoso, pois pode chegar a carbonizar compostos orgânicos, como tecidos de organismos vivos.
Na natureza, o ácido sulfúrico pode ser encontrado na forma diluída, por causa da sua alta solubilidade em água, na chuva ácida e em águas provenientes de fontes minerais que possuem sulfetos, como o sulfeto de ferro.
Saiba mais: Ponto de fusão e ebulição
Fórmula do ácido sulfúrico
O ácido sulfúrico é composto por dois átomos de hidrogênio, um de enxofre e quatro de oxigênio, resultando na fórmula molecular H2SO4, e sua fórmula estrutural é tetraédrica.
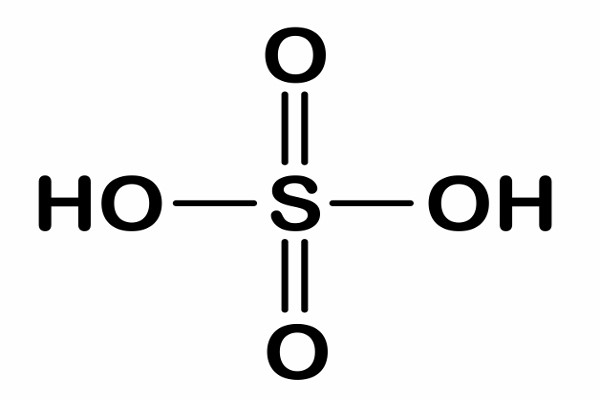
Assim como os outros ácidos, o ácido sulfúrico é solúvel em água, liberando o íon H+, nesse caso: dois cátions. Veja na reação:
H2SO4(aq) → 2 H+(aq) + SO42-(aq)
Para que serve?
O ácido sulfúrico é uma substância química muito produzida e utilizada pelas indústrias, e por isso o seu consumo é tido como indicativo da potência industrial de um país. Uma de suas mais conhecidas aplicações é como solução de baterias usadas em automóveis.

Além disso, o ácido sulfúrico é utilizado na produção de fertilizantes, no refino de petróleo, no tratamento de água, na produção de papel e na limpeza industrial como removedor de oxidação e ferrugem.
O ácido sulfúrico também é utilizado como catalisador em diversos processos químicos, como na fabricação do nylon e do carbono sólido.
Leia também: Diferença entre pilha e bateria
Perigos
O ácido sulfúrico é classificado como um dos ácidos mais perigosos que existem, devido ao seu poder corrosivo e desidratante. Em contato com a pele, o ácido pode provocar queimaduras graves por meio de uma reação de desidratação, decompondo proteínas, carboidratos e lipídios presentes na pele e nos músculos.
Os vapores liberados pelo ácido sulfúrico também são bastante prejudiciais, principalmente se inalados em grandes quantidades, provocando irritação dos olhos e das vias respiratórias.
Por esses motivos, deve-se tomar muito cuidado ao manipular ácido sulfúrico e armazená-lo de forma correta: em recipiente de vidro (uma vez que, dependendo da concentração do ácido, ele pode derreter o plástico) e com a devida rotulação da sua concentração.

Por Victor Ferreira
Professor de Química