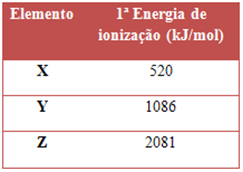
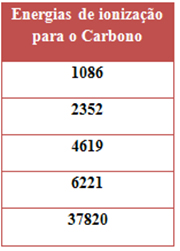
O átomo ou íon só perderá elétrons se ele receber energia suficiente, que é a energia de ionização.
Na prática, o mais importante é primeiro potencial de ionização ou primeira energia de ionização, que corresponde à remoção do primeiro elétron. Ela costuma ser a menor energia de ionização, pois como esse elétron é o mais afastado do núcleo, a sua força de atração com o núcleo é a menor, precisando de menos energia e sendo mais fácil removê-lo.
Além disso, com a perda de elétrons, o raio atômico diminui e o íon fica cada vez mais positivo, portanto, a atração com o núcleo fica mais forte e, consequentemente, será necessária mais energia para retirar o próximo elétron e assim sucessivamente.
Para considerar um exemplo, o átomo de sódio possui como primeira energia de ionização o valor de 406 kJ/mol. Já sua segunda energia de ionização é de 4560, isto é, muito maior que a primeira. Isso mostra que é necessário fornecer muito mais energia ao sódio para retirar dois elétrons do que apenas um. É por isso que na natureza é mais comum encontrar átomos de sódio com a carga +1.
Observe como isso ocorre no caso do alumínio a seguir:
13Al + 577,4 kJ/mol → 13Al1++ e-
13Al + 1816,6 kJ/mol → 13Al2++ e-
13Al + 2744,6 kJ/mol → 13Al3++ e-
13Al + 11575,0 kJ/mol → 13Al4++ e-
Assim, para o Alumínio temos a seguinte ordem de energia de ionização (EI):
1ª EI < 2ª EI < 3ª EI <<< 4ª EI
A partir desse fato, podemos concluir que:

Por isso, se considerarmos os elementos em uma mesma família ou num mesmo período da tabela periódica, veremos que conforme aumentam os números atômicos, menores são as energias de ionização, porque mais afastados do núcleo os elétrons estão. Desse modo, a energia de ionização cresce na tabela periódica de baixo para cima e da esquerda para a direita. Portanto, a energia de ionização é uma propriedade periódica.
Veja como isso é mostrado a seguir e compare os valores da primeira energia de ionização de alguns átomos, que foram obtidos experimentalmente em kJ (quilojoule):
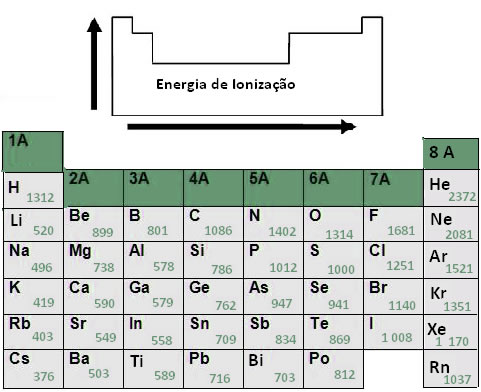
Observe como os valores das energias de ionização dos elementos do segundo período da Tabela Periódica são maiores que os do terceiro período e assim por diante. Atente também ao fato de que a primeira energia de ionização dos elementos da família 1A são menores que os da 2A e assim sucessivamente.
Aqueles elementos representativos que possuem baixa energia de ionização perdem elétrons para se tornarem estáveis, ou seja, ficarem com a configuração de gás nobre. Já os com alta energia de ionização (ametais) recebem elétrons ao invés de perdê-los.
Por Jennifer Fogaça
Graduada em Química