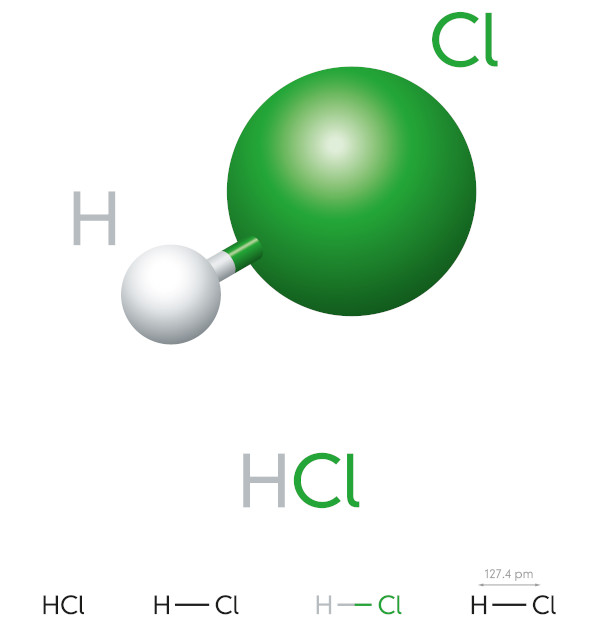
Ácido clorídrico é um hidrácido com alto potencial de ionização, é um líquido de aspecto amarelado, altamente corrosivo e tóxico. É utilizado em diversos processos industriais, como a fabricação de produtos de limpeza e de cloridratos farmacêuticos, em alimentos e em processos siderúrgicos.
Está presente também no organismo humano; o suco gástrico que atua na digestão de proteínas é uma solução de áci;do clorídrico e outras substâncias, como enzimas e sais. A exposição, inalação ou ingestão de ácido clorídrico concentrado é altamente nociva à saúde, podendo causar até a morte.
Leia também: Ácido sulfúrico – substância que possui alto poder corrosivo
Tópicos deste artigo
- 1 - Propriedades do ácido clorídrico
- 2 - Produção do ácido clorídrico
- 3 - Aplicação do ácido clorídrico
- 4 - Ácido clorídrico no organismo
- 5 - Perigos do ácido clorídrico
- 6 - Exercícios resolvidos
Propriedades do ácido clorídrico
- Composto inorgânico
- Ácido forte
- Alto potencial de ionização
- Líquido
- Aspecto amarelado
- Tóxico
- Corrosivo
- Volátil
- Higroscópico (tende a absorver água do ambiente)
- Solúvel em água
Produção do ácido clorídrico
O ácido clorídrico foi descoberto por um alquimista muçulmano chamado Jabir Ibne Haiane, também conhecido como Gaber e considerado o pai da química árabe. Ele sintetizou a substância com base em uma reação entre o sal marinho (NaCl) e o ácido sulfúrico (Na2SO4).
2NaCl + H2SO4 → Na2SO4 + 2HCl
Atualmente o ácido clorídrico é produzido em larga escala por meio da eletrólise de cloreto de sódio em solução aquosa. Desse processo obtém-se gás cloro (Cl2), gás hidrogênio (H2) e hidróxido de sódio (NaOH). Os gases cloro e hidrogênio reagem, formando ácido clorídrico:
Cl2 + H2 → 2HCl
No entanto, essa reação é extremamente exotérmica e de alta periculosidade. Atualmente a maior parte do ácido clorídrico produzido industrialmente está associada à produção de compostos orgânicos, sendo um processo mais econômico e seguro.
R-H + Cl2 → R-Cl + HCl
(Considere R um radical orgânico.)
Veja também: Dicas para determinar-se a força dos ácidos

Aplicação do ácido clorídrico
- Decapagem de metais: o ácido clorídrico é usado para fazer a “limpeza” dos metais antes de serem processados, tirando ferrugem, crosta e outras impurezas da sua superfície.
- Produção de compostos orgânicos: o ácido clorídrico é usado como reagente para obter-se cloreto de vinila, usado na fabricação de plásticos. Do ácido clorídrico provém também o cloropreno, que se aplica em borrachas sintéticas.
- Produção de compostos inorgânicos: o ácido clorídrico está presente em diversos processos industriais de fabricação de reagentes e compostos inorgânicos, entre eles estão os produtos destinados ao tratamento de água, como cloreto de ferro (III) e cloreto de alumínio.
- Usado como produto para limpeza: também comercializado como ácido muriático, o ácido clorídrico é usado para limpezas de áreas pós-construção civil, domésticas, e químicas de ferramentas e maquinário.
- Processamento de alimentos: o ácido clorídrico é aplicado em diversas reações para a produção de alimentos e aditivos, como a hidrólise de amido e proteínas, ou ainda no produto final para equilíbrio de pH.
- Produção de fármacos: o ácido clorídrico é usado na produção de cloridratos solúveis presentes em diversos medicamentos, como o cloridrato de doxiciclina, usado no tratamento de febre tifoide e varíola.
Ácido clorídrico no organismo
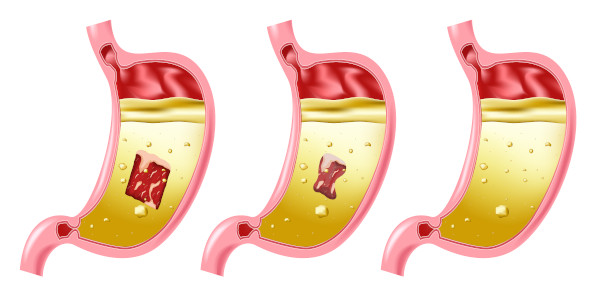
O ácido clorídrico está presente no nosso sistema digestório, o suco gástrico produzido por nosso estômago é uma solução de água, enzimas, ácido clorídrico, sais inorgânicos e uma pequena porcentagem de ácido lático.
O bolo alimentar é transformado em quimo, uma massa de caráter ácido (graças à ação do suco gástrico e sua composição ácida), é quando acontece a digestão de proteínas, transformadas em polipeptídios e aminoácidos que serão absorvidos pelo organismo.
Perigos do ácido clorídrico
O ácido clorídrico é um ácido muito forte e corrosivo, por isso o contato com a substâncias causa diversos danos:
- Pele: causa queimaduras e irritação.
- Olhos: causa severa irritação e pode causar cegueira.
- Inalação: causa irritação e ferimento nas vias aéreas superiores.
- Ingestão: provoca corrosão em todo sistema bocal, e no trato gastrointestinal, pode causar vômitos, hemorragias, diarreia, problemas de circulação, podendo levar à morte.
- Exposição contínua: ataca primeiro as zonas de mucosa, causando dermatite e conjuntivite, sangramento nas gengivas, fotossensibilização; a inalação frequente, ainda que em baixa concentração do composto, pode causar gastrite e sangramento nasal.
Acesse também: Características e propriedades do ácido acético

Exercícios resolvidos
Questão 1 – (Udesc) Com relação ao ácido clorídrico, pode-se afirmar que:
A) quando está em solução aquosa, permite a passagem de corrente elétrica.
B) é um diácido.
C) é um ácido fraco.
D) possui baixo grau de ionização.
E) é uma substância iônica.
Resolução
Alternativa A. O ácido clorídrico não é um diácido, pois possui apenas um H ionizável, mas sim um ácido forte, substância molecular com alto potencial de ionização. A ionização em meio aquoso promove a condução de corrente elétrica devido à existência de íons livres.
Questão 2 – Em uma solução de ácido clorídrico e água, podemos afirmar que a ocorrência de cloreto de hidrogênio (HCl) molecular é mínima, isso ocorre porque
A) o ácido clorídrico em contato com a água é diluído.
B) o cloreto de hidrogênio é uma substância que não solubiliza em água.
C) o cloreto de hidrogênio tem alto potencial de ionização, por isso, quando em meio aquoso, a molécula HCl forma íons H+ Cl-.
D) o ácido clorídrico, por ser muito volátil, separa-se da solução, restando apenas moléculas de água.
E) o ácido clorídrico é uma substância iônica, portanto, em solução aquosa, dissocia-se, formando íons.
Resolução
Alternativa C.
A) A resposta não condiz com a questão, o ácido clorídrico diluir-se em água não justifica a ausência de HCl molecular.
B) Incorreto, o cloreto de hidrogênio é solúvel e tem afinidade pela água.
C) Correta
D) Apesar de o ácido clorídrico ser volátil, essa segregação das duas espécies da solução não acontece de forma significativa.
E) O ácido clorídrico é uma solução de cloreto de hidrogênio e água, sendo que o cloreto de hidrogênio é uma substância molecular não iônica.
Por Laysa Bernardes Marques de Araujo
Professora de Química




