O ácido acético é um líquido incolor de cheiro irritante e penetrante e sabor azedo, que é quimicamente denominado de ácido etanoico e sua fórmula estrutural está demonstrada a seguir:
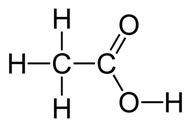
Veja que ele é um composto que pertence ao grupo orgânico dos ácidos carboxílicos.
Ele é o principal constituinte do vinagre, que é uma solução aquosa de 4 a 10% em massa de ácido acético. Ele foi obtido pela primeira vez por meio do etanol do vinho, que se oxida com o oxigênio presente no ar. Daí a origem do seu nome, pois vinho azedo vem do latim acetum que significa “vinagre”.
O uso desse composto é muito antigo, inclusive, as legiões romanas que conquistaram grande parte do mundo, conhecidas no século III a.C., marchavam longas distâncias e levavam consigo um frasco contendo vinho azedo diluído. Essa mistura de ácido acético estimulava a salivação dos soldados e diminuía a sensação de sede.

Hoje em dia, a indústria costuma usar o mesmo princípio, isto é, a oxidação do etanol (álcool etílico), para se produzir esse ácido:
H3C ─ CH2 ─ OH + O2 (ar) → H3C ─ COOH + H2O
Etanol oxigênio ácido acético ou etanoico água
No caso do vinagre, essa oxidação mostrada na reação química acima é obtida por meio de fermentação, com o auxílio do fungo Mycoderma aceti (chamado mãe do vinagre) e da enzima alcooloxidase. Podem-se usar também bactérias do gênero Acetobacter e Clostridium acetobtylicum. Porém, outro meio é o uso de um catalisador como o pentóxido de divanádio (V2O5).
Pode-se também produzir o ácido acético por meio da oxidação do metanol, pela destilação da madeira e a partir de derivados do petróleo.
Além de ser usado como tempero na alimentação, o acido acético também é usado na produção de acetato de vinila (para se fazer o polímero PVA), de anidrido acético e cloreto de acetila (usados em sínteses orgânicas), de ésteres (solventes, perfumes, essências, entre outros), de acetato de celulose (fibras têxteis), de acetatos inorgânicos etc.
Quando está na sua forma pura é chamado de ácido acético glacial, pois se solidifica a temperatura de 16,7ºC, ficando com o aspecto de gelo.

Por Jennifer Fogaça
Graduada em Química



