A densidade determina a quantidade de massa presente em um determinado volume. Tal conceito, embora simples, é de extrema importância para a Química. Por meio dela, é possível determinar propriedades da matéria, como o raio atômico dos metais, além de poder ser utilizada no controle de qualidade de diversas substâncias.
A densidade também é muito utilizada para determinar se um objeto flutuará em outro ou não. Por ser uma grandeza que depende da massa e do volume, acaba sendo afetada pela composição da substância, temperatura e pressão.
Leia também: O que estudar de Química Geral para o Enem?
Tópicos deste artigo
- 1 - Resumo sobre densidade
- 2 - O que é densidade?
- 3 - Como calcular a densidade?
- 4 - Fatores que afetam a densidade
- 5 - Densidade absoluta, densidade relativa e massa específica
- 6 - Densidade de alguns materiais
- 7 - Exercícios resolvidos sobre densidade
Resumo sobre densidade
-
A densidade de uma substância é a razão entre sua massa e o seu volume.
-
Por ser uma propriedade específica da matéria, pode ser utilizada na identificação de substâncias.
-
Também é utilizada na determinação de propriedades da matéria e no controle de qualidade.
-
A densidade determina se um corpo ou uma substância irá flutuar em outro ou não, pois corpos de menor densidade flutuam sobre outros de maior densidade.
-
Embora tenham diferenças conceituais, as palavras densidade e massa específica são utilizadas como sinônimos no cotidiano.
Anuncie aqui -
A densidade absoluta é um valor adimensional utilizado para determinar quão mais ou menos denso uma substância é em relação a outra.
-
Entre os elementos da Tabela Periódica, o ósmio é o elemento mais denso.
O que é densidade?
Em Química, a densidade determina a quantidade de massa presente em um determinado volume. Deve-se recordar que a palavra “densidade” transcende diversas áreas do conhecimento, sendo também utilizada em Física, Literatura, Matemática e tantas outras. Por isso, é essencial que o aluno tenha pleno conhecimento do conceito para não se confundir.
A densidade tem grande utilidade na Química. Usamos esse conceito para nos auxiliar na determinação de outras propriedades da matéria, como o raio atômico de metais. Também é comum utilizar valores de densidade para determinar se uma substância flutuará ou afundará em outra substância em um sistema heterogêneo, já que a densidade influencia diretamente na força peso de cada corpo ou substância. Quanto maior a densidade, maior a força peso; assim, objetos ou fluidos de maior densidade possuem uma força peso maior e, por isso, direcionam-se para o fundo dos recipientes em que estão.
Você já deve ter notado que, em derramamentos de petróleo no oceano, ele nunca afunda, pois é uma substância menos densa que as águas salgadas. O mesmo ocorre no Mar Morto, uma vez que a alta concentração de sais faz com que a densidade da água seja maior, favorecendo a flutuabilidade dos nadadores.

Em testes de laboratório e controle de qualidade, a densidade funciona para identificar substâncias ou determinar se estão dentro dos parâmetros estabelecidos pelas normas técnicas. Por exemplo, a Agência Nacional de Petróleo (ANP) determina parâmetros de qualidade para os combustíveis vendidos em postos.
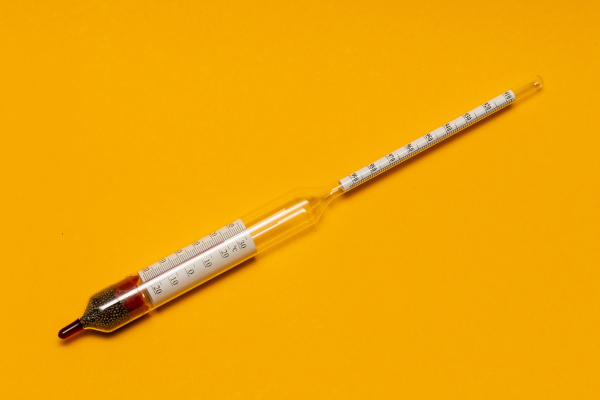
É muito comum a adulteração do etanol por adição de água, o que pode trazer sérios problemas ao funcionamento do veículo. Contudo, a adição de água faz aumentar a densidade do combustível e é por isso que existe, por norma da ANP, a obrigação de um densímetro acoplado à bomba, de modo que o consumidor possa atestar a qualidade do combustível vendido.
Como calcular a densidade?
A densidade de uma substância pura pode ser facilmente calculada pela seguinte fórmula:
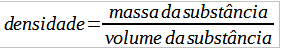
Por relacionar massa e volume, os valores de densidade possuem unidades como g/mL ou g.mL-1 (grama por mililitro), kg/L ou kg.L-1(quilograma por litro), além de utilizar unidades cúbicas, como g/cm³ ou g.cm-3 (grama por centímetro cúbico) e kg/m³ ou kg.m-3 (quilograma por metro cúbico).
Porém, para misturas homogêneas, a densidade da solução deve ser calculada por uma média ponderada, levando-se em consideração a quantidade de cada participante no sistema.
Por exemplo, o álcool 70 °INPM vem sendo muito utilizado nas medidas de prevenção ao novo coronavírus. O termo “NPM” significa Instituto Nacional de Pesos e Medidas e é uma graduação para indicar a massa de álcool (etanol) na água. Assim, o álcool 70 °INPM possui 70% de massa em álcool e 30% de massa em água.
Assim, como o álcool tem 70% na participação da massa da solução final, a densidade poderá ser calculada por meio da seguinte média ponderada:
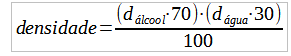
Na equação, dálcool é a densidade do álcool puro e dágua é a densidade da água pura.
Leia também: Quais são os estados químicos da matéria?
Fatores que afetam a densidade
A densidade é uma medida sensível às alterações de pressão, temperatura e composição.
A alteração da pressão tem grande influência em sistemas gasosos. Devemos lembrar que os gases são completamente expansíveis, o que quer dizer que sempre tomarão forma e volume do recipiente em que estão inseridos. Assim, um aumento da pressão ocasiona um sistema mais comprimido, ou seja, diminui-se o volume do gás. Já um sistema de menor pressão ocasiona um sistema mais expandido, o qual aumenta o volume do gás.
A temperatura também é capaz de alterar a densidade, pois diferentes temperaturas geram uma maior aproximação ou distanciamento das partículas da substância. Um aumento da temperatura faz com que as partículas tenham mais energia cinética, movimentando-se com mais velocidade e se distanciando mais umas das outras. Isso ocasiona um aumento do volume, diminuindo assim a densidade.
Já a diminuição da temperatura causa o efeito contrário. As partículas, agora com menor energia cinética, aproximam-se mais e, com menos grau de movimentação e velocidade, comprimem-se em um menor volume, o que aumenta a densidade.
Contudo, a água não segue essa tendência. É muito comum dizermos que a água possui uma imperfeição na sua variação da densidade com a temperatura. O que ocorre é que, a 4 °C, a água atinge seu valor máximo de densidade e, a partir daí, diferentemente de outras substâncias, começa a apresentar valores menores de densidade.
Abaixo de 4°C, a água se expande, em vez de se comprimir ainda mais. A explicação para tal fato é que, com menor agitação molecular (devido à menor temperatura), as moléculas de água começam a se agrupar em cristais, que ocupam um volume maior que aquele que seria ocupado caso essas moléculas estivessem isoladas e não formassem tal estrutura. Assim, a água no estado sólido é menos densa que a água no estado líquido. Você pode perceber isso, pois, ao colocar um cubo de gelo em um copo de água, ele flutua.
Essa “anomalia” da água é essencial para a manutenção da vida aquática. Quando o inverno se aproxima, a água dos lagos começa a se resfriar. Contudo, ao atingir uma temperatura de 4 °C, sua densidade começa a cair e, assim, massas de água líquida entre 0 °C e 4° C ocupam apenas as regiões da superfície. Com isso, apenas a água da superfície se congela, mantendo as camadas mais profundas no estado líquido, uma vez que são mais densas e quentes. Do contrário, a cada inverno, os lagos congelariam por completo, impedindo a proliferação e manutenção da vida aquática.

Por fim, a composição das substâncias também afeta a densidade delas. Imagine duas substâncias hipotéticas. Quando estão puras, elas possuem seus próprios valores de densidade. Porém, ao misturarmos as duas, a solução resultante possuirá uma densidade intermediária, que pode ser calculada por uma simples média ponderada.
Um experimento muito simples para retratar esse efeito é o que se coloca um ovo de galinha em água. Quando a água está pura, o ovo afunda no recipiente, indicando que possui uma maior densidade. Porém, ao se adicionar sal, que é uma substância miscível em água e também mais densa, a mistura homogênea água e sal ficará com maior densidade, fazendo o ovo flutuar.

Densidade absoluta, densidade relativa e massa específica
É muito comum vermos em livros de ciências os termos densidade absoluta, densidade relativa e massa específica, os quais, obviamente, podem causar certa confusão entre os estudantes.
A densidade absoluta é comumente associada como sinônimo de massa específica, sendo esta representada pela letra grega rô (ρ). A forma de cálculo é a que se conhece: a razão entre a massa da substância pelo seu volume.
Contudo, para que essa razão seja classificada como massa específica (ou densidade absoluta), a substância deve estar em sua forma pura (sem ser em uma mistura). Assim, cada substância pura possui seu próprio valor de massa específica em uma dada temperatura.
Além disso, podemos caracterizar a massa específica como uma propriedade específica da matéria. Isso quer dizer que cada substância pura tem seu próprio valor, que a identifica e diferencia das demais substâncias.
Deve ser dito que alguns autores apresentam outras formas de diferenciar os termos “massa específica” e “densidade”, dificultando-se uma padronização de conceitos. Porém, no cotidiano e em muitos livros e exames de vestibular, essa diferenciação fica em segundo plano, sendo ambos os termos utilizados como sinônimos.
Assim, o termo “densidade” pode ser utilizado para situações mais amplas, em que não são obedecidos os critérios específicos para que a medida seja considerada como massa específica ou densidade absoluta.
Já a densidade relativa é importante para determinar quão mais ou menos denso uma substância é em relação à outra.
Por exemplo, a densidade do alumínio é de 2,7 g/mL a 20 °C, enquanto a densidade do mercúrio é de 13,6 g/mL a 20 °C. Assim, a densidade relativa pode ser calculada como:
![]()
Com isso, podemos concluir que o mercúrio é cerca de cinco vezes mais denso que o alumínio. Repare que o valor final da densidade relativa é adimensional, ou seja, sem unidades. Isso porque está sendo feito o quociente de dois valores com a mesma unidade e, assim, elas se anulam. Toda densidade relativa deve ser expressa de forma adimensional.
Densidade de alguns materiais
-
Água: valor mais conhecido de densidade, é igual 1,0 g/mL na temperatura de 4 °C.
-
Ósmio: possui a maior densidade entre todos os elementos da Tabela Periódica, sendo de 22,5 g/mL a 20 °C.
-
Ar atmosférico: o ar que nós respiramos, o qual é uma grande mistura gasosa, possui densidade de 1,18 x 10-3 g/mL em temperatura ambiente.
-
Hélio: sua densidade é de 1,66 x 10-4 g/mL em temperatura ambiente, cerca de 10 vezes menos que a densidade do ar em mesmas condições. Por isso, balões de gás hélio ascendem quando soltos ao ar.
Anuncie aqui
-
Etanol combustível: o etanol vendido em postos de combustíveis (92,5 °INPM a 95,4 °INPM) deve possuir uma densidade entre 0,80 g/mL e 0,81 g/mL a 20 °C. Se vendido com densidade diferente desse valor, é considerado adulterado.

Exercícios resolvidos sobre densidade
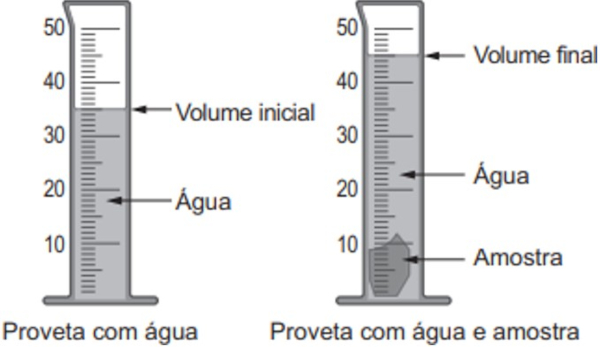
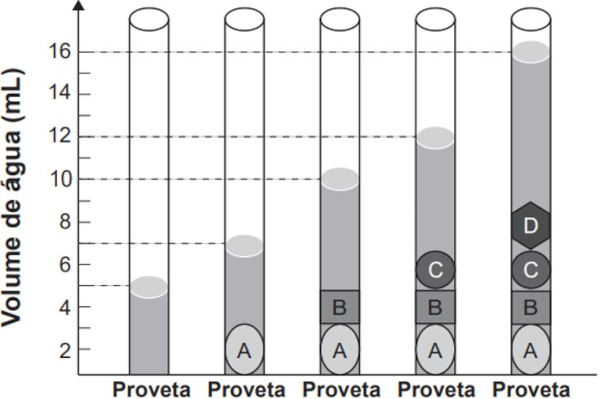
Questão 1 – (Enem 2020) As moedas despertam o interesse de colecionadores, numismatas e investidores há bastante tempo. Uma moeda de 100% cobre, circulante no período do Brasil Colônia, pode ser bastante valiosa. O elevado valor gera a necessidade de realização de testes que validem a procedência da moeda, bem como a veracidade de sua composição. Sabendo que a densidade do cobre metálico é próxima de 9 g cm−³, um investidor negocia a aquisição de um lote de quatro moedas A, B, C e D fabricadas supostamente de 100% cobre e massas 26 g, 27 g, 10 g e 36 g, respectivamente. Com o objetivo de testar a densidade das moedas, foi realizado um procedimento em que elas foram sequencialmente inseridas em uma proveta contendo 5 mL de água, conforme esquematizado.
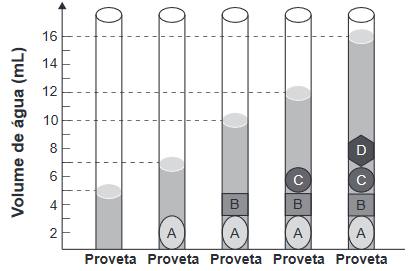
Com base nos dados obtidos, o investidor adquiriu as moedas:
A) A e B
B) A e C
C) B e C
D) B e D
E) C e D
Resolução
Alternativa D.
As moedas serão totalmente de cobre se os seus valores de densidade forem iguais a 9 g/cm³, a densidade do cobre puro. Lembre-se que 1 cm³ é igual a 1 mL.
Inicialmente a proveta contém apenas 5 mL de água. Ao se inserir a moeda A, esse volume é deslocado para 7 mL, conforme graduação presente na imagem. Assim, a moeda A tem um volume de 2 mL e sua densidade calculada como: dA = 26 g/2 mL → dA = 13 g/mL; podendo-se concluir que a moeda A não é de cobre.
Já a moeda B, ao ser inserida na proveta, desloca o volume de 7 mL para 10 mL, um acréscimo de 3 mL. Calculando-se sua densidade: dB = 27 g/3 mL → dB = 9 g/mL; podendo-se concluir que a moeda B é de cobre.
A moeda C aumenta de 2 mL o volume da proveta (deslocando de 10 mL para 12 mL), sua densidade é então: dC = 10 g/2 mL → dC = 5 g/mL; podendo-se concluir que a moeda C não é de cobre.
Por fim, a moeda D apresenta um volume de 4 mL, pois desloca o volume da proveta de 12 mL para 16 mL. Tendo massa de 36 gramas, sua densidade é: dD = 36 g/4 mL → dD = 9 g/mL; podendo-se concluir que a moeda D é de cobre.
Assim, as duas moedas de cobre são B e D, as quais são adquiridas pelo investidor, o que está descrito na alternativa D.
Questão 2 – (Enem 2020) O exame parasitológico de fezes é utilizado para detectar ovos de parasitos. Um dos métodos utilizados, denominado de centrífugo-flutuação, considera a densidade dos ovos em relação a uma solução de densidade 1,15 g mL-1. Assim, ovos que flutuam na superfície dessa solução são detectados. Os dados de densidade dos ovos de alguns parasitos estão apresentados na tabela.
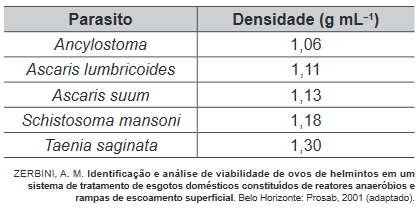
Considerando-se a densidade dos ovos e da solução, ovos de quais parasitos podem ser detectados por esse método?
A) A. lumbricoides, A. suum e S. mansoni.
B) S. mansoni, T. saginata e Ancylostoma.
C) Ancylostoma, A. lumbricoides e A. suum.
D) T. saginata, S. mansoni e A. lumbricoides.
E) A. lumbricoides, A. suum e T. saginata.
Resolução
Alternativa C.
A questão deixa claro que os ovos detectados são aqueles que flutuam na superfície da solução, cuja densidade é de 1,15 g/mL.
Flutuarão os ovos dos parasitos que possuírem um valor de densidade menor que a da solução.
Assim, serão detectados nesse teste os ovos dos parasitos Ancylostoma, Ascaris lumbricoides e Ascaris suum, pois, de acordo com a tabela apresentada, seus valores de densidade são menores que da solução. Sendo assim, alternativa C.
Por Stéfano Araújo Novais
Professor de Química