Os estados físicos da matéria são determinados pelo distanciamento entre as moléculas, conexões moleculares e energia cinética que movimenta as partículas de uma amostra. São eles:
- sólido;
- líquido;
- gasoso;
- plasma;
- condensado de Bose-Einstein.
Em estado sólido, temos moléculas bem agrupadas e com pouca movimentação. No extremo oposto, estão o estado gasoso e o plasma, nos quais as moléculas têm um espaçamento entre elas e alta energia cinética. Materiais em estado líquido ficam no meio-termo, não possuem forma física definida, apresentam mais energia cinética que um material sólido e um espaçamento entre as moléculas menor que materiais gasosos. O condensado de Bose-Einstein é uma descoberta relativamente nova que gira em torno da ideia de se ter uma amostra sem movimentação entre as moléculas, isto é, sem energia cinética.
Leia também: O que estudar de Química Geral para o Enem?
Tópicos deste artigo
- 1 - Estado sólido
- 2 - Estado líquido
- 3 - Estado gasoso
- 4 - Fatores que determinam os estados físicos
- 5 - Mudanças de estado físico
- 6 - Outros estados físicos
- 7 - Exercícios resolvidos
Estado sólido
As moléculas de um material em estado sólido conectam-se com uma força suficiente que resulta em formato e volume definidos. Nesse estado temos pouca energia cinética entre as partículas e, ainda que exista uma pequena movimentação entre elas, não é possível visualizá-la macroscopicamente (a olho nu).
A forma de um sólido pode ser alterada quando o material sofre ação de uma força mecânica (quebra, arranhão, amassado) ou quando há alteração de temperatura e pressão. Cada tipo de material tem resistência a esses impactos ou a mudanças externas, de acordo com a sua natureza.
-
Exemplo
Como exemplo, podemos citar o ouro, material sólido em temperatura ambiente com ponto de fusão de 1064,18 °C e ponto de ebulição de 2855,85°C.

Estado líquido
No estado líquido, não há forma física definida, mas há volume definido, o que nos impede de comprimir o material de forma significativa. Os líquidos têm força intermolecular fraca, o que permite manipular e separar partes de uma amostra com facilidade. A força de atração entre as moléculas impede que elas se movam livremente como um gás. Além disso, a tensão superficial (força de atração entre moléculas iguais) é a que possibilita a formação de gotas.
- Exemplo
O exemplo mais abundante e acessível que temos de material no estado líquido em condições normais de temperatura e pressão é a água, também considerada solvente universal.

Estado gasoso
Um material em estado gasoso não tem forma nem volume definidos. Possui alta capacidade de expansão em razão da energia cinética elevada. Quando colocado em um recipiente, o gás espalha-se indefinidamente e, se nessas condições de confinamento, o gás for aquecido, acontecerá um aumento na energia cinética e uma elevação na pressão do sistema.
Vale ainda ressaltar a diferença entre gás e vapor. Apesar de estarem no mesmo estado físico, eles têm naturezas diferentes. O vapor, quando colocado sob alta pressão ou diminuindo a temperatura, volta ao estado líquido. Os gases, por sua vez, são substâncias que, em condições normais, já estão no estado gasoso e, para se liquefazer, é necessário ter aumento de pressão e temperatura simultaneamente.
-
Exemplo
Um exemplo de substância gasosa está comumente dentro dos balões de festa, o gás hélio, que é um gás nobre e monoatômico (molécula de um átomo), sendo encontrado em estado gasoso para condições normais de temperatura e pressão. A densidade do hélio é menor que a do ar atmosférico, o que faz com que os balões flutuem.

Fatores que determinam os estados físicos
O que determina o estado físico da matéria é a organização de suas moléculas, o espaçamento entre elas e a energia cinética (energia de movimentação). Cada elemento possui um ponto de fusão e ebulição que definem o ponto crítico, isto é, em que temperatura e pressão o elemento mantém ou altera seu estado físico. Esse ponto crítico varia de acordo com a natureza do material. Além disso, para cada elemento, temos diferentes forças intermoleculares, o que também influencia o estado físico.
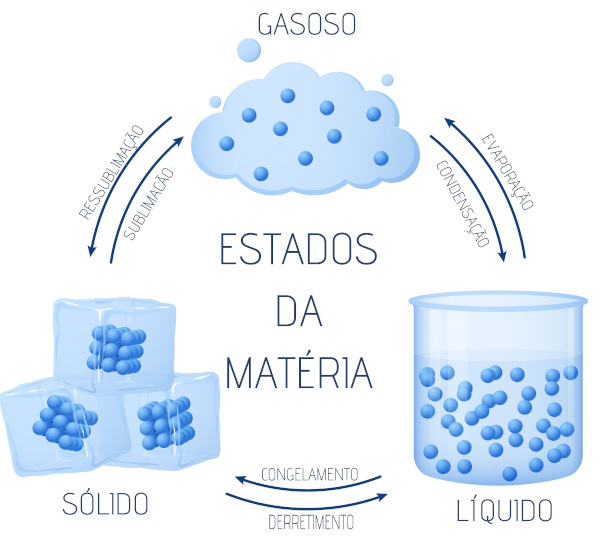
Mudanças de estado físico
As possíveis mudanças no estado físico ocorrem com a alteração de temperatura e pressão. Veja quais são elas:
- Fusão: passagem do estado sólido para o estado líquido por meio de aquecimento.
- Vaporização: passagem do estado líquido para o estado gasoso. Esse processo pode acontecer de três formas diferentes:
-
Ebulição: A mudança do estado líquido para o gasoso acontece ao se aquecer o sistema uniformemente, como no caso de uma chaleira em que parte da água evapora de acordo com o aquecimento.
-
Calefação: A mudança do estado líquido para o gasoso acontece de forma súbita, pois o material sofre uma rápida e significativa mudança de temperatura. Um exemplo é quando a gota d’água cai sobre uma chapa quente.
-
Evaporação: A mudança acontece gradativamente, pois apenas a superfície de contato do líquido com o restante do sistema evapora. Exemplo: secagem de roupas no varal.
- Condensação ou liquefação: passagem do estado gasoso para o estado líquido por meio de resfriamento.
- Solidificação: ocorre ao se reduzir ainda mais a temperatura, resultando no congelamento, isto é, passagem do estado líquido para o estado sólido.
- Sublimação: é a transição do estado sólido ao gasoso sem passar pelo estado líquido. Esse processo acontece quando a substância possui alto ponto de fusão e alta pressão de vapor. Exemplo: gelo-seco e naftalina.
Obs.: Utiliza-se o mesmo termo ou ressublimação para o processo inverso (passagem do estado gasoso para o sólido).
Outros estados físicos
Em 1932, Irving Langmuir, no Prêmio Nobel de Química, agregou o termo plasma a uma condição da matéria que já vinha sendo estudada desde 1879. Trata-se de um estado físico em que as partículas estão muito energizadas, têm um distanciamento entre elas e pouca ou nenhuma ligação entre as moléculas. Essas propriedades são bastante semelhantes às do estado gasoso, só que a energia cinética de um plasma é muito maior que a de um gás.
Esse tipo de condição da matéria não é comum na natureza terrestre, no entanto é abundante no Universo, visto que as estrelas são basicamente bolas de plasma em altas temperaturas. Artificialmente já se consegue manipular e agregar valor ao plasma, que é utilizado, inclusive, comercialmente em TVs de plasma, lâmpadas fluorecentes, condutores de LED, entre outros.
Em 1995, o condensado de Bose-Einstein foi estabelecido como um estado físico da matéria. Eric Cornell e Carl Weiman, utilizando ímãs e lasers, resfriaram uma amostra de rubídio, um metal alcalino, até que a energia entre as partículas estivesse próxima de zero. Experimentalmente, notou-se que as partículas se uniram, deixando de ser vários átomos e passando a se comportar em unidade, como um “superátomo”.
O condensado de Bose-Einstein tem características de um superfluido (fluido sem viscosidade e alta condutividade elétrica) e tem sido usado em estudos quânticos para investigar os buracos negros e o paradoxo de partículas-ondas.
Leia também: Diferença entre lâmpadas fluorecentes e incandescentes
Exercícios resolvidos
Questão 1- (Facimpa) Observe:
I – Uma pedra de naftalina deixada no armário.
II – Uma vasilha de água deixada no freezer.
III- Uma vasilha de água deixada no fogo.
IV – O derretimento de um pedaço de chumbo quando aquecido.
Nesses fatos estão relacionados corretamente os seguintes fenômenos:
A) I. Sublimação; II. Solidificação; III. Evaporação; IV. Fusão.
B) I. Sublimação; II. Sublimação; III. Evaporação; IV. Solidificação.
C) I. Fusão; II. Sublimação; III. Evaporação; IV. Solidificação.
D) I. Evaporação; II. Solidificação; III. Fusão; IV. Sublimação.
E) I. Evaporação; II. Sublimação; III. Fusão; IV. Solidificação.
Resolução
Alternativa A.
I – Sublimação: A naftalina é um composto apolar e de ponto de ebulição muito alto. Esse composto vai do estado sólido ao gasoso sem passar pelo estado líquido.
II – Solidificação: A água submetida à baixa temperatura do freezer congela, o que quimicamente chamamos de solidificação, que é a passagem do estado líquido para o estado sólido.
III – Evaporação: A água deixada num vasilhame ao fogo sofre um aumento de temperatura. O ponto de ebulição da água é 100°C, sendo assim, quando o sistema atingir essa temperatura, ela começará a evaporar, passando do estado líquido para o estado sólido.
IV – Fusão: O chumbo tem ponto de fusão de 327,5°C, que é uma temperatura relativamente alta; no entanto, o derretimento do chumbo é um processo comum nas indústrias, que nada mais é do que a passagem do estado sólido para o estado líquido.
Questão 2 - (Mackenzie-SP)

Pela análise dos dados da tabela, medidos a 1 atm, podemos afirmar que, à temperatura de 40 ºC e 1 atm:
A) o éter e o etanol encontram-se na fase gasosa.
B) o éter encontra-se na fase gasosa, e o etanol, na fase líquida.
C) ambos se encontram na fase líquida.
D) o éter encontra-se na fase líquida, e o etanol, na fase gasosa.
E) ambos se encontram na fase sólida.
Resolução
Alternativa B. Se o ponto de ebulição é o ponto em que a substância passa para o estado gasoso, o etanol a 40°C ainda estará no estado líquido. Já o éter tem um ponto de ebulição mais baixo, que é 34°C, portanto, a 40°C, estará em estado gasoso.
Questão 3 – (Unicamp) Icebergs flutuam na água do mar, assim como o gelo em um copo com água potável. Imagine a situação inicial de um copo com água e gelo, em equilíbrio térmico à temperatura de 0°C. Com o passar do tempo, o gelo vai derretendo. Enquanto houver gelo, a temperatura do sistema
A) permanece constante, mas o volume do sistema aumenta.
B) permanece constante, mas o volume do sistema diminui.
C) diminui e o volume do sistema aumenta.
D) diminui, assim como o volume do sistema.
Resolução
Alternativa B. A temperatura mantém-se constante até que o iceberg derreta-se por inteiro, pois acontece uma troca de calor em busca de equilíbrio térmico entre as duas fases da matéria. A água é um dos poucos elementos que admitem densidade diferente para diferentes estados físicos do mesmo composto.
Visualmente podemos verificar que a densidade do gelo é menor. No caso do iceberg e em um copo com água e gelo, o gelo fica na superfície. Isso acontece porque, ao se congelar a água, no processo de formação do gelo, ela ganha volume, mas a massa mantém-se a mesma de quando era água no estado líquido. Portanto, quando o iceberg derrete, ocorre uma diminuição do volume do sistema.
Por Laysa Bernardes Marques de Araújo
Professor de Química





