O etanol é uma substância química, de fórmula C2H6O, pertencente à função orgânica dos álcoois. Comercialmente, é conhecido como álcool etílico, sendo um líquido incolor, inflamável e miscível em água. Possui diversas aplicações industriais, entre elas como solvente e na produção de bebidas alcoólicas, embora sua principal forma de utilização seja como biocombustível.
Oriundo de matrizes vegetais, o etanol é produzido basicamente por fermentação de açúcares. É um biocombustível e gera menos dióxido de carbono para a atmosfera se comparado à gasolina, uma de suas grandes vantagens.
Contudo, o etanol nem sempre possui um preço competitivo e tem seu valor atrelado a outros fatores. No Brasil, o etanol começou a ser utilizado no começo do século XX e teve um grande levante com a introdução dos veículos flex fuel no mercado.
Leia também: Biomassa — a matéria orgânica destinada à fabricação de biocombustíveis e à produção de energia
Tópicos deste artigo
- 1 - Resumo sobre etanol
- 2 - O que é etanol?
- 3 - Para que serve o etanol?
- 4 - Produção do etanol
- 5 - Quais são as vantagens e desvantagens do etanol?
- 6 - Etanol no Brasil
- 7 - Quais são os efeitos do etanol para saúde?
- 8 - Diferenças entre etanol e álcool
Resumo sobre etanol
- O etanol é uma substância química de fórmula C2H6O.
- Pertence à função orgânica dos álcoois e é conhecido como álcool etílico comercialmente.
- É um líquido incolor, miscível em água e outros solventes, além de inflamável.
- É utilizado como solvente na indústria química, além de ser utilizado na fabricação de bebidas alcoólicas.
- Seu principal uso se dá como biocombustível, obtido de matrizes vegetais, como cana-de-açúcar e milho.
- O etanol é produzido pela fermentação de açúcares, principalmente.
- Sua grande vantagem está no aspecto ambiental, pois sua matriz vegetal retira gás carbônico da atmosfera.
- Sua principal desvantagem está na dependência dos fatores climáticos para uma boa produção.
- O etanol começou a ser introduzido na matriz energética brasileira no começo do século XX.
O que é etanol?
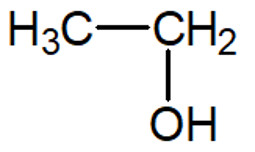
O etanol é uma substância química pertencente à função orgânica dos álcoois. Possui a seguinte fórmula: C2H6O. Às vezes é representado como C2H5OH.
Comercialmente, é conhecido como álcool etílico. É um líquido incolor; inflamável; miscível em água, éter etílico, propanona e clorofórmio; e solúvel em hidrocarbonetos.
Alguns dados pertinentes:
- Massa molar: 46,068 g.mol-1.
- Ponto de fusão: -114,14 °C.
- Ponto de ebulição: 78,24 °C.
- Densidade: 0,7893 g.cm-3.
Para que serve o etanol?
Quando se fala em etanol, pensa-se nos seus dois usos cotidianos mais comuns: produção de bebidas alcoólicas e como biocombustível. Contudo, a utilização desse composto é muito mais ampla. Não à toa, quase 110 bilhões de litros foram produzidos no mundo todo no ano de 2019.
Industrialmente, o etanol é um solvente de grande utilização, com preço favorável e sendo precursor de diversos compostos orgânicos. Ele é utilizado na produção de tintas, solventes, produtos de limpeza, detergentes, entre outros.
Ainda dentro da indústria, mas mais especificamente no campo de cosméticos, o álcool etílico é empregado na fabricação de perfumes, desodorantes, cremes diversos e produtos de higiene. Inclusive, no contexto da pandemia de covid-19, o álcool etílico hidratado 70% se mostrou um excelente agente limpante, servindo para a higienização das mãos em alternativa ao sabão.

E os seus usos atrelados à saúde não terminam na parte de higienização. O etanol também é aplicado em formulação de vacinas, antibióticos e antissépticos. No campo alimentício, além das bebidas alcoólicas, o etanol também está presente no vinagre, produto que também tem crescido no campo da limpeza.
Como biocombustível, o etanol é aplicado em motores de combustão interna com ignição por centelha (ciclo Otto), sendo uma alternativa mais ambientalmente adequada à gasolina e demais combustíveis fósseis.
Produção do etanol
Os principais produtores de etanol no mundo são os Estados Unidos e o Brasil. Os estadunidenses produzem mais da metade do etanol mundial, enquanto o Brasil ronda os 30% desse índice.
A forma mais comum de produção de etanol é por meio da fermentação de açúcares, tais como sacarose, frutose e glicose, encontrados em vegetais como o milho, a beterraba e a cana-de-açúcar, sendo esta a principal matéria-prima de etanol para o Brasil.
Inicialmente, a cana-de-açúcar deve ser limpa, de modo a retirar detritos ou quaisquer impurezas indesejadas. A partir daí, a cana segue para a moagem, onde será produzido um líquido chamado de melado. O rejeito desse processo é sólido, conhecido como bagaço. Enquanto o melado segue para a fabricação, o bagaço serve para a produção de energia.
O melado é purificado por decantação e fermentado por ação das leveduras, com produção de uma mistura de leveduras, açúcares não fermentados e etanol chamada de vinho fermentado.
Essa mistura segue para um processo de destilação, a fim de purificar o etanol. Nesse processo, é formado etanol anidro com cerca de 4% de água. Nessa forma, o etanol já pode ser usado como combustível.
Porém, para a fabricação de etanol anidro sem água, a substância segue para um processo de desidratação, em que o etanol atinge teores mínimos de 99,5%. O fluxograma a seguir apresenta um resumo do processo de produção do etanol.
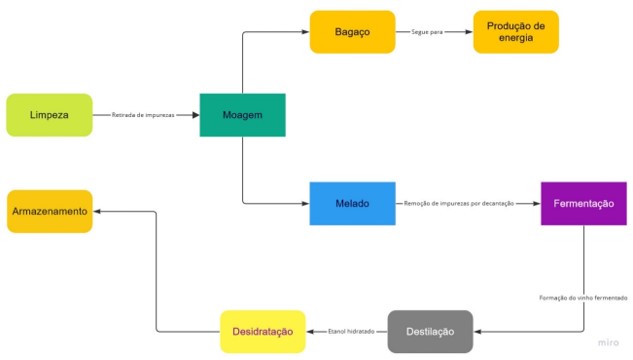
Veja também: Óleo diesel — um combustível fóssil obtido por meio da destilação do petróleo
Quais são as vantagens e desvantagens do etanol?
Uma das principais vantagens do etanol como combustível está na compensação de CO2 que ele é capaz de fazer. A matriz vegetal de que se extrai o etanol, por meio de fotossíntese, retira gás carbônico do ambiente durante seu processo de produção.
Dados trazidos pelo Centro Nacional das Indústrias do Setor Sucroenergético e Biocombustíveis apontam que a utilização do etanol evitou que mais de 515 milhões de toneladas de CO2 fossem jogadas na atmosfera desde o início dos carros flex no Brasil, em 2003.
Um estudo da Embrapa também aponta que a produção e o consumo de etanol de cana-de-açúcar brasileira emitem 73% a menos de dióxido de carbono se comparados aos processos de obtenção e queima de gasolina.
O fato de ser oriundo de uma matriz vegetal também coloca o etanol como renovável, ou seja, sua matriz é inesgotável.
Do ponto de vista energético, entretanto, o poder calorífico do etanol é menor que da gasolina, por exemplo, fazendo com que o consumidor não o utilize se o preço não for competitivo. Pelos dados de poder calorífico, calcula-se que o etanol só é mais viável que a gasolina se o preço do seu litro for inferior a 70% do preço do litro da gasolina.
O preço do etanol está atrelado a alguns fatores regulatórios do mercado internacional. Quando o preço do petróleo aumenta, é comum que a demanda por etanol combustível aumente, diminuindo a oferta e assim fazendo com que o produtor eleve seu preço.

Outro ponto que afeta o preço do etanol está nos níveis atingidos pela safra de sua matriz vegetal. Ciclos de adversidades climáticas impactam diretamente a produção, como períodos de seca e estiagem, diminuindo assim a área de cultivo.
No caso brasileiro, o etanol também concorre com o açúcar, outro importante produto extraído da cana. Valorizações do produto no exterior impactam na produção do etanol combustível, diminuindo assim a disponibilidade de cana-de-açúcar para produção de álcool.
Etanol no Brasil
O etanol começou a ser introduzido na matriz energética brasileira no começo do século XX, como consequência de sucessivas crises no setor açucareiro e como tentativa da redução de dependência do petróleo importado.
Em 1933, o então presidente Getúlio Vargas criou o Instituto de Álcool e Açúcar (IAA), e em 1938, a Lei 737 obrigou a adição de etanol anidro à gasolina produzida no país.
Entretanto, o grande avanço do etanol como combustível ocorreu em 1975, com o lançamento do Programa Nacional do Álcool (Proálcool), com o objetivo de diminuir a dependência em relação ao petróleo importado.
Àquela altura, o Brasil importava cerca de 80% de seu petróleo consumido, correspondendo a aproximadamente 50% de sua balança comercial. A década de 1970, aliás, ficou marcada por duas grandes crises petrolíferas, uma em 1973 e outra em 1979.
Contudo, o etanol não era tão competitivo, e exigiam-se subsídios para que fosse devidamente colocado no mercado. O fim do regime militar fez com que os subsídios também cessassem, e, assim, na segunda metade da década de 1980, houve uma diminuição da participação desse biocombustível.
No governo Collor, o IAA foi extinto, e os subsídios à produção de açúcar também foram retirados, tornando o Brasil um grande exportador de açúcar.
O etanol sofreu um novo impulso com a introdução dos veículos flex fuel em 2003. Uma redução drástica nos seus custos de produção e o aumento internacional do valor do petróleo fez com que o etanol tomasse destaque como grande competidor da gasolina.
Quais são os efeitos do etanol para saúde?
Poucos são os dados referentes aos riscos à saúde humana por exposição ao etanol. De fato, a inalação de vapores pode ser irritante para garganta, olhos e nariz, causando também cefaleia, fadiga e sonolência.
Contudo, a ingestão pode trazer grandes problemas, como visão embaçada, diminuição da coordenação motora, dificuldade na fala, apagões, náuseas, vômitos. A ingestão em grandes quantidades pode até causar convulsões, coma e problemas respiratórios.
Por ser um líquido inflamável, o etanol deve ser manipulado com cautela perto de chamas. O etanol, por sua grande disponibilidade, lidera os índices de causa de queimaduras, porque muitas pessoas o utilizam para cozinhar.
Diferenças entre etanol e álcool
Apesar de, no cotidiano, utilizarmos etanol e álcool como sinônimos, na Química não se deve fazê-lo. Segundo a Iupac, álcool é um termo utilizado para designar compostos que possuem o grupo hidroxila (OH) ligado a um carbono saturado (que só faz ligações simples, de hibridação sp3).
O etanol é um desses compostos, com dois carbonos na cadeia. Contudo, diversos são os álcoois existentes, por isso não se deve utilizar, em Química, os termos como sinônimos.
Crédito de imagem
Vinicius R. Souza / Shutterstock
Por Stéfano Araújo Novais
Professor de Química




