O objetivo deste texto é falar sobre as fórmulas dos ácidos segundo a teoria de Arrhenius, a qual diz que ácido é toda substância que, quando adicionada à água, ioniza-se e produz o cátion hidrônio (representado por H+ ou H3O+) e um ânion (X-) qualquer.
![]()
Equação de ionização de um ácido qualquer
Com base na definição de Arrhenius, a fórmula dos ácidos apresenta um padrão característico, que é HyX. Dessa forma, o que diferencia um ácido de outro, em relação às suas fórmulas, é o tipo de ânion (X) e a quantidade de hidrogênios (y).
Ânions
Os ânions utilizados na construção da fórmula dos ácidos podem apresentar cargas -1 (monovalentes), -2 (bivalentes), -3 (trivalentes) ou -4 (trivalentes). Veja os principais ânions que comumente fazem parte da fórmula de um ácido:
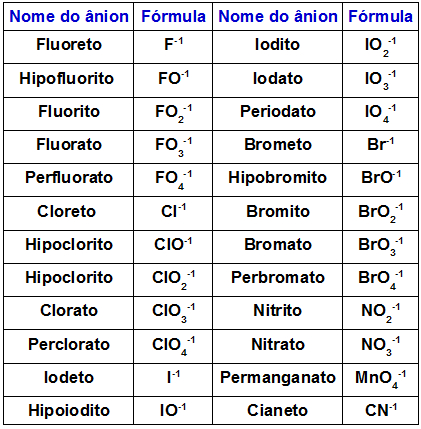
Tabela com os principais ânions monovalentes

Tabela com os principais ânions bivalentes

Tabela com os principais ânions trivalentes

Tabela com os principais ânions tetravalentes
Quantidade de hidrogênios na fórmula do ácido
A quantidade de hidrogênios (y) na fórmula de um ácido depende exclusivamente do tipo de ânion que ele apresenta. Assim, na fórmula do ácido, teremos:
-
Apenas um hidrogênio (y = 1), se o ânion for monovalente;
-
Dois hidrogênios (y = 2), se o ânion for bivalente;
-
Três hidrogênios (y = 3), se o ânion for trivalente;
Anuncie aqui -
Quatro hidrogênios (y = 4), se o ânion for tetravalente.
Exemplos de construção de fórmulas de ácidos
→ Fórmula do ácido sulfuroso
Como o nome do ácido termina com o termo oso e ele sempre substitui a terminação ito de um ânion, temos o ânion bivalente sulfito (SO3-2). A fórmula do ácido é H2SO3.
→ Fórmula do ácido piroarsênico
Como o nome do ácido termina com o termo ico e ele sempre substitui a terminação ato de um ânion, temos o ânion tetravalente piroarsenato (As2O7-4). A fórmula do ácido é H4As2O7.
→ Fórmula do ácido fluorídrico
Como o nome do ácido termina com o termo ídrico e ele sempre substitui a terminação eto de um ânion, temos o ânion monovalente fluoreto (F-1). A fórmula do ácido é HF.
→ Fórmula do ácido sulfídrico
Como o nome do ácido termina com o termo ídrico e ele sempre substitui a terminação eto de um ânion, temos o ânion bivalente sulfeto (S-2). A fórmula do ácido é H2S.
→ Fórmula do ácido oxálico
Como o nome do ácido termina com o termo ico e ele sempre substitui a terminação ato de um ânion, temos o ânion bivalente oxalato (C2O4-2). A fórmula do ácido é H2C2O4.
→ Fórmula do ácido permangânico
Como o nome do ácido termina com o termo ico e ele sempre substitui a terminação ato de um ânion, temos o ânion monovalente permanganato (MnO4-1). A fórmula do ácido é HMnO4.
Por Me. Diogo Lopes Dias