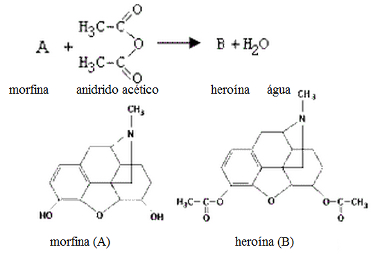
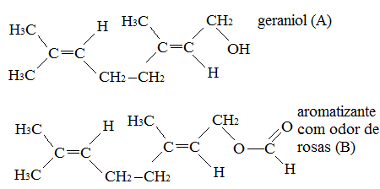
Esterificação é um processo reacional que objetiva a produção de ésteres com base em ácidos carboxílicos (ou derivados) e álcoois (ou fenóis). Tal reação se utiliza de um mecanismo que junta uma adição nucleofílica ao carbono acílico (carbonílico), seguido de uma eliminação.
A esterificação catalisada por um ácido é conhecida como esterificação de Fischer. Distingue-se da saponificação, pois esta se trata de uma hidrólise em meio básico, bem como da transesterificação, que se trata de uma alcoólise.
A esterificação é de grande importância para a indústria alimentícia, pois os ésteres têm função flavorizante, mimetizando sabores e aromas de alimentos naturais, como frutas. Na indústria farmacêutica, pode ser empregada para a síntese do ácido acetilsalicílico, um importante fármaco sintético, além de alguns anti-inflamatórios. Também pode ser empregada na polimerização, assim, produzindo os chamados poliésteres.
Leia também: Reações orgânicas — quais os principais tipos?
Tópicos deste artigo
- 1 - Resumo sobre esterificação
- 2 - Videoaula sobre esterificação
- 3 - O que é a reação de esterificação?
- 4 - Como acontece a reação de esterificação?
- 5 - Uso da esterificação no cotidiano
- 6 - Esterificação de Fischer
- 7 - Qual a diferença entre esterificação e saponificação?
- 8 - Reações de transesterificação
- 9 - Exercícios sobre esterificação
Resumo sobre esterificação
- A reação de esterificação consiste na produção de éster com base em um ácido carboxílico (ou um derivado) com álcool ou fenol.
- Essa reação ocorre por um mecanismo de adição nucleofílica seguido por uma eliminação no carbono acílico (carbonílico).
- Os ésteres podem ser usados na indústria alimentícia, na indústria farmacêutica e na fabricação de polímeros sintéticos.
- A esterificação de Fischer é uma modalidade de esterificação, em que um ácido carboxílico reage com álcool ou fenol, catalisada por ácido.
- Saponificação não é uma esterificação e sim uma hidrólise básica.
- Transesterificação também não é uma esterificação de fato, sendo considerada uma alcoólise. Nesta, um éster é convertido em um novo éster.
Videoaula sobre esterificação
O que é a reação de esterificação?
Considera-se uma reação de esterificação um processo químico para a síntese de ésteres. A formação do éster ocorre pela reação entre um ácido carboxílico (também podendo ser um cloreto de ácido carboxílico ou um anidrido de ácido carboxílico) com álcool ou fenol.
Como acontece a reação de esterificação?
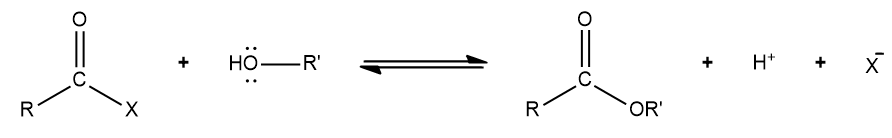
As esterificações ocorrem por meio de adições nucleofílicas seguidas por eliminação no carbono acílico (carbonílico) do ácido carboxílico (ou seu derivado). Isso porque esse carbono apresenta uma carga parcial positiva, dada a maior eletronegatividade dos átomos do oxigênio ao qual ele se encontra ligado, fazendo com que se torne deficitário de densidade eletrônica, e, assim, torna-se propenso ao ataque de nucleófilos (espécies que se atraem por regiões ou cargas positivas).

O ataque nucleofílico ao carbono da carbonila dá origem a um intermediário tetraédrico, já que a hibridização do carbono muda de sp2 para sp3. Tal movimento reacional é também facilitado por outros dois motivos: o carbono da carbonila está mais disponível espacialmente (algo que os químicos entendem como baixo impedimento estérico) e a alta eletronegatividade do oxigênio lhe permite acomodar um par de elétrons da ligação dupla carbono-oxigênio.
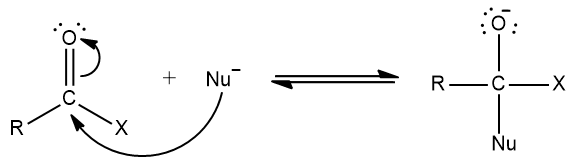
Ocorre que o intermediário tetraédrico é instável, uma vez que o grupo X, representado na imagem anterior, é também eletronegativo. Contudo, tanto o ácido carboxílico quanto seus derivados, propensos à reação descrita, têm a eliminação da espécie X facilitada, já que essa é uma base fraca de Lewis e, uma vez em solução, apresenta baixa reatividade, não realizando um novo ataque nucleofílico ao composto formado.
Com a espécie X sendo eliminada, há também o restabelecimento da ligação π por parte do oxigênio. Assim, na prática, vemos uma substituição do carbono acílico.
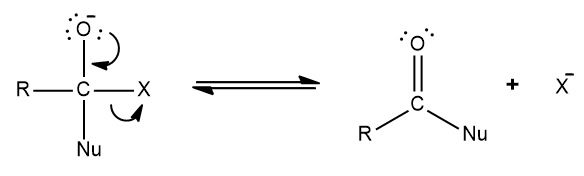
Nas esterificações, o nucleófilo pode ser um álcool ou um fenol. No caso, o ataque nucleofílico ao carbono acílico é feito pelo oxigênio do grupo hidroxila, que apresenta pares de elétrons desemparelhados.
Uso da esterificação no cotidiano
→ Na indústria alimentícia
Os ésteres são utilizados como flavorizantes na indústria alimentícia, ou seja, substâncias capazes de mimetizar sabor e odor de alimentos, tais como frutas. Assim, são comumente aplicados como aditivos, realçando o aroma de uma bebida ou alimento. A tabela a seguir traz exemplos de alguns sabores ou aromas capazes de ser produzidos por ésteres.
|
Éster |
Aroma/sabor |
|
Butanoato de etila |
Abacaxi |
|
Metanoato de isobutila |
Framboesa |
|
Metanoato de etila |
Pêssego |
|
Etanoato de pentila |
Pêra |
|
Etanoato de octila |
Laranja |
|
Etanoato de etila |
Maçã |
|
Etanoato de isobutila |
Morango |
|
Butanoato de butila |
Damasco |
|
Heptanoato de etila |
Vinho |
→ Na indústria farmacêutica
Na indústria farmacêutica, podem estar presentes no revestimento de cápsulas ou em princípios ativos. O ácido acetilsalicílico (AAS) — um dos primeiros fármacos a serem produzidos em laboratório e comercializado sob o nome de Aspirina, com propriedades anti-inflamatórias e antipirética — é produzido via esterificação do ácido salicílico com o anidrido acético, sob aquecimento.
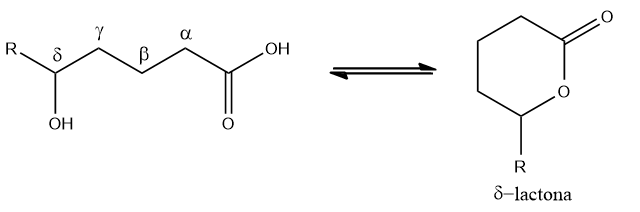
Ainda na indústria farmacêutica, existem também os ésteres cíclicos, conhecidos como lactonas. Tais compostos são produzidos via esterificação intramolecular de ácidos carboxílicos que tenham uma hidroxila em carbono gama (γ) ou delta (δ) em relação à carbonila. Podem ser empregados na fabricação de alguns antibióticos, como a eritomicina e a nonactina. A vitamina C, ácido ascórbico, é também uma lactona.
→ Outras aplicações da esterificação

Os ésteres também compõem uma classe de polímeros sintéticos, os poliésteres. Destacam-se os ésteres polivinílicos, utilizados em tintas e vernizes. Outro poliéster de grande destaque é o politereftalato de etileno, o PET, amplamente empregado na fabricação de garrafas, embalagens, fibras, filmes fotográficos, entre outros usos. Os poliésteres também estão presentes em fibras têxteis, assim, são utilizados na fabricação de tecidos.
Veja também: Como ocorre uma reação de polimerização
Esterificação de Fischer
A esterificação de Fischer (assim chamada por conta de seu desenvolvedor, o cientista Emil Fischer, em 1895, com auxílio de Arthur Speier) consiste em uma esterificação de um ácido carboxílico pela ação de um álcool (ou fenol), catalisada por um ácido (em geral, ácido sulfúrico, H2SO4).
O catalisador, utilizado para acelerar o processo químico, torna-se essencial, pois, na sua ausência, em condições ambiente de temperatura e pressão, a reação se desenvolveria lentamente por conta da possibilidade de reversibilidade. Além disso, tal reação tem a formação de água e é facilitada pela elevação da temperatura.
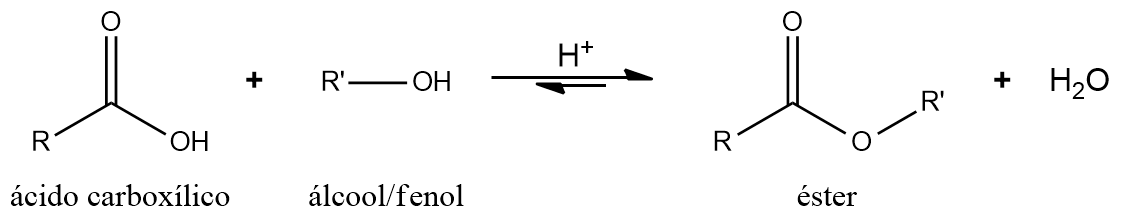
Por conta da reversibilidade, o equilíbrio deve ser deslocado na direção de formação do produto. Entre as estratégias, destacam-se a utilização de excesso de reagentes, a remoção do éster ou a remoção da água, podendo ser tanto por destilação quanto por um agente desidratante. A remoção de água é também importante, pois pode causar hidrólise do éster formado, diminuindo o rendimento reacional.
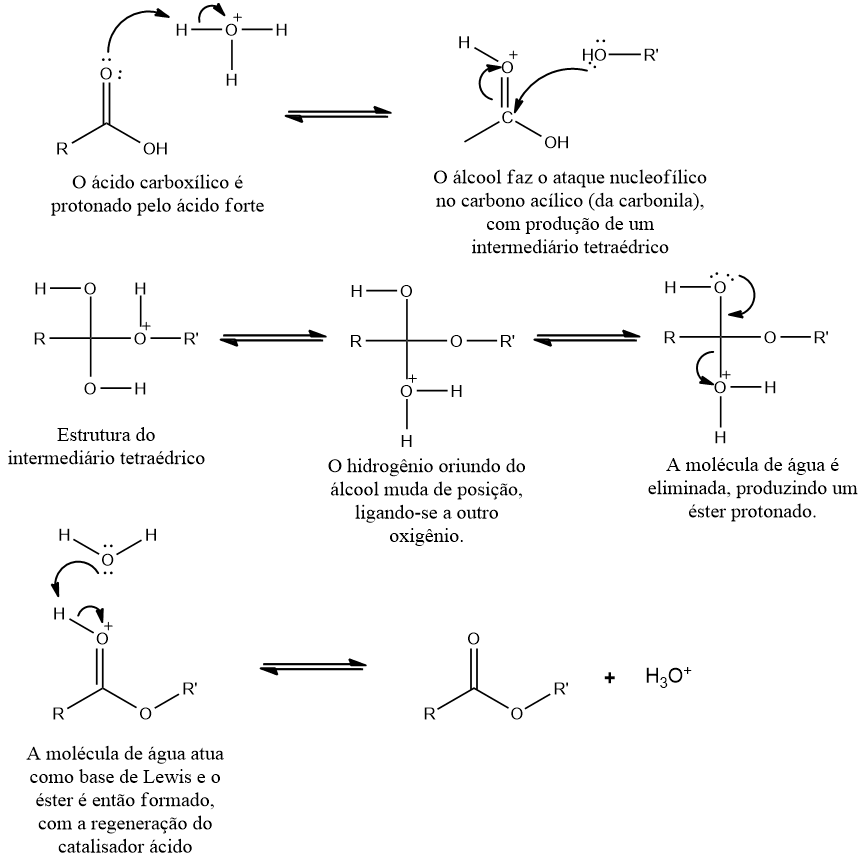
O ácido catalisador precisa ser forte, pois assim impede o ácido carboxílico de estar dissociado no meio. O mecanismo da esterificação de Fischer é o que se segue:
Qual a diferença entre esterificação e saponificação?
A esterificação, como pontuado, é um processo reacional que objetiva a produção do éster por meio da reação entre um ácido carboxílico ou derivado com um álcool ou fenol. Já a saponificação consiste em uma hidrólise do éster em meio básico, produzindo um sal de ácido carboxílico, empregado na fabricação de sabão (por isso o nome saponificação).
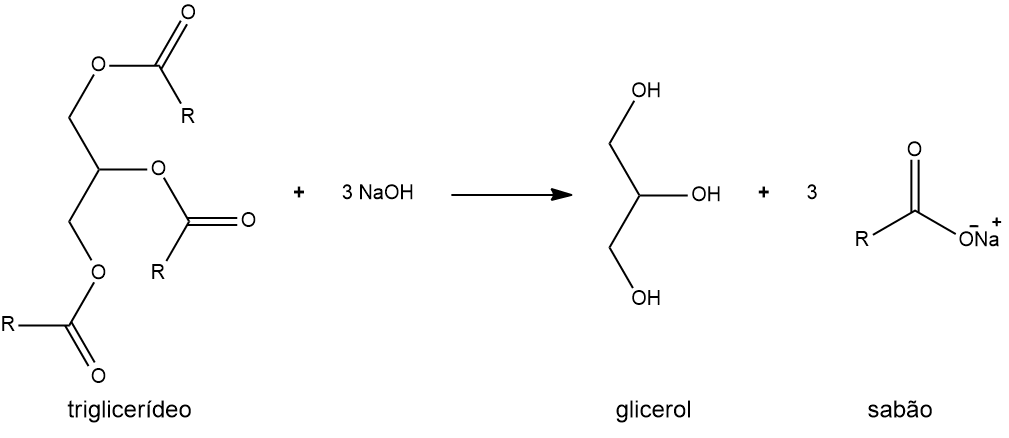
Hidrólise é uma reação em que a molécula do éster é quebrada pela ação da água, o que pode ser tanto em meio ácido quanto em meio básico. Na saponificação, o éster a ser hidrolisado é um triglicerídeo (éster de ácido graxo), tendo como subproduto o glicerol (conhecido como glicerina). Observe o processo a seguir.
Reações de transesterificação
A reação de transesterificação ocorre quando um éster reage com um álcool, na ausência de água (para evitar hidrólise), formando um novo éster e um novo álcool, ou seja, o éster é convertido (transformado) em um outro éster. De modo geral, tal reação se configura como uma alcoólise.
A reação de transesterificação necessita de catalisador, pois ocorre muito lentamente. Isso porque, após o ataque nucleofílico, o éster elimina um alcóxido, uma base de Lewis muito forte e reativa.
A transesterificação é utilizada para síntese de biodiesel. No caso, o éster reagente a ser utilizado é também o triglicerídeo (como na saponificação), com a diferença que são formados novos ésteres (biodiesel) e não sais de ácido carboxílico.
Saiba mais: Como as substâncias catalisadoras atuam?
Exercícios sobre esterificação
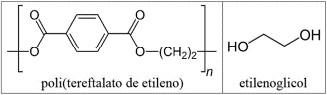
Questão 1. (UnB 2º Dia/2023) Considerando-se o poli(tereftalato de etileno), um polímero de condensação obtido pela esterificação de um monômero com o etilenoglicol, e as fórmulas moleculares constantes da tabela a seguir, é correto afirmar que o monômero que reage com o etilenoglicol, para formar o poli(tereftalato de etileno), é o ácido benzoico.
a) Certo
b) Errado
Resposta: B, errado.
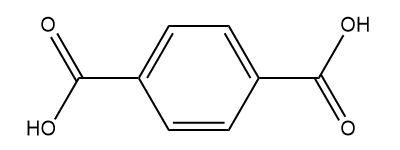
O poli(tereftalato de etileno) apresenta dois grupos carbonila. A carbonila do éster, no processo de esterificação, é oriunda do ácido carboxílico, tendo duas carbonilas; logo, entende-se que o monômero utilizado se tratava de um ácido dicarboxílico. O ácido benzoico é um ácido carboxílico com apenas um único grupo carbonila. O monômero em questão é o ácido representado a seguir, conhecido como ácido tereftálico.
Questão 2. (Unifenas Manhã/2019.1) As essências são usadas na indústria alimentícia porque são capazes de conferir variados aromas e sabores aos produtos artificiais. Nos alimentos naturais, o sabor depende de uma série de compostos químicos como os açúcares, responsáveis pelos sabores adocicados e os ácidos, que dão o sabor azedo. Já nos alimentos industrializados, é preciso usar extratos naturais ou flavorizantes para se chegar a um gosto semelhante ao real. Por exemplo, o sabor e aroma de fruta, adicionados aos sucos artificiais, gomas de mascar, bombons, gelatinas, sorvetes e iogurtes, são efeitos das essências de ésteres. Confira alguns exemplos:
- Acetato de pentila: esse aromatizante do grupo de ésteres é responsável pelo aroma artificial de banana nos produtos.
- Etanoato de butila: é a essência que dá o sabor de maçã-verde às gomas de mascar, balas, sucos, entre outros.
- Butanoato de etila: esse é o éster utilizado nos alimentos para fornecer o aroma de abacaxi.
- Metanoato de etila: o metanoato de etila está presente nos itens com aroma artificial de groselha.
- Acetato de propila: a presença desse éter nos alimentos confere-lhes o sabor artificial de pera.
Das reações abaixo, a que representa a formação do éster responsável pelo aroma artificial de groselha é
a) CH3COOH + CH3OH →
b) CH2O + CH3COOH →
c) CH3CH2OH + CH3COOH →
d) CH3CH2OH + HCOOH →
e) HCOOH + CH3OH →
Resposta: Letra D
O responsável pelo aroma artificial de groselha é o metanoato de etila. Na nomenclatura oficial Iupac, a parte do nome que recebe -oato é derivada do ácido carboxílico, enquanto a que recebe o sufixo -ila é derivada do álcool ou fenol. Assim sendo, o ácido carboxílico é o ácido metanóico e o álcool é o etanol.
Fontes
BRUICE, P. Y. Organic Chemistry. 8. ed. Upper Saddle River, Nova Jersey: Pearson Education Inc., 2015.
COSTA, T. S.; ORNELAS, D. L.; GUIMARÃES, P. I. C.; MERÇON, F. Confirmando a Esterificação de Fischer por Meio dos Aromas. Química Nova Na Escola. n. 19, mai. 2004
SOLOMONS, T. W. G.; FRYHLE, C. B.; SNYDER, S. A. Química Orgânica: volumes 1 e 2. 12. ed. Rio de Janeiro: LTC, 2018.
OLIVEIRA, C. A.; SOUZA, A. C. J.; SANTOS, A. P. B.; SILVA, B. V.; LACTHER, E. R.; PINTO, A. C. Síntese de ésteres de aromas de frutas: um experimento para cursos de graduação dentro dos princípios da Química Verde. Revista Virtual de Química. v. 6, n. 1, p. 152-167, 2014.