Uma reação de adição é um processo químico em que átomos de uma substância inorgânica são acrescentados a uma molécula orgânica, a qual deve apresentar obrigatoriamente uma das seguintes características:
-
Estrutura aberta contendo ligação ou ligações pi;
Anuncie aqui -
Estrutura fechada saturada (apenas com ligações sigma);
-
Estrutura fechada insaturada (com uma ligação pi ou aromática).
Os compostos orgânicos que apresentam essas caraterísticas são os seguintes hidrocarbonetos:
-
Anuncie aqui
-
Ciclanos;
-
Ciclenos;
Durante uma reação de adição, ocorre o rompimento de uma ou mais ligações pi, ou de uma ligação sigma (no caso exclusivo de um ciclano), fazendo com que surjam duas ou mais valências livres (sítios de ligação) nos carbonos envolvidos, como no exemplo abaixo:
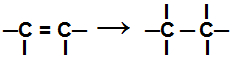
Rompimento da ligação pi em um alceno
Após o rompimento dessa ligação, deve ocorrer a adição dos átomos nos novos sítios de ligação criados no composto orgânico. Listamos a seguir os tipos de reações de adição que podem ser realizados com os compostos orgânicos.
Hidrogenação
Nessa reação de adição, além do composto orgânico, o outro reagente é o gás hidrogênio (H2). Em cada um dos carbonos, onde ocorre a cisão (quebra da ligação sigma ou pi, como visto anteriormente), haverá a ligação de um átomo de hidrogênio referente à quantidade de ligações rompidas.
Quando realizamos a hidrogenação do ciclobutano, por exemplo, uma ligação sigma é rompida entre os carbonos 1 e 2. Em seguida, um átomo de hidrogênio liga-se a cada um desses carbonos:
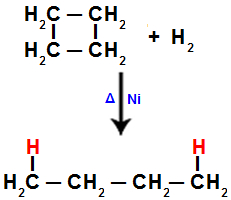
Equação representando a hidrogenação no ciclobutano
Halogenação
Além do composto orgânico, o outro reagente nessa reação de adição é um halogênio molecular (gás cloro-Cl2, gás flúor-F2, iodo sólido-I2 e bromo líquido-Br2). Em cada carbono, onde ocorre a cisão (quebra da ligação sigma ou pi, como visto anteriormente), haverá a ligação de um átomo de halogênio referente à quantidade de ligações rompidas.
Assim, quando realizamos a halogenação (utilizando o gás cloro) do ciclopropeno, a ligação pi é rompida entre os carbonos 1 e 2. Em seguida, um átomo de cloro liga-se a cada um desses carbonos:
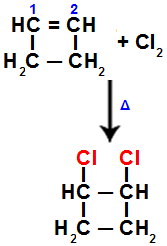
Equação representando a halogenação no ciclopropeno
Reação de adição com halogenidretos
Um halogenidreto é um hidrácido inorgânico, formado por um átomo de hidrogênio e um átomo de halogênio, como o ácido clorídrico (HCl), o ácido fluorídrico (HF), ácido bromídrico (HBr), ácido iodídrico (HI).
Na reação de adição com halogenidreto, além do composto orgânico, o outro reagente é um halogenidreto, por isso um dos carbonos, onde ocorre a cisão (quebra da ligação sigma ou pi, como visto anteriormente), deve receber o átomo de hidrogênio, e o outro recebe o halogenidreto.
De acordo com a regra de Markovnikov, o átomo de carbono mais hidrogenado (ou o carbono ligado a um radical menor) deve receber o hidrogênio, e o carbono menos hidrogenado (ou o carbono ligado a um radical maior) deve receber o halogenidreto.
Por exemplo, quando realizamos essa reação no propeno com o ácido clorídrico (HCl), a ligação pi é rompida entre os carbonos 1 e 2. Em seguida, o hidrogênio liga-se ao carbono 1 (mais hidrogenado) e o cloro ao carbono 2 (menos hidrogenado):
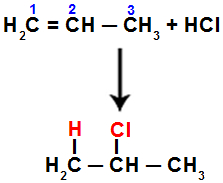
Equação representando a adição com halogenidreto no propeno
Reação de hidratação
A molécula de água, ao ionizar, produz o cátion hidrônio (H+) e o ânion hidróxido (OH-). Por essa razão, nessa reação de adição, além do composto orgânico, o outro reagente é a água. Assim, um dos carbonos, onde ocorre a cisão (quebra da ligação sigma ou pi, como visto anteriormente), recebe o cátion de hidrônio, e o outro recebe o ânion de hidróxido.
De acordo com a regra de Markovnikov, o átomo de carbono mais hidrogenado (ou o carbono ligado a um radical menor) deve receber o hidrônio, e o carbono menos hidrogenado (ou o carbono ligado a um radical maior) deve receber o hidróxido.
Quando realizamos a hidratação do penta-1,4 dieno, por exemplo, a ligação pi é rompida entre os carbonos 1 e 2, e entre os carbonos 4 e 5. Em seguida, os carbonos 1 e 5 recebem o hidrônio, e os carbonos 2 e 4 recebem o hidróxido:
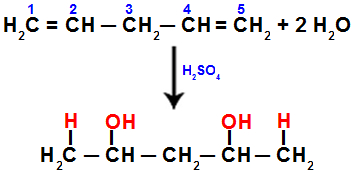
Equação representando a adição com hidratação no penta-1,4 dieno
Por Me. Diogo Lopes Dias