Oxidação energética em alcinos é uma reação orgânica que ocorre quando um alcino (hidrocarboneto que apresenta uma ligação tripla entre dois carbonos) é adicionado a uma solução ácida com o reagente de Baeyer (Permanganato de Potássio - KMnO4).
OBS.: Uma reação de oxidação energética pode ser realizada com o dicromato de potássio (K2Cr2O7), e não apenas com o permanganato de potássio.
Sempre que uma reação de oxidação energética em alcinos é realizada, os produtos que podem ser originados são ácidos carboxílicos, água (o único item que aparece em qualquer uma delas) e dióxido de carbono (CO2).
Reagente Baeyer em meio ácido
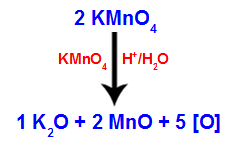
Quando o reagente de Baeyer é misturado com água, na presença de um ácido (substância capaz de liberar íons H+), ocorre a formação de dois óxidos (óxido de potássio e o óxido de manganês II) e oxigênios nascentes ().
Mecanismos da oxidação energética em alcinos
-
1º Mecanismo: quebra da ligação tripla.
Inicialmente, ocorre o ataque à ligação tripla pelos oxigênios nascentes formados pelo reagente de Baeyer. Esse ataque faz com que a ligação tripla seja completamente rompida.
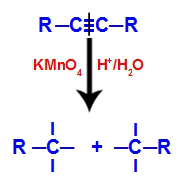
Rompimento da ligação tripla pelo ataque dos oxigênios nascentes
Com o rompimento da ligação tripla, o alcino é dividido em duas partes. Em cada um dos carbonos que estavam realizando a ligação tripla, surgem três valências livres.
-
2º Mecanismo: Interação dos grupos hidroxila
Cada uma das valências livres nos carbonos onde estava a ligação tripla são ocupadas por grupos hidroxila (OH), formando um poliol (álcool com várias hidroxilas).
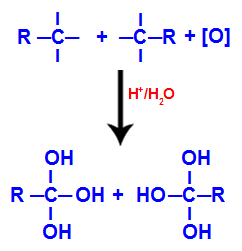
Formação do poliol com grupos hidroxila após a quebra da ligação tripla
OBS.: Caso o carbono onde estava a ligação tripla tenha um átomo de hidrogênio ligado a ele, esse átomo de hidrogênio receberá um oxigênio nascente e também formará mais uma hidroxila.
-
3º Mecanismo: Formação de moléculas de água
Quando um carbono apresenta dois ou mais grupos OH, passa a ser uma estrutura muito instável em virtude da presença de grupos extremamente eletronegativos. Assim, pela instabilidade, a molécula sofre uma autodesidratação, ou seja, uma hidroxila liga-se ao hidrônio (H+) de outra hidroxila e forma água.
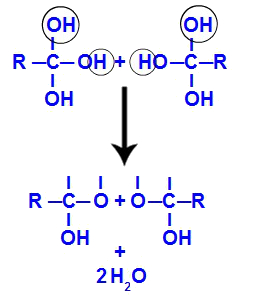
Formação de moléculas de água a partir de duas hidroxilas presentes no poliol formado
-
4º Mecanismo: Formação dos produtos
Após a formação das moléculas de água, o carbono perde uma ligação em virtude da saída de uma hidroxila, e o oxigênio da outra hidroxila também perde uma ligação que estava sendo realizada com um hidrogênio. Logo, entre esse carbono e o oxigênio, surge uma ligação dupla, que forma uma carbonila (C=O) e estabiliza ambos.
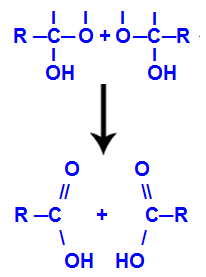
Formação da carbonila nas duas estruturas obtidas a partir doalcino
Exemplo de equação de oxidação energética em alcinos
Exemplo: Oxidação energética do But-1-ino
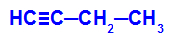
Fórmula estrutural do but-1-ino
Quando o but-1-ino é colocado em um meio que apresenta reagente de Bayer, água e ácido, ocorre o rompimento da ligação tripla existente entre os carbonos 1 e 2, em razão do ataque dos oxigênios nascentes existentes no meio, como na equação abaixo:
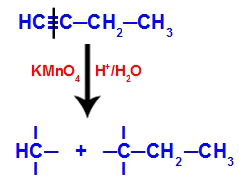
Rompimento das ligações no but-1-ino
Após o rompimento da ligação tripla, os carbonos 1 e 2 recebem três hidroxilas, mas o carbono 1 terá mais uma porque ele apresentava um átomo de hidrogênio (que se liga a um oxigênio nascente), formando dois polióis (fragmento 1 e 2).
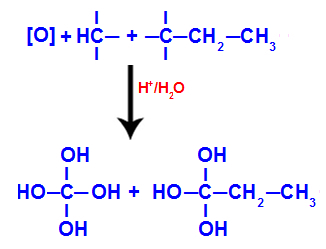
Equação representando a formação dos polióis
Logo em seguida, como os polióis são instáveis, temos a formação de moléculas de água a partir das hidroxilas. No fragmento 1, surge uma molécula de água (por haver três hidroxilas) e, no fragmento 2, surgem duas moléculas (por haver quatro hidroxilas).
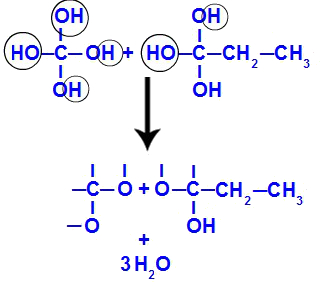
Formação de moléculas de água a partir dos fragmentos do but-1-ino
Por fim, temos a formação da ligação dupla entre o carbonos que perderam hidroxila e os oxigênios que perderam hidrogênio, o que dá origem a carbonilas.
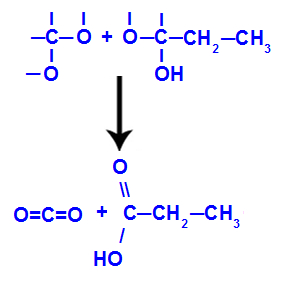
Formação das carbonilas nos fragmentos do but-1-ino
Com a equação acima, podemos observar que o but-1-ino deu origem a um ácido carboxílico e dióxido de carbono (CO2).
Por Me. Diogo Lopes Dias