Um aldeído é todo composto orgânico que possui o grupo carbonila ligado a um hidrogênio, ou seja, o seu grupo funcional sempre vem da extremidade de uma cadeia carbônica e é dado por:
O
│ ║
─ C ─ C ─ H
│
Grupo Funcional
dos Aldeídos
Já as cetonas são aqueles compostos orgânicos que possuem o grupo carbonila entre dois carbonos. Portanto, seu grupo funcional nunca irá aparecer na extremidade de uma cadeia carbônica.
O
│ ║ │
─ C ─ C ─ C ─
│ │
Grupo Funcional
das Cetonas
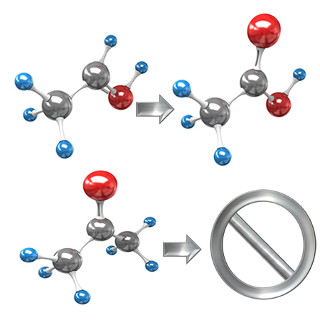
Quando esses dois tipos de compostos são expostos a agentes oxidantes, somente os aldeídos reagem. Isso ocorre porque o carbono ligado ao oxigênio na carbonila adquire caráter positivo, visto que o oxigênio é mais eletronegativo e atrai mais fortemente os elétrons da ligação química.
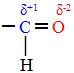
Assim, um oxigênio nascente que estiver no meio irá atacar esse carbono, colocando-se exatamente entre a ligação carbono-hidrogênio. No caso dos aldeídos, forma-se um composto do grupo dos ácidos carboxílicos, e, no caso das cetonas, não há reação, porque seu carbono da carbonila não está ligado a nenhum hidrogênio.
O O
║ ║
R ─ C ─ H + →R ─ C ─ OH
Aldeído Ácido carboxílico
O
║
R ─ C ─ R + →não reage
Cetona
Desse modo, é muito comum em laboratório realizar reações de oxidação para identificar se determinada substância é um aldeído ou uma cetona. Entre os oxidantes que costumam ser usados estão o reativo de Tollens (solução aquosa amoniacal de nitrato de prata), o reativo de Fehling (solução aquosa de sulfato de cobre em meio básico e tartarato duplo de sódio e potássio) e o reativo de Benedict (solução aquosa de sulfato de cobre em meio básico e citrato de sódio).
O reativo de Benedict é usado principalmente em fitas de papel para detectar a presença e concentração de glicose (um poliálcool-aldeído) na urina.
Algo interessante acontece quando se usa o reativo de Tollens para oxidar um aldeído, forma-se um espelho de prata nas paredes do recipiente. Isso acontece porque o aldeído é oxidado a ácido carboxílico, enquanto os íons prata (Ag+) são reduzidos a Ag0 (prata metálica), que se deposita nas paredes do recipiente.
Veja como essa reação pode ser representada no caso do propanal sendo oxidado a ácido propanoico:
O O
║ ║
H3C ─ CH2 ─ C ─ H + H2O → H3C ─ CH2 ─ C ─ OH + 2e- + 2 H+
2 Ag+ + 2e- → 2 Ag0
2 NH3 + 2 H+ → 2 NH4+
O O
║ ║
H3C ─ CH2 ─ C ─ H + 2 Ag+ + 2 NH3 +H2O → H3C ─ CH2 ─ C ─ OH + 2 Ag0 + 2 NH4+
propanal reativo de Tollens ácido propanoico prata metálica
(aldeído) (solução aquosa amoniacal (ácido carboxílico) (espelho de prata)
de nitrato de prata)
Por Jennifer Fogaça
Graduada em Química