Um dos grandes desafios para quem está aprendendo Química se chama distribuição eletrônica. O que vamos apresentar neste contexto pode facilitar em muito seus estudos relacionados à configuração de elétrons proposta pelo cientista Linus Pauling.
O número máximo de elétrons que cabe em cada camada ou nível de energia é dado através da tabela:
Nível de Energia Camada Nº Máximo de elétrons
1° K 2
2° L 8
3° M 18
4° N 32
5° O 32
6° P 18
7° Q 8
A ordem crescente de energia dos subníveis é a ordem na sequência das diagonais. O diagrama de Linus Pauling é representado abaixo:
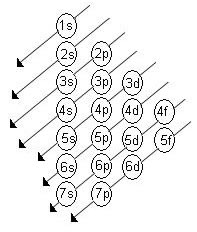
Regras básicas:
1. O número atômico (Z) do elemento, no estado neutro, indica a quantidade de elétrons a ser distribuída. Esse número é representado na parte inferior esquerda, do símbolo do elemento.
2. Utilizando o diagrama de Pauling, comece a distribuir os elétrons de cima para baixo, levando em consideração a ordem crescente de energia (orientada pelo sentido das setas).
3. Preencha os subníveis com o nível máximo de elétrons. Se um determinado subnível só comporta 6 elétrons, não ultrapasse essa quantia.
4. Confira o número de elétrons fazendo a soma dos mesmos em cada subnível.
Vamos colocar em prática?
Distribua os elétrons do átomo de ferro (Z=26).
Se o número atômico é 26, significa que no átomo normal de ferro há 26 elétrons. Aplicando o diagrama de Pauling, teremos:

Por Líria Alves
Graduada em Química