PUBLICIDADE
O ponto de fusão e ebulição são, repectivamente, as temperaturas em que os materiais passam do estado sólido para o líquido e do estado líquido para o gasoso ou a temperatura máxima em que o líquido pode permanecer nesse estado físico em uma determinada pressão.
Os pontos de fusão e ebulição dos elementos químicos da Tabela Periódica variam de acordo com os seus números atômicos, o que significa, então, que são propriedades periódicas.
Na Tabela Periódica, a ordem de crescimento das temperaturas de fusão e ebulição dos elementos químicos segue o seguinte esquema de setas:
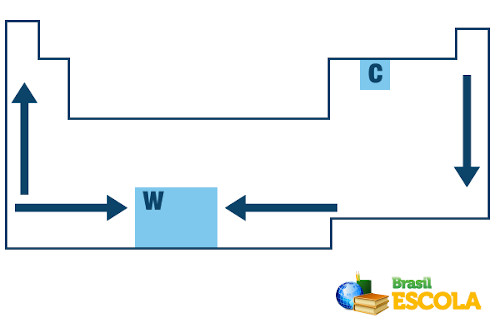
Crescimento do ponto de fusão e de ebulição na Tabela Periódica
Veja que, quando consideramos os elementos pertencentes a uma mesma família do lado esquerdo da Tabela, os pontos de fusão e ebulição diminuem conforme o número atômico do elemento aumenta, ou seja, de baixo para cima. Isso pode ser visto nos valores dos pontos de fusão e ebulição a 1 atm para os elementos da família 1 mostrados a seguir:
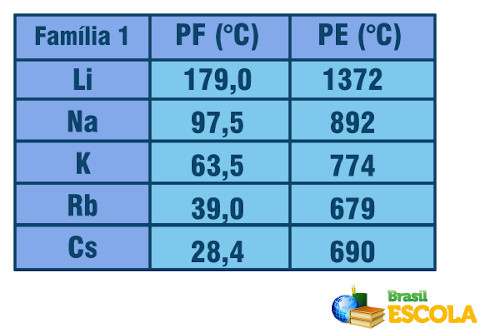
Pontos de fusão e ebulição dos elementos da família 1
Já do lado direito da Tabela Periódica ocorre o contrário, o sentido do crescimento do ponto de fusão e de ebulição dos elementos pertencentes a uma mesma família aumenta de cima para baixo. Por isso, os elementos com menores temperaturas de fusão e ebulição estão situados na parte superior da Tabela. A única exceção é o carbono, que possui um ponto de fusão igual a 3550 ºC e um ponto de ebulição igual a 4287ºC.
Do contrário, a maioria desses que possuem pontos de fusão e ebulição baixos apresenta-se como gases ou como líquidos em temperatura ambiente ao nível do mar. Como é o caso dos gases nobres, do nitrogênio, do oxigênio, do flúor e do cloro, que estão na parte superior à direita na Tabela.
Agora, quando se trata de elementos pertencentes ao mesmo período (mesma linha na Tabela), vemos que os pontos de fusão e ebulição aumentam das laterais para o centro da Tabela. Veja o exemplo para os elementos do segundo período:
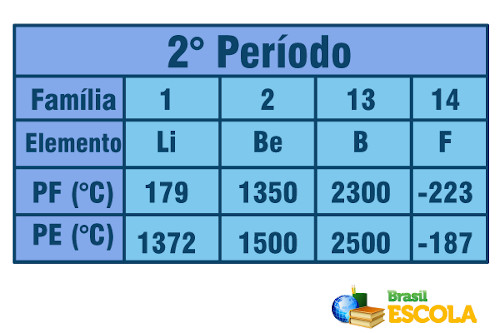
Ponto de fusão e ponto de ebulição para os elementos do segundo período da Tabela Periódica
O tungstênio (W) é um elemento que fica no centro da Tabela Periódica e o seu ponto de fusão é o maior entre os metais, sendo igual a 3422ºC. É por isso que ele é usado nos filamentos de lâmpadas incandescentes, pois consegue suportar altas temperaturas sem derreter.
Por Jennifer Fogaça
Graduada em Química





