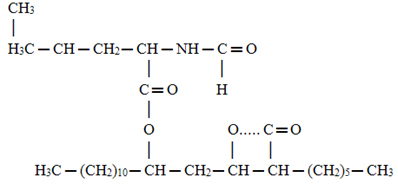
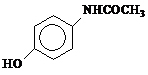
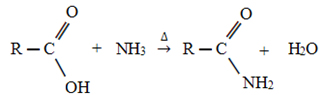As amidas são compostos orgânicos caracterizados pela presença de um nitrogênio (N) ligado diretamente a uma carbonila (C=O). São substâncias disponíveis de forma natural, uma delas é nas excretas dos mamíferos (ureia), mas podem ser obtidas também por síntese artificial.
As amidas podem ser produzidas, por exemplo, por desidratação do sal de amônio, processo utilizado na fabricação de polímeros. São utilizadas também como fertilizantes, devido a sua disponibilidade de nitrogênios, e como medicamento, tendo ação antimicrobiana.
Leia mais: Acrilamida – amida que pode ser originada do aquecimento de alguns alimentos
Tópicos deste artigo
- 1 - Estrutura das amidas
- 2 - Classificação das amidas
- 3 - Nomenclatura das amidas
- 4 - Propriedades das amidas
- 5 - Aplicação das amidas
- 6 - Obtenção das amidas
- 7 - Exercícios resolvidos
Estrutura das amidas
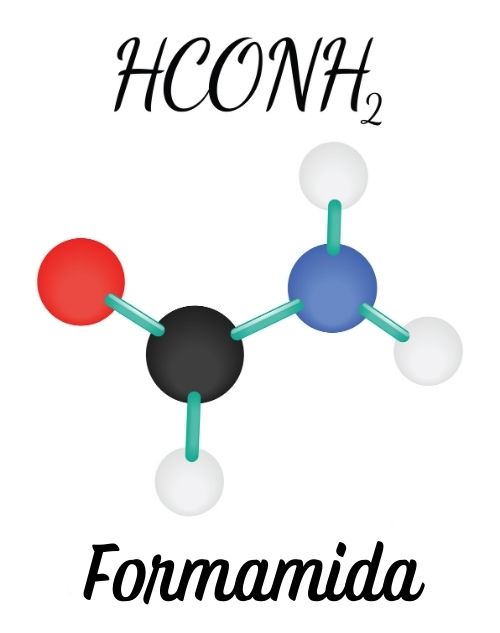
As amidas são formadas por um nitrogênio ligado diretamente a uma carbonila ou grupo acila (R-C=O). A dupla ligação entre o carbono e o oxigênio e a possibilidade da movimentação dessa dupla para o nitrogênio conferem à molécula geometria planar, diferentemente das aminas, que possuem geometria piramidal.
Classificação das amidas
-
Classificação de acordo com o número de substituintes orgânicos
Assim como as aminas, as amidas são classificadas de acordo com o número de radicais orgânicos substituintes que o nitrogênio tiver, porém, para as amidas, temos que considerar que um dos ligantes do grupo obrigatoriamente será o grupo acila, ou seja, teremos apenas amidas do tipo:
- Amida não substituída: possui o nitrogênio ligado a dois hidrogênios e um grupo carbonila.
Exemplo:
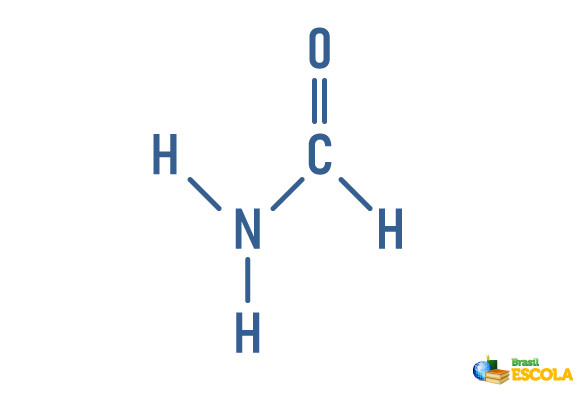
- Amina monosubstituída: possui o nitrogênio ligado a um hidrogênio, um grupo carbonila e um radical orgânico. Nesse caso, em que um dos hidrogênios foi substituído por uma cadeia carbônica, considere R como um grupo orgânico.
Exemplo:
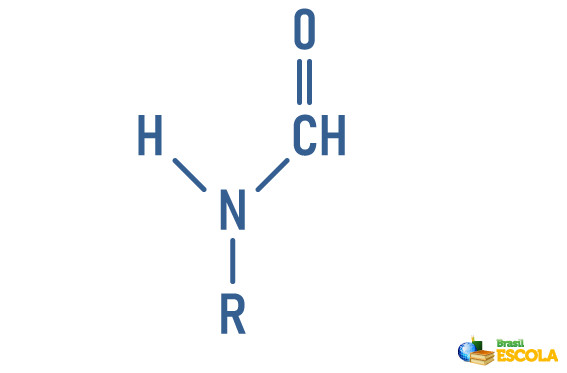
- Amina dissubstituída: possui o nitrogênio ligado a dois radicais orgânicos e a uma carbonila. Nesse caso, os dois hidrogênios foram substituídos por cadeias carbônicas.
Exemplo:
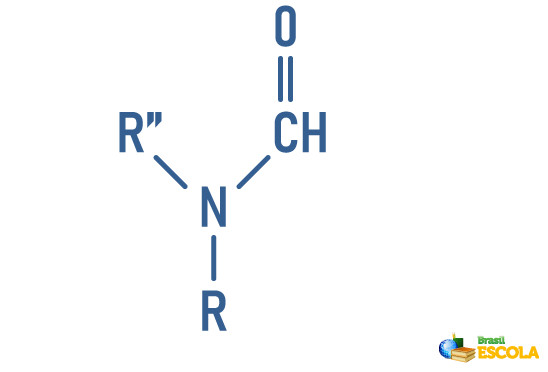
Veja também: Como classificar os haletos orgânicos?
-
Classificação de acordo com o número de carbonilas ligadas ao nitrogênio
As amidas podem ser classificadas também de acordo com o número de carbonilas ligadas diretamente ao nitrogênio da molécula.
- Amidas primárias: apenas um grupo acila ligado ao nitrogênio (R-CO)NH2 .
- Amidas secundárias: duas carbonilas ou grupo acila ligado ao nitrogênio (R-CO)2NH.
- Amidas terciárias: três grupos acilas ligados ao nitrogênio (R-CO)3N.
Nomenclatura das amidas
A nomenclatura para amidas será dada por:
|
prefixo indicativo de número de carbonos na cadeia + localização e infixo indicando insaturações (quando houver) + terminação amida |
Veja o quadro a seguir:
|
Prefixo (n° de carbonos) |
Infixo (saturação da cadeia) |
Sufixo (grupo funcional) |
|||
|
1 carbono |
Met- |
Apenas ligações simples |
-an- |
Amidas |
-amida |
|
2 carbonos |
Et- |
||||
|
3 carbonos |
Prop- |
1 ligação dupla |
-en- |
||
|
4 carbonos |
But- |
||||
|
5 carbonos |
Pent- |
2 ligações duplas |
-dien- |
||
|
6 carbonos |
Hex- |
||||
|
7 carbonos |
Hept- |
1 ligação tripla |
-in- |
||
|
8 carbonos |
Oct- |
||||
|
9 carbonos |
Non- |
2 ligações triplas |
-diin- |
||
|
10 carbonos |
Dec- |
||||
A contagem dos carbonos deve iniciar-se pelo lado mais próximo do nitrogênio do grupo funcional.
Exemplos:
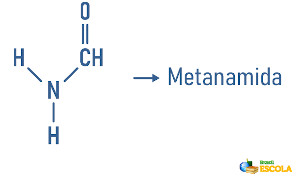

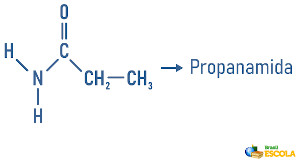
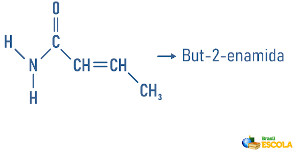
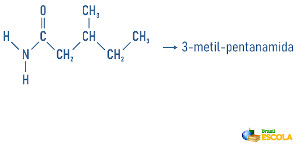
As aminas podem ainda receber em sua nomenclatura uma especificação sobre a classificação da molécula:
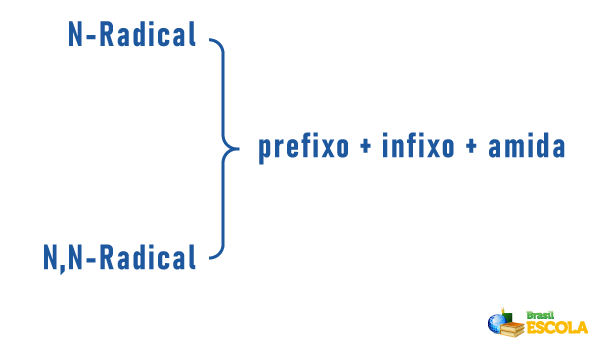
Lembrando que nomenclatura para radicais é formada por: prefixo indicando número de carbonos + terminação “il” ou “ila”. Os radicais posicionam-se na nomenclatura em ordem alfabética.
Exemplos:
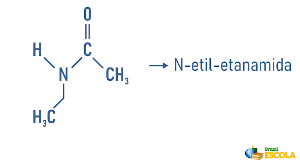
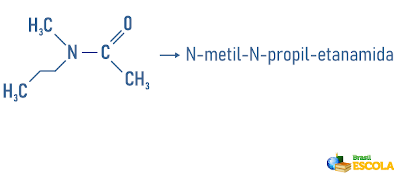
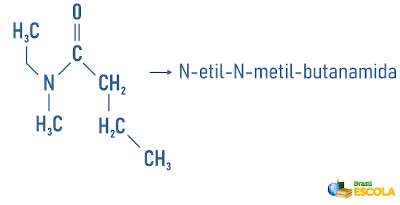
Acesse também: Nomenclatura de hidrocarbonetos cíclicos e ramificados
Propriedades das amidas
- Elevado ponto de fusão e ebulição, que terá valor escalonado de acordo com o tamanho e arranjo espacial da cadeia carbônica.
- Altamente polares, devido à presença da carbonila e do nitrogênio.
- Amidas não substituídas e monossubstituídas realizam ligação de hidrogênio.
- Moléculas menores e mais simples são solúveis em água. O tamanho da molécula interfere também na solubilidade das amidas: quanto maior a cadeia carbônica, menos solúvel elas serão em água.
- As amidas têm caráter básico pela propensão a receberem íons H+.
Aplicação das amidas
- Utilizadas como intermediadoras na fabricação de polietilenos como nylon.
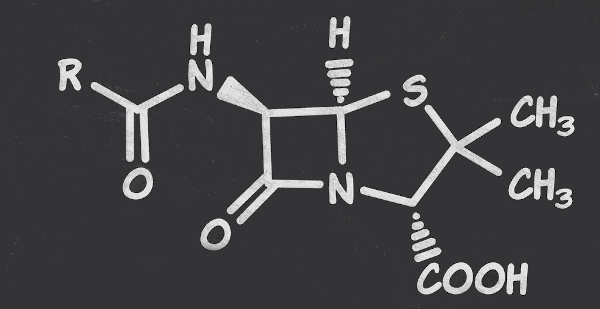
- Aplicadas na formulação de medicamentos como a sulfanilamida e penicilina, princípios ativos de medicamentos bactericidas no controle de infecções.
- A ureia que pode ser obtida de forma sintética ou como produto excretado por mamíferos, é uma substância do grupo amida, uma diamida. É utilizada como suplemento alimentar na agropecuária e como fertilizante.

Obtenção das amidas
As amidas são facilmente encontradas de forma natural, mas sua obtenção de forma sintética ainda é amplamente utilizada em processos industriais. Veja, a seguir, algumas reações de produção da amida com base em outros compostos nitrogenados.
-
Reação de desidratação de sal de amônio
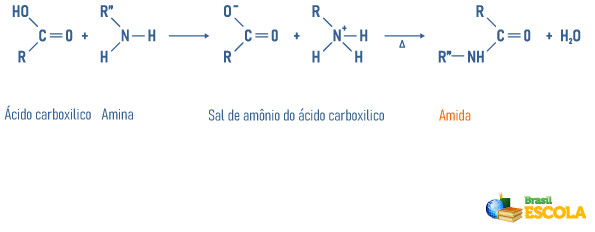
-
Reação de aminas com cloreto ácido
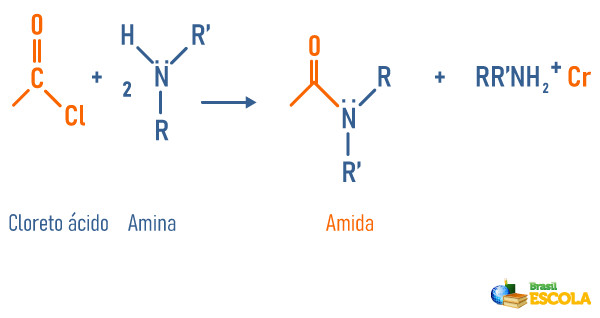
-
Reação de anidridos com aminas
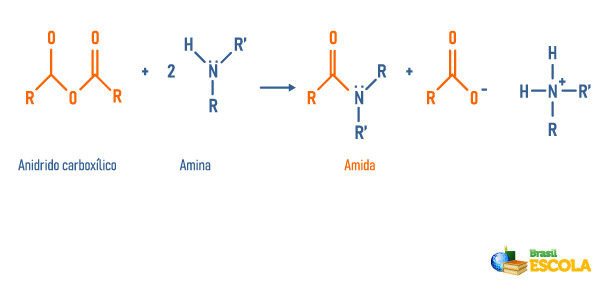
-
Reação de ésteres com aminas
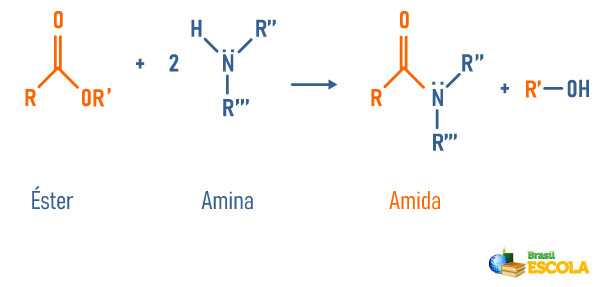
-
Rearranjo estrutural de uma aldoxima
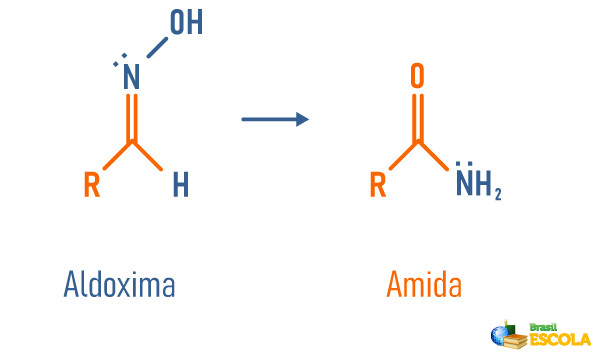
-
Hidratação de nitrilas
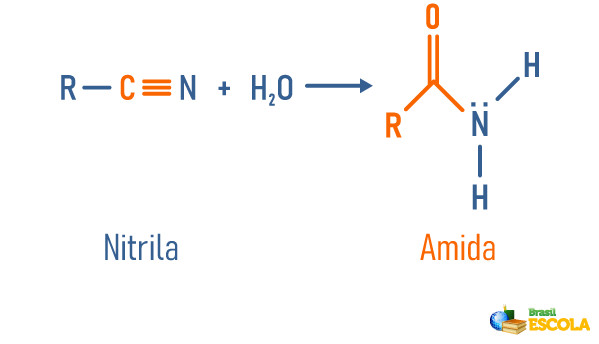
Leia também: Hidrólise de amidas – reação utilizada para obtenção de importantes substâncias
Exercícios resolvidos
Questão 1 – (UFRS) O aspartame, representado adiante, é um adoçante artificial usado em muitos refrigerantes e alimentos de baixa caloria.
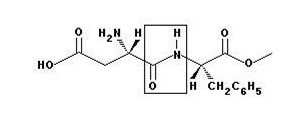
O grupo enquadrado na figura é característico da função orgânica
A) éster.
B) amida.
C) aminoácido.
D) amina.
E) carboidrato.
Resolução
Alternativa B. O grupo funcional selecionado na figura é uma amida, devido à presença de uma carbonila (C=O) ligada diretamente ao nitrogênio (N).
Questão 2 – (UNESP) Em agosto de 2005, foi noticiada a apreensão de lotes de lidocaína que teriam causado a morte de diversas pessoas no Brasil, devido a problemas de fabricação. Esse fármaco é um anestésico local muito utilizado em exames endoscópicos, diminuindo o desconforto do paciente. Sua estrutura molecular está representada a seguir:
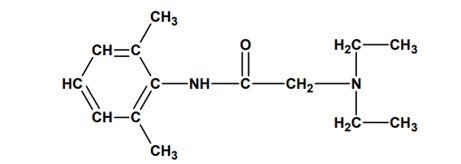
e apresenta as funções:
A) amina secundária e amina terciária.
B) amida e amina terciária.
C) amida e éster.
D) éster e amina terciária.
E) éster e amina secundária.
Resolução
Alternativa B.
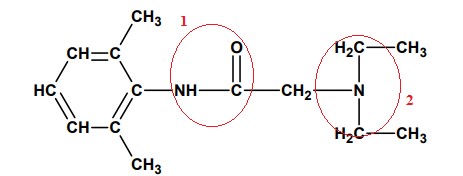
Após selecionar e numerar as partes características de cada função orgânica, vamos fazer a análise de cada uma:
1- Trata-se de uma AMIDA pela presença do grupo acila, (R-C=O) ligado diretamente ao nitrogênio, monossubstituída.
2- Como não temos a presença do grupo acila (R-C=O), e sim apenas o nitrogênio ligado diretamente a outros carbonos, nesse grupo temos uma AMINA TERCIÁRIA, porque todos os três hidrogênios, antes ligados ao nitrogênio, foram substituídos por grupos orgânicos.
Por Laysa Bernardes Marques de Araújo
Professora de Química