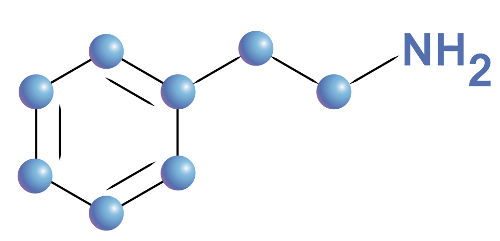
Aminas são compostos orgânicos nitrogenados que derivam da substância amônia (NH3) pela substituição de um ou mais hidrogênios por radicais orgânicos. De acordo com a quantidade de hidrogênios substituídos, as aminas podem ser classificadas em:
-
Amina primária: formada pela substituição de um hidrogênio da amônia por um radical orgânico;
Anuncie aqui
![]()
-
Amina secundária: formada pela substituição de dois hidrogênios da amônia por dois radicais orgânicos.
![]()
-
Amina terciária: formada pela substituição dos três hidrogênios da amônia por três radicais orgânicos.
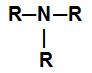
Tópicos deste artigo
- 1 - Características físicas das Aminas
- 2 - Características químicas das Aminas
- 3 - Regra de nomenclatura das aminas
- 4 - Aplicações das aminas
Características físicas das Aminas
-
São compostos polares;
-
Aminas primárias e secundárias são capazes de realizar ligações de hidrogênio;
-
Aminas terciárias realizam interação dipolo permanente;
-
As aminas com até cinco carbonos são solúveis em água e etanol. Já as aminas com seis ou mais carbonos são praticamente insolúveis em água, mas solúveis em solventes orgânicos;
Anuncie aqui -
Aminas que apresentam estrutura aromática são mais densas que a água;
-
Aminas que apresentam de um a três carbonos são gasosas em temperatura ambiente. Já as que apresentam de quatro a doze carbonos são líquidas em temperatura ambiente;
-
De uma forma geral, as aminas apresentam ponto de fusão e de ebulição mais elevados apenas em relação a qualquer composto orgânico apolar.
Características químicas das Aminas
-
São consideradas bases orgânicas, segundo a teoria de Bronsted-Lowry;
-
Aminas aromáticas apresentam um menor caráter básico em virtude do fenômeno da ressonância;
-
Quanto maior o caráter básico da amina, maior a probabilidade de reação com certa substância;
Anuncie aqui -
Na presença de um ácido, as aminas realizam reação de neutralização, já que apresentam caráter básico.
Regra de nomenclatura das aminas
Para fornecer o nome a uma amina, basta seguir a regra estabelecida pela União Internacional da Química Pura e Aplicada (IUPAC), descrita a seguir:
Nome do radical ou radicais + amina
OBS.: Se a amina tiver radicais diferentes, devemos seguir a ordem alfabética.
Acompanhe alguns exemplos:
Exemplo 1: Amina primária
![]()
Na amina primária desse exemplo, temos a presença de uma radical propil, assim, o seu nome é propilamina.
Exemplo 2: Amina secundária
![]()
Na amina secundária desse exemplo, temos a presença do radical metil (à esquerda do nitrogênio) e do radical etil (à direita do nitrogênio). O seu nome é, seguindo a ordem alfabética, etil-metilamina.
Exemplo 3: Amina terciária
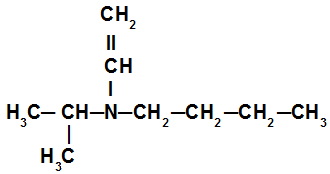
Na amina secundária desse exemplo, temos a presença do radical isopropil (à esquerda do nitrogênio), do radical butil (à direita do nitrogênio) e do radical vinil (abaixo do nitrogênio). O seu nome é, portanto, butil-isopropil-vinilamina.
Aplicações das aminas
-
Muito utilizadas na produção de vários compostos orgânicos;
Anuncie aqui -
Utilizadas na fabricação de sabões;
-
Utilizadas no processo de vulcanização da borracha;
-
Utilizadas na fabricação de corantes.