Radicais em Química Orgânica são conjuntos de átomos ligados entre si e que apresentam um ou mais elétrons livres (valências livres). Receberam o nome apropriado de radicais orgânicos, nestes compostos, um carbono tem um elétron desemparelhado. Se aplicarmos esse conceito à Teoria dos orbitais, este elétron estaria sozinho num orbital.
Como surgem os radicais livres?
A ligação covalente entre carbono e hidrogênio dá origem aos hidrocarbonetos. A ruptura homolítica dessa ligação é que faz surgir os radicais livres, veja a reação:
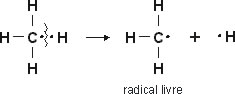
A equação acima representa a Cisão (quebra) de ligações e consequente formação do radical •CH3.
É importante enfatizar que um Radical é um grupo de átomos eletronicamente neutros. Surgem da cisão homolítica de ligações covalentes e ocorre sem perda ou ganho de elétrons.
Se ocorresse a cisão heterolítica, o produto não seria um radical e sim íons com carga positiva (cátions) ou carga negativa (ânions). O Hidrogênio desemparelhado seria representado como H+ e não como • H.
Conclusão: a quebra das ligações em Química Orgânica dá origem a radicais orgânicos, representados genericamente por R ―.
Por Líria Alves
Graduada em Química
Equipe Brasil Escola
Veja mais!
Propriedades dos compostos orgânicos
Química Orgânica - Química - Brasil Escola


