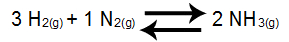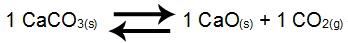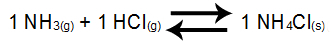O que é Kc?
O que é Kc? Trata-se da sigla que representa a constante de equilíbrio químico em termos de concentração em quantidade de matéria.

Imprimir
Texto:
A+
A-
Escrito por: Diogo Lopes Dias
Escritor oficial Brasil Escola
De estudante para estudante
Mande sua pergunta
Artigos Relacionados
O que é Kp?
Entenda o que é Kp, a constante do equilíbrio em termos de pressão, e saiba como obtê-la utilizando obrigatoriamente as pressões parciais de todos os gases presentes em um equilíbrio químico, que podem estar em atmosferas (atm) ou em milímetros de mercúrio (mmHg). Clique aqui e descubra mais sobre esse assunto!
O que é Química?
Relação entre constantes de equilíbrio Kc e Kp
Neste artigo você encontrará uma dedução completa que leva às expressões que relacionam as constantes de equilíbrio Kc e Kp e exemplos de como aplicá-las.
Química
Cálculo da constante de equilíbrio Kc
Conheça um método fácil para se calcular o valor da constante de equilíbrio Kc das reações reversíveis.
Química
Molaridade ou concentração molar
Clique aqui e descubra o que é molaridade ou concentração molar. Conheça sua fórmula e descubra como calculá-la.
Química
Constantes de Equilíbrio Kc e Kp
A constante do equilíbrio químico será dada pela divisão do Kdireto pelo Kinverso.
Química
Exercícios resolvidos sobre equilíbrios químicos
Teste seus conhecimentos e aprenda mais com esta lista de exercícios resolvidos sobre equilíbrios químicos. Por meio deste material, você poderá entender melhor como trabalhar constantes do equilíbrio (Kp, Kc e Ki), deslocamento do equilíbrio, pH e pOH, bem como equilíbrio nas chamadas soluções-tampão.
Química
Equilíbrio químico no Enem
Clique neste link e tenha acesso a um material com resoluções completas de alguns exercícios sobre equilíbrio químico das últimas edições do Enem. Para acompanhar a solução desses exercícios, é interessante relembrar assuntos como força de ácidos e bases, hidrólise salina, pH e deslocamento de equilíbrio.
Química
PUBLICIDADE