A isomeria óptica está ligada ao fato de a molécula orgânica ser assimétrica. Na maioria das vezes a assimetria da molécula é identificada por meio da presença de um carbono assimétrico ou quiral, isto é, carbonos que possuem os quatro ligantes diferentes entre si.
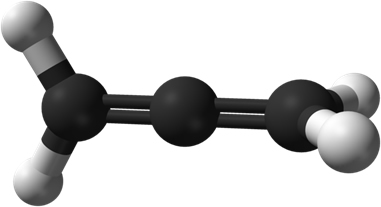
No entanto, existem moléculas que não possuem carbonos assimétricos, mas que ainda assim são assimétricas e, consequentemente, possuem atividade óptica. Entre elas temos os compostos alênicos, isto é, derivados do aleno, o alcadieno mais simples que existe:
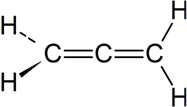
Conforme se pode ver no caso do composto alênico genérico abaixo, apesar de nenhum de seus carbonos possuírem quatro ligantes diferentes, não sendo assimétricos, a molécula possui uma conformação espacial que a deixa assimétrica. Além disso, ela não é superponível em relação à sua imagem especular:
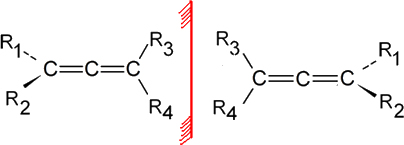
Assim, temos dois compostos opticamente ativos, o dextrogiro (desvia o plano de luz polarizada para a direita) e o levogiro (desvia o plano de luz polarizada para a esquerda). Temos também um composto opticamente inativo, que se trata da mistura racêmica, ou seja, 50% do dextrogiro e 50% do levogiro. Visto que cada um desses isômeros desvia o plano de luz polarizada com o mesmo ângulo, mas em sentidos opostos, um anula o outro e a mistura não possui atividade óptica.
Isso pode ocorrer com alcadienos com ligações duplas conjugadas ou consecutivas, desde que possuam dois substituintes diferentes nos dois átomos que ficam nas extremidades das ligações duplas.
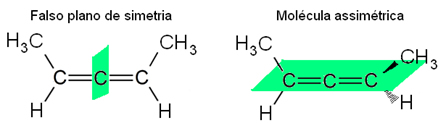
Se não tomarmos cuidado, podemos nos enganar achando que a molécula é simétrica, visto que possui os ligantes de cada átomo de carbono iguais aos do outro carbono. Mas, como mostrado abaixo, a molécula é assimétrica:
Por Jennifer Fogaça
Graduada em Química