A isomeria óptica é um tipo de isomeria espacial, ou estereoisomeria, que estuda o comportamento das substâncias quando submetidas a um feixe de luz polarizada. Para entender melhor, leia o texto “Luz Polarizada”.
Assim como em todo tipo de isomeria, os isômeros ópticos possuem a mesma fórmula molecular, mas são diferenciados por sua atividade óptica.
Por exemplo, considere a molécula de ácido lático mostrada abaixo. Visto que ela não é simétrica, ela pode dar origem a dois tipos de ácidos láticos:
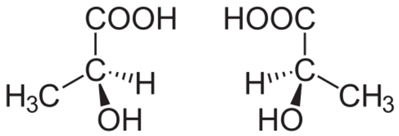
Quando submetemos essas duas moléculas a um feixe de luz polarizada, notamos que uma delas desvia o feixe de luz polarizada para a direita, sendo denominada de dextrogiro (ácido d-lático); e a outra desvia para a esquerda, denominada de levogiro (ácido ℓ-lático). O ácido lático dextrogiro é obtido pela ação de bactérias no extrato de carne, e o ácido lático levogiro a partir da fermentação da sacarose pelo Bacillus acidi levolactiti.
Portanto, esses dois compostos são isômeros ópticos.
Um modo de verificar se a molécula de determinado composto realiza atividade óptica é por observar se a molécula possui algum carbono assimétrico (C*), isto é, que possui 4 ligantes diferentes.
Note que isso ocorre na estrutura do ácido lático, sendo que esse tipo de carbono é chamado de quiral, que origina-se de uma palavra em grego que significa “mão’. Assim, como nossa mão, os estereoisômeros ópticos são a imagem especular um do outro, sendo chamados devido a isso de enantiômeros.
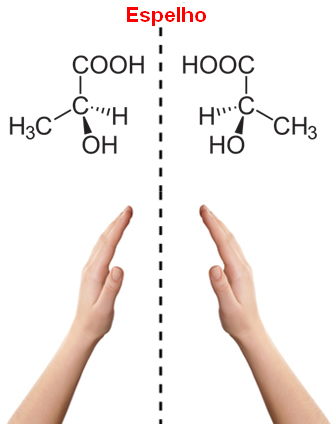
Além disso, deve-se observar também se as estruturas de suas moléculas não se sobrepõem, porque se a estrutura de determinada molécula e sua imagem se sobreporem sem alteração, então serão a mesma molécula e não isomeros ópticos.
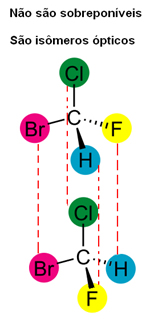
No entanto, é somente por meio da utilização de um polarímetro que é possível saber com certeza se um isômero óptico é dextrogiro ou levogiro.
Esses dois compostos, apesar de serem quimicamente e fisicamente iguais, possuem propriedades totalmente diferentes. Uma mistura deles é opticamente inativa, ou seja, não desvia o plano de luz polarizada e é chamada de mistura racêmica.
Por Jennifer Fogaça
Graduada em Química