Veremos neste texto como é construído um gráfico de mudança de estado físico para qualquer substância pura, como interpretar esse tipo de diagrama e como o gráfico das misturas é representado.
Para tal, vamos considerar o exemplo da água. Imagine que pegamos um copo com gelo em uma temperatura de – 10 ºC e iniciamos um processo de aquecimento, sob pressão de 1 atm. À medida que a temperatura for aumentando, passando de -10 ºC para -9 ºC, para – 8ºC e assim sucessivamente, o gelo permanecerá no estado sólido até atingir a temperatura de 0 ºC.
Nesse ponto, ele começa a passar para o estado líquido, ou seja, começa a ocorrer a fusão. A temperatura não continuará aumentando como antes, mas permanecerá constante em 0ºC até que todo o gelo tenha derretido:
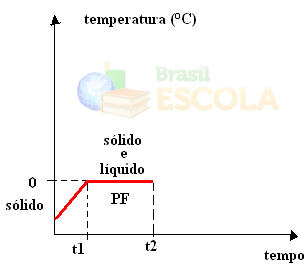
Depois da fusão de todo o sólido, a temperatura do sistema continuará a aumentar até atingir a temperatura de 100ºC. Nessa temperatura, a água que estava no estado líquido começará a passar para o estado de vapor, ou seja, ela entrará em ebulição.
Assim como aconteceu no ponto de fusão, no ponto de ebulição, a temperatura também permanecerá constante até que todo o líquido vire vapor. Depois disso, se continuarmos aquecendo o sistema, a temperatura continuará a subir:
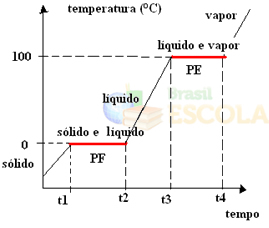
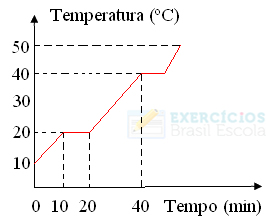
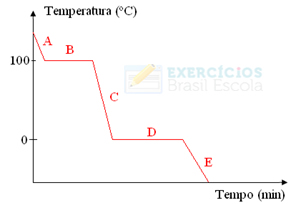
Pronto! Esse é o gráfico ou diagrama que representa a mudança de estado físico da água ou a sua curva de aquecimento. Se fosse o processo inverso, teríamos a seguinte curva de resfriamento da água:
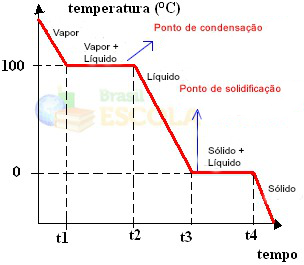
Um aspecto muito importante nesses gráficos é que eles são formados dois patamares, ou seja, há dois pontos em que a temperatura permanece constante por um tempo. Isso ocorre sempre na mudança de estado de uma substância pura. A única diferença são os valores dos pontos de fusão e de ebulição.
O oxigênio, por exemplo, ao contrário da água, não é líquido, mas gasoso em temperatura ambiente (cerca de 20ºC). Isso acontece porque seu ponto de fusão ao nível do mar é igual a -223,0 ºC e seu ponto de ebulição é de -183,0 ºC. Veja o seu gráfico de mudança de estado físico:
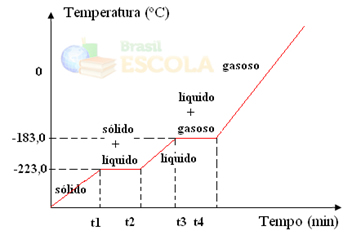
Gráficos de misturas comuns
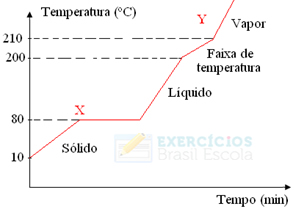
Se estivermos aquecendo ou resfriando uma mistura, o ponto de fusão e o ponto de ebulição não terão valores determinados e constantes, ou seja, não se formarão os dois patamares observados nos gráficos acima.
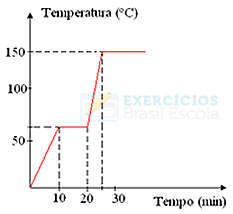
As mudanças de estados físicos ocorrerão em faixas de temperatura, e não em um valor fixo. O ponto de fusão, por exemplo, começará em uma dada temperatura e terminará em outra, e o mesmo ocorrerá com o ponto de ebulição, como mostrado no gráfico a seguir:
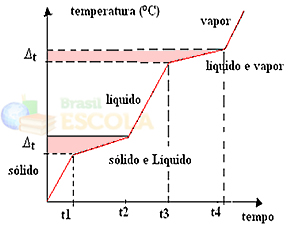
Duas exceções são as misturas eutética e azeotrópicas. Veja o que acontece com elas:
a) Mistura eutética
A mistura eutética comporta-se como se fosse uma substância pura durante a fusão, ou seja, nesse ponto, a temperatura mantém-se constante do início ao fim da mudança de estado de agregação.
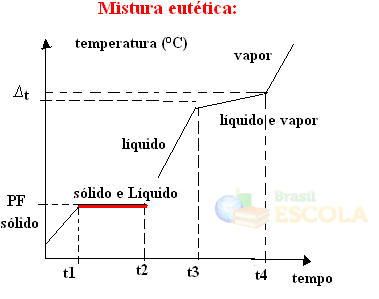
b) Mistura azeotrópica
A mistura azeotrópica comporta-se como uma substância pura durante a ebulição, ou seja, nesse ponto, a temperatura mantém-se constante do início ao fim da mudança de estado de agregação.
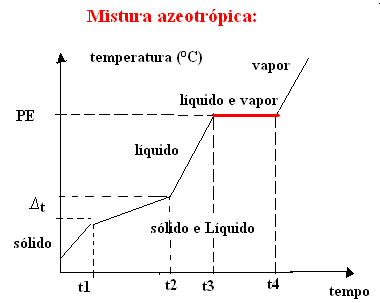
Por Jennifer Fogaça
Graduada em Química