O formol (formalina) é uma solução formada pela mistura de água e metanal. Como o metanal é o componente principal dessa mistura, é permitido associar o nome formol ao termo metanal. Assim, sempre que nos referirmos ao formol, também estamos fazendo referência ao metanal.
→ Características químicas do formol
O formol, ou metanal, apresenta uma substância orgânica com um átomo de carbono ligado a um oxigênio e a dois hidrogênios, como podemos observar em sua estrutura abaixo:
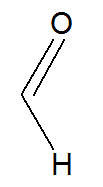
Fórmula estrutural do metanal
Na estrutura do metanal, temos um grupo carbonila (carbono que realiza uma dupla ligação com o oxigênio), logo, ele pertence à função aldeído. Como possui só um carbono, trata-se do menor aldeído existente.
O metanal apresenta alta inflamabilidade (queima com facilidade), além de ser capaz de reagir quimicamente com as mais diversas substâncias. Veja alguns exemplos de substâncias que reagem com o formol:
- Albumina (proteína encontrada, por exemplo, na clara do ovo);
- Caseína (proteína encontrada no leite);
- Óxidos (substâncias inorgânicas binárias cujo elemento mais eletronegativo é o oxigênio, desde que apresente NOX -2, como o CO2);
- Nitrometano (substância orgânica formada pela associação do grupo nitro (NO2) com um radical metil (CH3));
- Carbonato de manganês (MnCO3 - sal inorgânico utilizado na produção de cerâmicas);
- Peróxidos (substâncias inorgânicas binárias cujo elemento mais eletronegativo é o oxigênio, desde que apresente NOX -1, como o H2O2);
→ Características físicas do formol
- Em temperatura ambiente, ele é um líquido claro;
- Massa molar igual a 30 g/mol;
- Seu ponto de fusão é de -92oC;
- Seu ponto de ebulição é de 96oC;
- Sua taxa de evaporação é similar à da água;
- A solubilidade em água é infinita;
- É solúvel em solventes orgânicos, como o etanol, propanona e éter;
- Suas moléculas apresentam geometria trigonal plana;
- Sua densidade é de 1,1 g/cm3;
- Seu pH (concentração de íons H+) varia de 3 a 4 (é uma substância ácida).
→ Produção do formol
O formol pode ser obtido a partir de alguns processos químicos, mas o método mais utilizado é a oxidação catalítica do metanol.
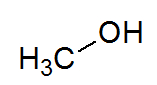
Fórmula estrutural do metanol
No processo de oxidação do metanol, utiliza-se como catalisador um óxido metálico ou a prata. Além do catalisador, o metanol é submetido a uma mistura gasosa (composta por hidrogênio, monóxido de carbono e dióxido de carbono), sendo convertido em metanal.
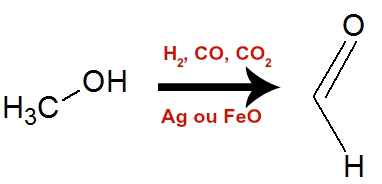
Formação do metanal
→ Utilizações do formol
- Produção de alguns cosméticos;
- Utilizado como desinfetante;
- Utilizado para embalsamar peças de cadáveres;
- Participa da produção de seda artificial;
- Produção de celulose;
- Produção de tintas;
- Produção de corantes;
- Produção de vidros e espelhos;
- Produção de explosivos;
- Produção de germicidas e fungicidas agrícolas;
- Produção de borracha sintética e no tratamento da borracha natural.
→ Legislação em relação ao uso do formol
A Agência Nacional de Vigilância Sanitária (Anvisa) é um órgão do Governo Federal que regulamenta o uso e a venda de substâncias que estão relacionadas de forma direta ou indireta com a saúde humana. Assim, o uso ou não do formol é regulamentado por ela.
Desde o ano de 2001, a Anvisa libera apenas a concentração de 0,2% de formol em produtos cosméticos, nos quais atua como conservante. Apenas nos endurecedores de esmalte que essa concentração é de 5%.
Em 2008, a Anvisa proibiu, por meio de uma resolução (Resolução da Diretoria Colegiada no35), o uso do formol na produção de qualquer produto saneante, ou seja, aqueles utilizados para a limpeza (detergentes, desinfetante etc). Em 2009, uma nova resolução da ANVISA proibiu a venda do formol em todo e qualquer estabelecimento (farmácias, supermercados, armazém etc).
Infelizmente alguns profissionais continuam utilizando o formol para realizar o alisamento capilar em clientes, desobedecendo às normas estabelecidas pela Anvisa, assim como alguns fabricantes de produtos saneantes. Vale ressaltar que essa prática está sujeita à punição legal.
→ Prejuízos que o formol pode provocar no ser humano
Desde 2004, a Agência Internacional de Pesquisa em Câncer (IACR) classifica o formol como uma substância carcinogênica para o ser humano, ou seja, capaz de provocar algum tipo de câncer. Além de ser causador do câncer, o formol pode ainda provocar os seguintes males:
Em contato com a pele, provoca:
- Irritação
- Vermelhidão
- Dor
- Queimaduras
Em contato com os olhos, provoca:
- Irritação
- Vermelhidão
- Dor
- Lacrimação
- Visão embaçada
- Cegueira (quando em grande quantidade)
Quando ingerido, provoca:
- Queimação
- Lesões no trato gastrointestinal
- Dores abdominais
- Náuseas
Quando seus vapores são inalados, provocam:
- Dor de garganta
- Irritação do nariz
- Tosse
- Diminuição da frequência respiratória
- Aumento da sensibilização do trato respiratório
- Ferimentos graves nas vias respiratórias
- Edema pulmonar
- Pneumonia
- Bronquite
Outros:
- Morte por intoxicação
- Aumento do fígado
- Queda do cabelo
- Alergias
Por Me. Diogo Lopes Dias



