Superóxidos são substâncias inorgânicas binárias, isto é, formadas por apenas dois elementos químicos, sendo um deles metal alcalino (família IA) ou alcalinoterroso (família IIA) e o outro, e mais eletronegativo, o oxigênio.
![]()
Fórmula binária apresentando apenas dois elementos
Não podemos confundir um superóxido com um peróxido ou um óxido, mesmo que esses dois compostos binários apresentem elementos das mesmas famílias ligados ao oxigênio. Então, como diferenciar esses três compostos?
A diferença está no NOX que o oxigênio apresenta nessas três substâncias. Em um óxido, o NOX é sempre -2, e, nos peróxidos, o NOX é sempre -1. Já nos superóxidos, o NOX do oxigênio é igual a -1/2.
Como o oxigênio do superóxido, os metais das famílias dos alcalinos e dos alcalinoterrosos apresentam NOX fixos, +1 e +2, respectivamente. Os superóxidos possuem, portanto, um padrão de fórmulas químicas:
-
Para metais alcalinos:
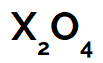
Fórmula geral de um superóxido com um metal alcalino qualquer
-
Para metais alcalinoterrosos:
Anuncie aqui
.jpg)
Fórmula geral de um superóxido com um metal alcalinoterroso qualquer
Tópicos deste artigo
Nomenclatura dos superóxidos
A nomenclatura dos superóxidos pode ser feita por uma regra bastante simples:
Superóxido + de + nome do metal
Assim, para nomear um superóxido, basta conhecer o metal que acompanha o oxigênio, como no exemplo a seguir:
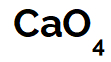
Fórmula do superóxido formado pelo elemento cálcio
Como nesse superóxido temos a presença do elemento cálcio, seu nome é superóxido de cálcio.
Reações químicas com superóxidos
Os superóxidos são compostos químicos que apresentam a natureza de reagir com os seguintes compostos:
-
Água: quando os peróxidos reagem com a água, formam uma base (constituída pelo metal do superóxido) e o peróxido de hidrogênio (H2O2).
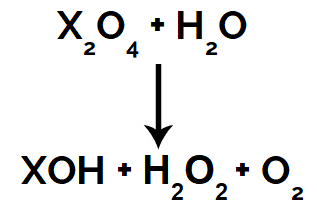
Produtos formados em uma reação de superóxido com água
Como o peróxido de hidrogênio sofre decomposição:
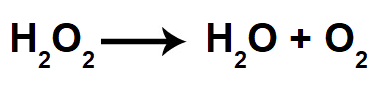
Equação da decomposição do peróxido de hidrogênio
A água formada na decomposição do peróxido de hidrogênio cancela um ou mais mol no reagente da equação do superóxido com água. Por esse motivo, no produto da equação da reação entre um superóxido e água, há apenas a base e o gás oxigênio.
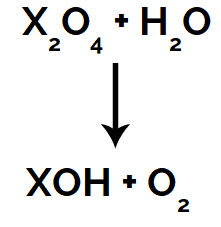
Equação da reação do superóxido com água
-
Ácidos inorgânicos: quando os peróxidos reagem com um ácido inorgânico, sempre dão origem a um sal – originado pela interação do cátion do superóxido com o ânion do ácido –, gás oxigênio e peróxido de hidrogênio.
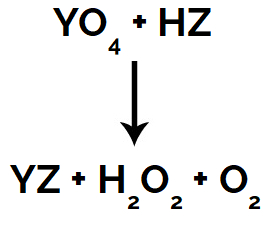
Equação da reação do superóxido com ácido inorgânico
Em meio ácido, o peróxido de hidrogênio não sofre decomposição, portanto, não ocorre a formação de água nessa reação com superóxidos.
Por Me. Diogo Lopes Dias



