O texto Primeira lei da radioatividade ou primeira lei de Soddy mostrou a primeira lei geral que corresponde ao que ocorre quando um átomo de um elemento radioativo sofre um decaimento alfa.
A segunda lei da radioatividade ou segunda lei de Soddy refere-se ao decaimento beta. Veja o que essa lei diz:
“Quando um átomo emite uma partícula beta, seu número atômico (Z) aumenta uma unidade e seu número de massa (A) permanece o mesmo.”
Genericamente, podemos representar essa lei por meio da seguinte equação:
ZAX → -10β + Z+1AY
O número atômico (Z) é a quantidade de prótons existentes no núcleo atômico. Já o número de massa (A) corresponde à soma dos prótons e dos nêutrons existentes no núcleo (A = p + n). Isso significa que o átomo obtido é um isóbaro do átomo original, ou seja, possuem o mesmo número de massa.
Veja um exemplo: o tório- 231 emite uma partícula beta e forma o protactínio-231:
23190Th→ -10β + 23191Pa
Observe que há conservação do número de massa e do número atômico nos dois membros da equação:
A: 231 = 0 + 231;
Z: 90 = -1 + 91.
Assim, é possível usar essa regra para descobrir qual partícula foi emitida ou qual átomo foi formado.
Conforme explicado no texto Emissão beta (β), essa emissão é como um elétron, pois ela possui carga de -1 e não apresenta massa. Mas então por que o número atômico aumenta e o número de massa permanece constante?
Essa fato foi explicado por uma hipótese lançada pelo físico italiano Enrico Fermi (1901-1954).

Um selo postal impresso por volta de 2001 nos EUA mostra uma imagem do vencedor do Prêmio Nobel de Física, Enrico Fermi
Enrico Fermi propôs o seguinte:
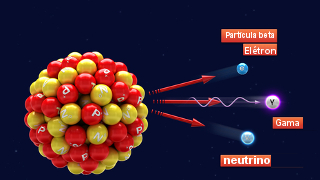
“A emissão da partícula beta ocorre quando um nêutron instável no interior do núcleo atômico desintegra-se, formando um próton que permanece no núcleo. Ao mesmo tempo essa desintegração forma a partícula beta (-10β), que é semelhante ao elétron e é emitida pelo núcleo juntamente à radiação gama (γ – é somente uma radiação eletromagnética, não possuindo carga elétrica e nem massa) e um neutrino (00ν, partícula de carga e massa nulas).”
Ou seja:
01n → 11p + -10β + 00 γ + 00ν
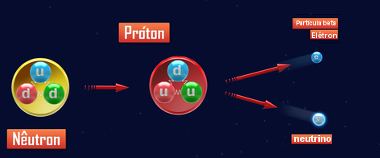
Desintegração do nêutron para a emissão da partícula beta
O próton e o nêutron possuem praticamente a mesma massa e é por isso que, quando um átomo emite uma partícula beta, seu número de massa (A) permanece o mesmo, ou seja, enquanto o nêutron desintegra-se, o próton é formado, substituindo-o no núcleo, por assim dizer. Visto que o próton é formado, o número atômico aumenta uma unidade.
Veja na ilustração a seguir mais um exemplo de como essa lei realmente se aplica nos casos de decaimentos beta. Nela, o isótopo 14 do elemento carbono emite uma partícula beta, transformando-se no nitrogênio-14:
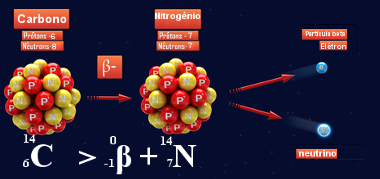
Decaimento beta do carbono-14 que gera o nitrogênio-14
__________________
* Imagem com direitos autorais: catwalker / Shutterstock.com.
Por Jennifer Fogaça
Graduada em Química