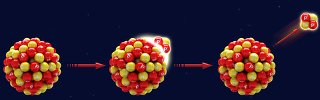
As emissões radioativas naturais são três: alfa (α), beta (β) e gama (γ). Alguns cientistas passaram a estudar a natureza dessas emissões e foram criadas algumas leis gerais para a radioatividade. Entre esses cientistas, um que fez contribuições notáveis para o estudo do decaimento radioativo natural foi o físico e químico inglês Frederick Soddy (1877-1956).

Um selo postal impresso na Suécia, por volta de 1981, mostra uma imagem do vencedor do Prêmio Nobel de Química de 1921, Frederick Soddy*
A primeira lei da radioatividade, também conhecida como primeira lei de Soddy, tem relação com o decaimento alfa. Veja o que essa lei diz:
“Quando um átomo sofre um decaimento alfa (α), o seu número atômico (Z) diminui duas unidades e o seu número de massa (A) diminui quatro unidades”.
Genericamente, podemos representar essa lei pela seguinte equação:
ZAX → 24α + Z-2A-4Y
Isso acontece com todo elemento radioativo que emite uma partícula alfa, pois, conforme mostrado no texto Emissão alfa (α), essa partícula é constituída por dois prótons e dois nêutrons — de forma semelhante ao que ocorre com o núcleo de um átomo de hélio — e é representada por 24α.
O número atômico (Z) é o mesmo que o número de prótons. Assim, visto que com a emissão de uma partícula alfa dois prótons são perdidos, o número atômico diminui duas unidades. Já o número de massa (A) corresponde à soma dos prótons com os nêutrons. Como a partícula alfa possui dois prótons e dois nêutrons, o número de massa diminui quatro unidades quando o núcleo emite uma partícula dessa.
Veja um exemplo: o urânio-235, ao sofrer um decaimento alfa, resulta no tório. Veja que seu número atômico diminuiu exatamente duas unidades (92 – 90 = 2) e seu número de massa diminuiu quatro unidades (235 – 231 = 4):
92235U → 24α + 90231Th
O número atômico e o número de massa conservam-se iguais no primeiro e no segundo membro dessa equação. Assim, se você quiser descobrir qual partícula foi emitida ou qual elemento foi originado, basta relacionar essas grandezas.
Olhando na tabela periódica, vemos que o tório localiza-se duas casas antes do urânio. Isso é óbvio porque os elementos químicos estão dispostos na tabela periódica em ordem crescente de número atômico e o número atômico diminuiu duas unidades:

Localização dos elementos tório e urânio na Tabela Periódica
Isso nos leva à outra generalização:
Todo átomo que emite uma partícula alfa transforma-se no átomo do elemento que fica duas casas à esquerda do elemento original.
__________________
* Imagem com direitos autorais: catwalker / Shutterstock.com.
Por Jennifer Fogaça
Graduada em Química