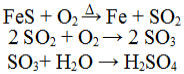As reações inorgânicas são transformações da matéria onde ocorrem mudanças na composição química, resultando em um ou mais produtos. Veja os tipos de reações que podem ocorrer:
Metais com a água
Metais alcalino e alcalino-terrosos (Ca, Ba, Sr, Ra) fazem reação branda com a água à temperatura ambiente.
2 Na (s) + 2 HOH (l) → 2 NaOH (aq) + H2 (g)
Os produtos da reação do metal alcalino Sódio (Na) com água são: hidróxido de sódio (NaOH) e gás hidrogênio (H2).
Reação onde uma única substância composta origina dois ou mais produtos.
2 H2O → 2 H2 + O2
É possível obter hidrogênio e oxigênio através da decomposição da água.
Síntese ou adição
Reação onde duas substâncias originam um único composto.
2 Mg +O → 2 MgO
Repare que a junção dos dois elementos, magnésio (Mg) e oxigênio (O), deu origem a apenas um produto: MgO (óxido de magnésio).
Também chamada de reação de simples troca ou substituição, onde uma substância simples reage com uma substância composta originando uma substância simples e uma substância composta.
Cl2 + 2 NaBr →2 NaCl + Br2
Cloro (Cl) - substância simples - se une ao Brometo de sódio (NaBr) – substância composta.
Também conhecida como reação de metátese, é a reação onde duas substâncias compostas se misturam formando duas novas substâncias.
H2SO4 + BaCl2 → BaSO4↓ + 2HCl
Ácido sulfúrico (H2SO4) e Cloreto de bário (BaCl2): substâncias compostas que se unem para formar o precipitado sulfato de bário (BaSO4↓) e ácido clorídrico (HCl).
Por Líria Alves
Graduada em Química