A destilação simples é uma técnica de separação de misturas homogêneas líquidas, baseada na diferença das temperaturas de ebulição dos componentes. Na destilação simples, ocorre a separação da mistura em dois componentes: o resíduo, rico nos componentes menos voláteis, e o destilado, rico nos componentes mais voláteis.
A destilação simples ocorre mediante aquecimento da mistura inicial, que, durante a ebulição, forma um vapor rico nos componentes mais voláteis. Esse vapor, posteriormente, é condensado e, então, coletado, concluindo a separação. A destilação simples é muito importante, mas necessita de uma significativa diferença de temperatura de ebulição dos componentes para uma separação efetiva.
Leia também: De que formas ocorre a separação de misturas?
Tópicos deste artigo
- 1 - Resumo sobre destilação simples
- 2 - O que é destilação simples?
- 3 - Exemplos de destilação simples
- 4 - Equipamentos para destilação simples
- 5 - Como funciona a destilação simples?
- 6 - Quais as diferenças entre destilação simples e destilação fracionada?
- 7 - Exercícios resolvidos sobre destilação simples
Resumo sobre destilação simples
- A destilação simples é uma técnica que separa uma mistura homogênea líquida em dois componentes, chamados de resíduo e de destilado, a partir das diferenças das temperaturas de ebulição dos componentes da mistura.
- O resíduo é rico nos componentes menos voláteis, enquanto o destilado é rico nos componentes mais voláteis.
- Na destilação simples, a mistura inicial é aquecida até sua ebulição, com a formação de um vapor rico nos componentes mais voláteis.
- O vapor é condensado durante a destilação, fazendo com que ele seja coletado adequadamente, concluindo-se, assim, a separação.
- Para uma destilação simples efetiva, necessita-se de uma boa diferença de temperaturas de ebulição dos componentes da mistura.
O que é destilação simples?
A destilação simples é um método de separação em que realiza a separação dos componentes de uma mistura homogênea líquida por meio da diferença de temperaturas de ebulição desses componentes. Isso porque, segundo a Termodinâmica, o vapor produzido a partir de uma mistura homogênea em ebulição é mais rico no componente mais volátil (de menor ponto de ebulição).
Exemplos de destilação simples
A destilação simples é uma técnica muito útil, a qual pode ser utilizada nas situações que apresentamos a seguir.
- Produção de água destilada: é uma água quimicamente pura, sem a presença de outros componentes que não moléculas de H2O.

- Recuperação de solvente: solventes voláteis podem ser recuperados ao fim do experimento para serem futuramente reutilizados por meio da destilação simples.
- Purificação de líquidos: a destilação pode ser empregada para a remoção de solutos não voláteis de líquidos, tirando, assim, a carga de possíveis agentes contaminantes.
- Produção de bebidas alcoólicas: grãos fermentados podem produzir concentrações de até 16% de etanol, que acaba sendo o limite máximo de concentração alcoólica em vinhos e em cervejas. Com isso, a destilação simples é empregada para produção de bebidas alcoólicas mais fortes, com concentração alcoólica na faixa dos 40%, como é o caso do gim, da vodca e da cachaça.
Confira também: Podemos beber água destilada?
Equipamentos para destilação simples

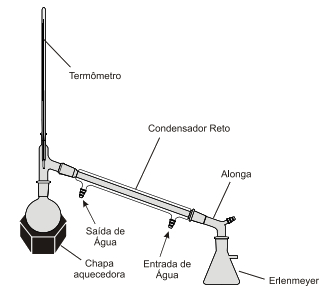
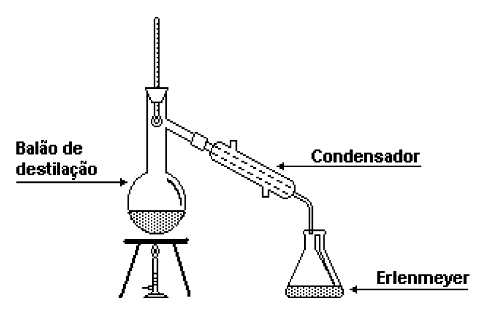
Em geral, uma destilação simples precisa dos equipamentos que apresentamos a seguir.
- Fonte de aquecimento: como o líquido será levado à ebulição, faz-se necessária a utilização de uma fonte de aquecimento, que pode ser uma manta de aquecimento ou um bico de Bunsen.
- Balão de destilação: é comum a utilização de um balão de fundo redondo para conter a mistura inicial. Seu formato auxilia em um aquecimento mais uniforme e, portanto, mais seguro, além de ter menos risco de quebra em temperaturas mais elevadas.
- Tubo condensador: é uma estrutura formada por dois tubos, um mais externo e outro mais interno. No condensador, como o próprio nome deixa em evidência, o vapor sofre condensação, pois, ao passar pelo tubo interno, é refrigerado por um fluido, em geral água, que passa pelo tubo externo. A água (ou qualquer outro fluido refrigerante) deve ser adicionada, através de uma mangueira, pelo orifício localizado ao final do condensador, pois, assim, evita um possível choque térmico com o vapor que está entrando no tubo.
- Frasco coletor: serve para receber o destilado na forma líquida, logo após ele passar pelo condensador. Em geral, utiliza-se um Erlenmeyer, muito por conta de seu bocal mais estreito, mas também é possível a utilização de béqueres ou de semelhantes.
- Termômetro: serve para fazer o controle de temperatura durante o processo, auxiliando a identificar o momento em que a destilação se inicia e se encerra.
Como funciona a destilação simples?
Na destilação simples, a mistura líquida homogênea é aquecida até ebulição. O vapor formado é rico no componente de menor ponto de ebulição da mistura. Esse vapor, portanto, ascende pela aparelhagem até chegar no tubo condensador. Agora, a mistura foi separada em duas partes: uma que permanece no balão de destilação, com os componentes menos voláteis, e o vapor, que segue com o componente (ou os componentes) de menor ponto de ebulição.
O vapor, ao chegar no condensador, sofre uma queda substancial de temperatura, fazendo com que sofra condensação e se torne um líquido novamente. Agora, como líquido, escorre até o frasco coletor.
A destilação simples só permite a separação da mistura em duas partes: o resíduo de destilação, que apresenta o componente da mistura com maior ponto de ebulição, e o destilado, que apresenta o componente da mistura com menor ponto de ebulição. Dessa forma, para que essa separação seja mais efetiva, a diferença de temperatura de ebulição dos componentes da mistura deve ser grande (pelo menos 50 °C). Do contrário, caso os pontos de ebulição sejam próximos, a composição final do resíduo de destilação e do destilado podem ser muito semelhantes, indicando uma separação insatisfatória.
Quais as diferenças entre destilação simples e destilação fracionada?
A destilação simples permite apenas a separação da mistura inicial em apenas duas frações. Há uma limitação de que o destilado e o resíduo da destilação terão sempre uma concentração, ainda que diferentes, de todos os componentes da mistura inicial. Obviamente que essas concentrações se tornam mais distintas conforme se vê uma maior diferença nos pontos de ebulição dos componentes da mistura de partida, e, por isso, sugere-se que a diferença de pontos de ebulição dos componentes seja de, pelo menos, 50 °C.
Para superar essas limitações, foi criada a destilação fracionada, a qual funciona como uma espécie de destilações simples sucessivas, criando um efeito cascata conhecido como retificação. Na destilação fracionada, o vapor percorre um caminho maior até o condensador, permitindo, assim, um maior gradiente de temperatura. Assim sendo, alguns componentes do vapor podem, em determinado momento, sofrer condensação antes de chegarem ao condensador, enriquecendo o vapor no componente mais volátil.
Esse líquido que é formado antes da chegada ao condensador retorna em direção ao balão de destilação, encontrando vapor ascendente e permitindo trocas de calor que também favorecem o enriquecimento do vapor no componente mais volátil. Com isso, a separação é muito mais efetiva.

Além de uma separação mais satisfatória, a destilação fracionada permite a obtenção de diversas frações de destilado, ou seja, de diversas composições distintas do que vem sendo destilado. Isso é aplicado no refino de petróleo, em que uma coluna de destilação, muito alta, é usada para criar um gradiente de temperatura. Tal coluna apresenta saídas em diversos níveis de altura, o que permite a obtenção de derivados do petróleo com composições químicas distintas.
Veja também: Destilação fracionada — mais detalhes sobre como ocorre esse processo
Exercícios resolvidos sobre destilação simples
Questão 1
(UFJF) A técnica de destilação para a produção de bebidas alcoólicas a partir da fermentação de soluções de açúcares é descrita desde o século IX na região onde atualmente encontra-se o país Iraque.
Podemos afirmar que a técnica se baseia nas diferenças de:
A) Solubilidade entre dois ou mais compostos.
B) Configuração eletrônica entre dois ou mais compostos.
C) Densidade entre dois ou mais compostos.
D) Temperatura de ebulição entre dois ou mais compostos.
E) Temperatura de fusão entre dois ou mais compostos.
Resolução:
Alternativa D.
A destilação é empregada em misturas líquidas homogêneas, em que, por meio do aquecimento, os compostos mais voláteis acabam se separando da mistura durante a ebulição. Dessa forma, é uma técnica que depende da diferença dos pontos de ebulição dos componentes da mistura.
Questão 2
(Uece) Em um balão de destilação, um estudante de química introduziu água, cloreto de sódio, dicromato de potássio, areia, pó de giz e sulfeto de hidrogênio.
Ao final da destilação, uma substância que será transferida juntamente com a água é
A) o cloreto de sódio.
B) a areia.
C) o sulfeto de hidrogênio.
D) o dicromato de potássio.
Resolução:
Alternativa C.
Apenas a parte homogênea da mistura líquida sofrerá a destilação. Dessa forma, tanto a areia quanto o giz, por não se dissolverem na água, não estão sob análise. O cloreto de sódio e o dicromato de potássio são compostos iônicos cuja característica é o elevado ponto de ebulição. Já o sulfeto de hidrogênio é um composto covalente volátil. Dessa forma, ao se proceder a destilação, a água carreará consigo o componente mais volátil que, nesse caso, é o sulfeto de hidrogênio.
Crédito de imagem
Fontes
NICHOLS, L. Organic chemistry lab techniques: uses of simple distillation. In: NICHOLS, L. Organic Chemistry Lab Techniques. [S. l.]: LibreTexts, 2022. Disponível em: https://chem.libretexts.org/Bookshelves/Organic_Chemistry/Organic_Chemistry_Lab_Techniques_(Nichols)/05%3A_Distillation/5.02%3A_Simple_Distillation/5.2A%3A_Uses_of_Simple_Distillation.
PETLYUK, F. B. Distillation Theory and Its Application to Optimal Design of Separation Units. 1a ed. Cambridge, Reino Unido: Cambridge University Press, 2004.
SMITH, R.; JOBSON, M. Distillation. In: Encyclopedia of Separation Science. 1a ed. p. 1117-1134. Estados Unidos: Academic Press, 2000.
SPEIGHT, J. G. The Chemistry and Technology of Petroleum. 5ª ed. Flórida, EUA: CRC Press, 2014.
VIDROSLAB. Balões de fundo redondo. [S. l.]: Vidroslab, . Disponível em: https://www.vidroslab.com.br/baloes-de-fundo-redondo.
VOGELPOHL, A. Distillation – The Theory. 4a ed. Berlim, Alemanha: de Gruyter, 2015.