No nosso organismo ocorrem constantemente reações essenciais para a manutenção da vida. Por exemplo, os nutrientes dos alimentos que consumimos, como as proteínas, os carboidratos e as gorduras são convertidos em outras substâncias que podemos absorver. Essas transformações se dão de forma demasiadamente rápida graças à presença de enzimas.
As enzimas são moléculas de proteínas com grande massa molar que atuam como catalisadores biológicos, também chamados de biocatalisadores, ou seja, elas conseguem acelerar o metabolismo (reações do organismo).
Por exemplo, um pirulito sobre uma mesa demorará muito tempo para se decompor em contato apenas com o oxigênio do ar. Mas, quando o consumimos, a reação entre o açúcar do pirulito e o oxigênio de organismo ocorre em poucos segundos, pois as enzimas agem sobre as moléculas de açúcar criando estruturas que reagem mais facilmente, acelerando a reação.

As enzimas são altamente específicas, o que significa que cada uma age como catalisadora biológica de apenas uma reação. Isso ocorre porque a enzima possui um centro ativo que se combina com o composto que irá sofrer a ação enzimática. Esse composto é chamado de substrato. É como se a enzima fosse a chave de uma fechadura (substrato).
No esquema abaixo, isso é exemplificado:
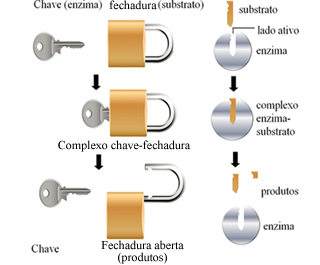
Observe que a enzima reage com o substrato de maneira específica, criando um composto intermediário que se decompõe facilmente, originando os produtos. Além disso, a enzima é regenerada não sendo consumida na reação, como ocorre com todos os catalisadores.
Um exemplo de enzima que está presente no estômago é a pepsina. Se colocarmos um pedaço de carne em contato com a pepsina, a carne será decomposta rapidamente. Se no lugar da pepsina, usarmos somente o ácido clorídrico, que é o principal componente do suco gástrico, veremos que a carne demorará muito tempo para ser decomposta. Portanto, a presença dessa enzima em nosso organismo é essencial para decompor as proteínas, que são os substratos da pepsina.
Outro exemplo está no transporte de gás carbônico no corpo humano. No interior das nossas hemácias existe a enzima anidrase carbônica que converte o gás carbônico em ácido carbônico cerca de 5 mil vezes mais rápido do que sem a sua presença!
Agora, uma catálise enzimática que podemos visualizar no cotidiano é quando nos machucamos e aplicamos água oxigenada sobre o ferimento. No momento ocorre uma intensa efervescência, que é a decomposição da água oxigenada. Essa decomposição ocorre muito lentamente, mas quando colocamos o produto em contato com o sangue, uma enzima chamada catalase aumenta a velocidade da reação.
Além disso, visto que a catalase do sangue não é consumida, a efervescência continuará à medida que adicionarmos mais água oxigenada no local.

Uma utilização benéfica desse conceito é feita em exames laboratoriais para diferenciar dois tipos de bactérias: os estafilococos e os estreptococos. Apenas os estafilococos contêm catalase. Assim, no teste, adiciona-se água oxigenada na amostra, se efervescer, é os estafilococos, se não efervescer, é os estreptococos.
Por Jennifer Fogaça
Graduada em Química