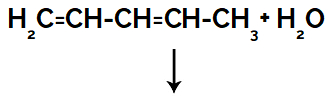
As reações de hidratação em alcadienos são reações de adição, ou seja, os componentes (hidrônio e hidróxido) da molécula de água são adicionados a um alcadieno.
Os alcadienos são hidrocarbonetos que apresentam cadeia aberta e duas ligações duplas (formadas por uma ligação sigma e uma pi) entre carbonos, como podemos visualizar na estrutura a seguir:
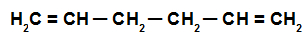
Fórmula estrutural de uma alcadieno
Para que a reação de hidratação em alcadienos seja realizada, é fundamental que a ligação pi, presente na ligação dupla, seja rompida pela influência de calor e ácido sulfúrico (H2SO4). Com o rompimento da ligação pi, surgem dois sítios de ligação, cada um em um dos carbonos envolvidos na ligação dupla.
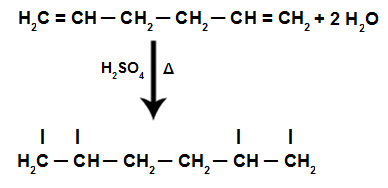
Surgimento de sítios de ligação com o rompimento da ligação pi
O surgimento dos sítios de ligação na molécula do alcadieno é necessário para que os íons (H+ e OH-) provenientes da água sejam adicionados ao alcadieno, formando, por exemplo, um diálcool (álcool com duas hidroxilas).
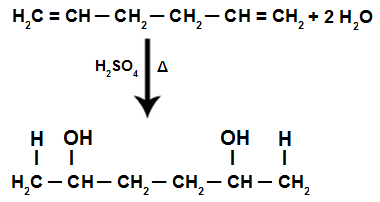
Adição de H+ e OH- na estrutura de um alcadieno
OBS.: A adição do H+ e do OH- na estrutura do alcadieno segue a regra de Markovnikov, ou seja, o H+ liga-se ao carbono mais hidrogenado, e o OH- liga-se ao carbono menos hidrogenado.
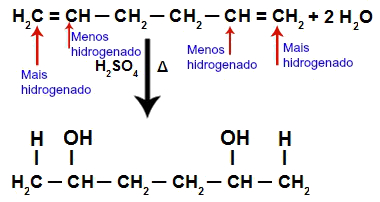
Exemplo da aplicação da regra de Markovnikov na hidratação de alcadienos
Como existem diferentes tipos de alcadienos no que diz respeito à posição das ligações duplas, pode ser que a hidratação de um alcadieno forme compostos diferentes. Veja os casos a seguir:
→ Alcadieno acumulado ou condensado
Trata-se de um alcadieno que apresenta as duas ligações duplas envolvendo simultaneamente três átomos de carbono, ou seja, não existe nenhuma ligação simples separando os carbonos envolvidos nas ligações duplas.
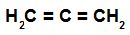
Fórmula estrutural de um alcadieno acumulado
Durante a reação de hidratação de um alcadieno alternado, as ligações pi são rompidas, sendo os H+ adicionados aos carbonos mais hidrogenados e os OH- adicionados aos carbonos menos hidrogenados:
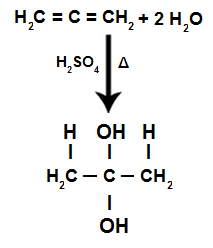
Equação da reação de hidratação de alcadieno acumulado
Temos que na hidratação de um alcadieno acumulado um mesmo átomo de carbono recebe as duas hidroxilas, formando um diálcool gêmino, que é uma estrutura instável.
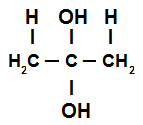
Estrutura do diálcool gêmino formado
Como o diálcool gêmino é instável, temos a formação de uma molécula de água com os componentes das duas hidroxilas e a criação de uma ligação pi entre o carbono e o oxigênio.
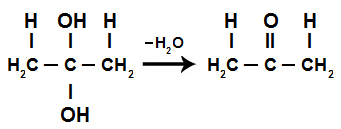
Formação de uma cetona a partir de um diálcool gêmino
Logo, a reação de hidratação de alcadienos acumulados resultará na formação de uma cetona.
→ Alcadieno conjugado ou alternado
Trata-se de um alcadieno que apresenta as duas ligações duplas envolvendo simultaneamente quatro átomos de carbono, ou seja, existe uma ligação simples separando os carbonos envolvidos nas ligações duplas.
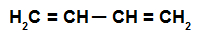
Fórmula estrutural de um alcadieno alternado
Nos alcadienos alternados, ocorre a ressonância de suas ligações duplas. Assim, os elétrons da ligação pi mudam de posição (setas vermelhas), como no esquema a seguir:
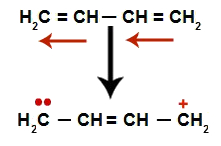
Esquema representando a ressonância em um alcadieno alternado
Temos, de forma geral, o surgimento de uma ligação dupla exatamente entre os carbonos onde estavam as duas duplas anteriormente e a criação de dois sítios de ligação, um em cada carbono que não está mais realizando a ligação dupla (no exemplo, os carbonos 1 e 4). Os carbonos 1 e 4 da cadeia recebem o H+ e o OH- provenientes da água.
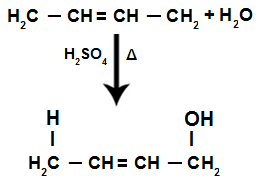
Hidratação parcial no alcadieno alternado
Após a ressonância, a ligação pi da nova ligação dupla é rompida, e um H+ e um OH- são adicionados à molécula do alcadieno. O OH é adicionado ao carbono mais próximo do primeiro grupo OH adicionado pelo fato de ele sofrer a atração eletrônica do grupo, que é mais eletronegativo.
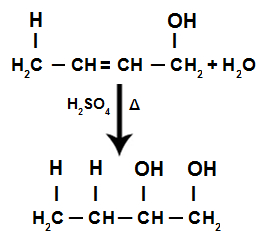
Término da hidratação em um alcadieno alternado
Por causa da ressonância, dizemos que o alcadieno alternado sofreu uma hidratação 1,4, formando um diálcool.
→ Alcadieno isolado
Trata-se de um alcadieno que apresenta as duas ligações duplas envolvendo simultaneamente pelo menos cinco átomos de carbono, ou seja, existem pelo menos duas ligações simples separando os carbonos envolvidos nas ligações duplas.
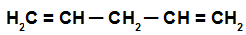
Fórmula estrutural de um alcadieno isolado
Durante a reação de hidratação de um alcadieno isolado, as ligações pi são rompidas, sendo os H+ adicionados aos carbonos mais hidrogenados e os OH- adicionados aos carbonos menos hidrogenados.
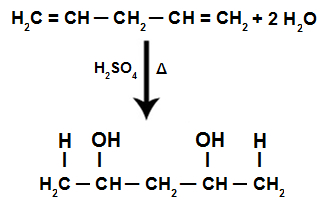
Equação da reação de hidratação de alcadieno isolado
Logo, na adição de um alcadieno isolado, temos a formação de um diálcool apenas.
Por Me. Diogo Lopes Dias