Uma reação de oxidação em compostos orgânicos ocorre quando há a entrada de oxigênio (ou saída de hidrogênio) na molécula orgânica.
| Uma oxidação branda só ocorre em hidrocarbonetos com insaturação, ou seja, com duplas (alcenos) ou triplas (alcinos) ligações. |
Para que hidrocarbonetos saturados oxidem, é necessária uma oxidação mais energética.
A oxidação branda utiliza o reativo de Baeyer, que corresponde a uma solução aquosa de permanganato de potássio (KMnO4) em meio neutro ou ligeiramente alcalino (básico – OH1-), a frio. Esse reativo é assim chamado porque o químico alemão Adolf Von Baeyer propôs um teste, chamado de teste de Baeyer, para identificar alcenos e seus isômeros ciclanos.
Esse teste funciona da seguinte maneira: como veremos mais à frente, um alceno reage com o permanganato de potássio, dessa forma a sua coloração, inicialmente violeta, fica incolor e há o surgimento de um precipitado marrom (MnO2). No entanto, os ciclanos não reagem com o permanganato de potássio. Assim, se a solução permanecer violeta, é um ciclano.
A figura abaixo mostra que o teste deu positivo para alcenos apenas no tubo de ensaio da esquerda, pois apareceu o precipitado marrom.

A reação de oxidação dos alcenos se inicia da decomposição do permanganato, produzindo o oxigênio:
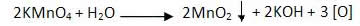
Oxidação branda de alcenos:
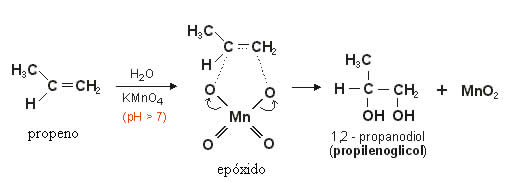
Esse oxigênio produzido reagirá com a dupla ligação do alceno formando um epóxido que, posteriormente, através da hidrólise, transforma-se em um diálcool ou diol vicinal (glicol), isto é, dois grupos OH em carbonos vizinhos.
No exemplo abaixo vemos a oxidação branda do propeno:
Oxidação branda de alcinos:
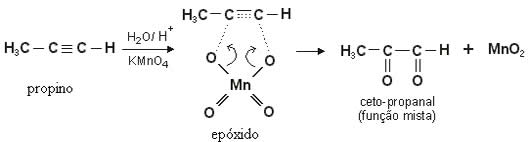
No caso dos alcinos, o produto formado será dicetonas. Com exceção do etino (HC≡CH), onde houver dois hidrogênios ligados em cada carbono participante da ligação tripla, será formado um aldeído.
Observe a oxidação branda do propino, com formação de uma dicetona:
Por Jennifer Fogaça
Graduada em Química
Equipe Brasil Escola



