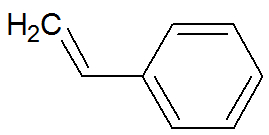
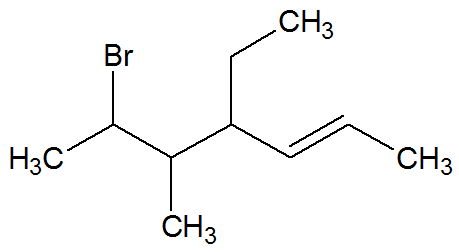
Os compostos organoclorados fazem parte da função orgânica dos haletos orgânicos. Os haletos são formados pela substituição de um ou mais hidrogênios ligados ao carbono pela mesma quantidade de halogênios (elementos da família 17 da tabela periódica). Quando o halogênio é o cloro, temos um composto organoclorado.
A nomenclatura dos organoclorados segue a seguinte regra:
Quantidade de Cl (mono*, di, tri etc.) + cloro + nome do hidrocarboneto
*O prefixo mono é opcional (normalmente ele não é colocado).
Exemplos:
H3C ─ Cl: Clorometano
H3C ─ CH2 ─ Cl: Cloroetano
Cl ─ CH2 ─ Cl: Diclorometano
Cl ─ CH ─ Cl: Triclorometano
│
Cl
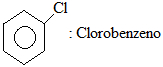
Fórmula do clorobenzeno
Na maioria dos casos, é necessário indicar a localização do cloro, que, nesse caso, não é considerado como o grupo funcional, mas sim como um substituinte. Isso significa que, ao numerar a cadeia principal, não começamos necessariamente o mais próximo do cloro, mas começamos o mais próximo de uma insaturação. Se não há insaturação, mas ramificações, adotamos a regra dos menores números possíveis. Veja os exemplos a seguir:
Cl
│
H3C ─ CH2 ─ CH2 ─ CH ─ CH3: 2-cloropentano
Cl
│
H2C ═ CH ─ CH2 ─ CH ─ CH3: 4-cloropent-1-eno (veja que não é o 2-cloropent-4-eno, pois se começa a numerar a cadeia o mais próximo da insaturação);
CH3
│
H3C ─ CH ─ CH2 ─ Cl: 1-cloro-2-metilpropano (veja que não é 3-cloro-2-metilpropano por causa da regra dos menores números possíveis);
CH3 Cl
│ │
H3C ─ CH ─ CH2 ─ CH ─ CH2 ─CH3: 4-cloro-2-metil-hexano (veja que não é 3-cloro-5-metil-hexano).
Hoje em dia, existem cerca de onze mil organoclorados produzidos industrialmente, que são utilizados em várias áreas, como na produção de plásticos e pesticidas, principalmente, e em pastas de dentes e soluções para higiene bucal.
Dentre os principais compostos organoclorados, podemos destacar:
*Clorofórmio: é o triclorometano (CHCl3) mostrado a seguir. Antigamente ele era usado como anestésico por inalação em cirurgias, mas esse uso deixou de ser aplicado quando se descobriu que ele era tóxico e podia levar à morte, como já ocorreu. Mais detalhes sobre esse aspecto podem ser vistos no texto Composição e Aplicações do Clorofórmio.
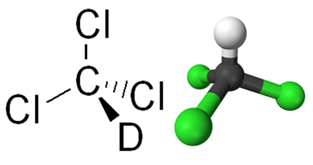
Fórmula estrutural do clorofórmio
*Inseticidas: Dois exemplos de inseticidas organoclorados são o BHC (hexaclorobenzeno) e o DDT (diclorodifeniltricloroetano), cuja nomenclatura oficial é 1,1,1-tricloro-2,2-di (p-clorofenil)etano.
O DDT foi usado pela primeira vez em 1942, durante a Segunda Guerra Mundial, para combater o mosquito transmissor da malária e outras doenças, como a febre amarela, além de impedir também que piolhos transmitissem a tifo. O DDT foi muito eficaz nesse sentido, porém, ele foi banido em muitos países. Nos países em que ele ainda é permitido, o seu uso é controlado.
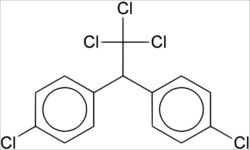
Fórmula estrutural do DDT
Os pesticidas organoclorados estão bastante em evidência principalmente por causa dos problemas ambientais que eles causam, configurando-se, assim, como uma questão bastante complexa e que gera divergências de opiniões.
Os que são contra o seu uso apontam para o fato de que eles são compostos que têm alta persistência no ambiente (alta resistência à degradação química e biológica) e alta solubilidade em lipídios, isto é, acumulam-se em tecidos gordurosos do organismo humano e animal, trazendo sérios problemas, principalmente ao fígado.
O DDT também é “acusado” de dizimar populações inteiras de aves, focas, entre outros animais, de atacar as cascas dos ovos das aves, de ser causador de câncer nos seres humanos e de alterar os níveis hormonais, provocando feminilização de machos, defeitos congênitos, infertilidade, depressão do sistema imunológico e comprometimento das funções mentais.
* Dioxinas: Grupo de compostos organoclorados bioacumulativos e tóxicos. O mais perigoso é o 2,3,7,8-TCDD (2,3,7,8-tetraclorodibenzo-p-dioxina).
Essa substância é liberada principalmente na queima de compostos clorados, como na incineração do PVC. É liberada também na produção do PVC, na utilização do cloro como alvejante na indústria de papel, durante a produção de herbicidas seletivos e pode aparecer em alguns alimentos de origem animal (como o ovo), pois a dioxina acumula-se ao longo da cadeia alimentar.
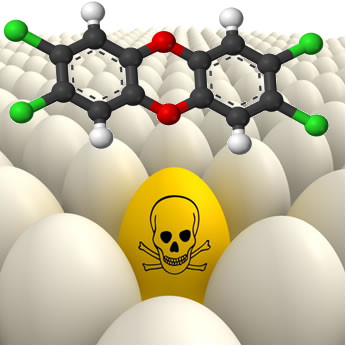
A dioxina pode aparecer em ovos em virtude de seu efeito acumulativo
* Plástico PVC (Policloreto de vinila): é um polímero formado pela adição sucessiva de várias moléculas de cloreto de vinila:
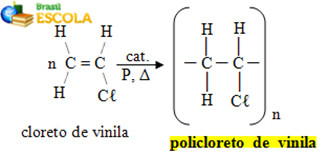
Reação de formação do policloreto de vinila
Esse plástico é usado como substituto do couro, na fabricação de sapatos, bolsas e roupas; na forração de móveis e no estofamento de automóveis. É usado também em películas para embalar alimentos e em fraldas, toalhas de mesa, cortinas de banheiro, revestimento de fios e cabos elétricos. Vale ressaltar que a principal aplicação do PVC rígido é em tubos para encanamentos.
Por Jennifer Fogaça
Graduada em Química




.jpg)