A resposta para a pergunta o que é solução saturada é muito simples, pois, trata-se de uma mistura que apresenta a maior quantidade de soluto que certa quantidade solvente consegue dissolver a uma determinada temperatura.
Como na solução saturada o solvente sempre dissolve o máximo de soluto, teremos visualmente, nesse caso, um sistema homogêneo, ou seja, com apenas uma fase.

Representações de soluções saturadas
Assim, se adicionarmos qualquer quantidade a mais do soluto na solução saturada, não haverá dissolução completa e essa quantidade adicionada a mais ficará no fundo do recipiente, se mais densa que o solvente, ou na superfície, se menos densa que o solvente.
A solução saturada, com quantidade de soluto que se aglomera no fundo do recipiente, pode receber um dos títulos propostos abaixo:
-
Solução saturada com precipitado;
-
Solução saturada com corpo de chão;
-
Solução saturada com corpo de fundo.
Anuncie aqui
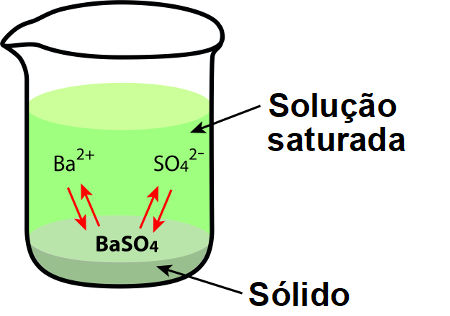
Representação de uma solução saturada com precipitado
Sem conhecer o coeficiente de solubilidade, que é a quantidade máxima de soluto que um solvente consegue dissolver a uma determinada temperatura, não é possível determinar se uma solução é saturada.
A seguir, veja alguns exemplos de formação de soluções.
1º Exemplo: Uma solução foi preparada com a adição de 20 g do soluto X a 100 g solvente Y a 10 oC. Sabendo que o coeficiente de solubilidade é de 15 g do soluto X por 100 g de solvente a 10 oC, podemos afirmar que temos uma solução saturada?
O coeficiente de solubilidade indica que 100 g do solvente Y dissolvem 15 g de soluto X a 10 oC. Como a solução foi preparada utilizando 20 g de X em 100 g de Y, logo o solvente dissolverá o seu limite, que é 15 g, e sobrarão 5 g de soluto não dissolvidos. Portanto, essa é uma solução saturada com corpo de fundo.
2º Exemplo: Uma solução foi preparada adicionando 40 g do soluto X a 200 g solvente Y a 25 oC. Sabendo que o coeficiente de solubilidade é de 20 g do soluto X por 100 g de solvente a 25 oC, podemos afirmar que se trata de uma solução saturada?
O coeficiente de solubilidade indica que 100 g do solvente Y podem dissolver 20 g de soluto X a 25 oC. A solução foi preparada utilizando 40 g de X em 200 g de Y, logo o solvente dissolverá o seu limite, pois 200 g de solvente dissolvem 40 g de soluto, assim como 100 g de solvente dissolvem 20 g de soluto. Portanto, temos uma solução saturada.
3º Exemplo: Uma solução foi preparada adicionando 25 g do soluto X a 100 g solvente Y a 30 oC. Sabendo que o coeficiente de solubilidade é de 35 g do soluto X por 100 g de solvente a 30 oC, podemos afirmar que temos uma solução saturada?
O coeficiente de solubilidade indica que 100 g do solvente Y dissolvem 35 g de soluto X a 30 oC. A solução foi preparada adicionando 25 g de X a 100 g de Y, assim, o solvente dissolverá uma quantidade inferior ao seu limite, que é 35 g, faltando 10 g de soluto para atingir o seu máximo de dissolução. Portanto, temos uma solução que não é saturada.
Atenção: Quando o solvente dissolve uma quantidade abaixo do seu limite, forma-se uma solução insaturada.
Por Me. Diogo Lopes Dias