Os estados físicos da água são os estados de agregação que essa substância pode apresentar de acordo com as condições de temperatura e pressão. A água pode se apresentar em três estados diferentes para nós:
- sólido (gelo);
- líquido (água);
- gasoso (gás).
Os estados físicos da água podem ser atingidos em temperaturas diferentes quando em pressões diferentes. Por exemplo, o arranjo cristalino da água na fase gelo permite que, quanto maior a pressão, menor será a temperatura de fusão. A água também é capaz de sublimar, porém apenas em baixas pressões (0,006 atm).
Leia também: Quais são os estados físicos da matéria?
Tópicos deste artigo
- 1 - Resumo sobre os estados físicos da água
- 2 - Quais são os estados físicos da água?
- 3 - Mudanças de estado físico da água
- 4 - Exercícios resolvidos sobre estados físicos da água
Resumo sobre os estados físicos da água
- Os estados físicos da água são os estados de agregação dessa substância em função da temperatura e pressão.
- A água pode se apresentar na forma sólida, líquida e gasosa.
- Em pressão do nível do mar (1 atm), a água se funde a 0 °C e se vaporiza aos 100 °C.
- A água pode apresentar, pelo menos, 10 formas diferentes de gelo, sendo apenas uma estável em condições ambiente.
- A água só pode se sublimar em condições de baixíssima pressão (0,006 atm).
- O gelo se cristaliza de uma forma não convencional, fazendo com que, quanto maior a pressão, menor será a temperatura de fusão da água.
Quais são os estados físicos da água?
Os estados físicos da água são os estados de agregação que a água apresenta em diferentes condições de temperatura e pressão. A água pode se apresentar em três estados físicos: sólido, comumente conhecido como gelo; líquido, o mais comum nas condições ambiente e, por isso, chamado de água; e o gás, o qual ocorre quando as moléculas estão mais espaçadas, com baixa interação intermolecular.
Mudanças de estado físico da água
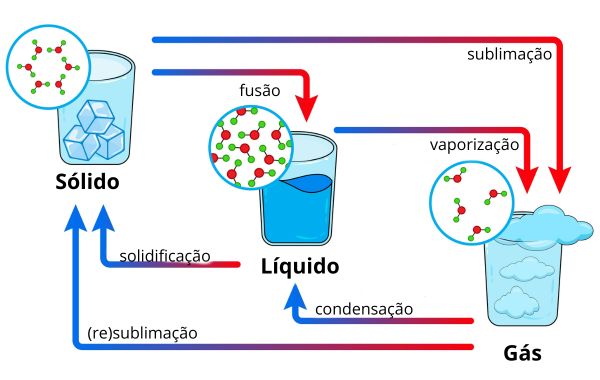
Em nível do mar, quando a pressão atmosférica é de 1 atmosfera (760 Torr), a água muda de fase aos 0 °C (quando se solidifica ou se funde) e aos 100 °C (quando se vaporiza ou se condensa). Para fundir-se, vaporizar-se e sublimar-se, a água precisa absorver energia na forma de calor. Do contrário, para solidificar-se, condensar-se e ressublimar-se (sólido para gás), deve perder energia na forma de calor.
A explicação para tal relação é que, durante a fusão, vaporização e sublimação, as interações intermoleculares devem ser rompidas, e, para tal, há necessidade de energia. Do contrário, durante a solidificação, condensação e ressublimação, as moléculas de água perdem energia cinética com o estabelecimento das interações intermoleculares e a energia sobressalente é liberada na forma de calor.
Nessas condições de pressão, a água não pode sofrer sublimação (quando o sólido passa diretamente para o gás e vice-versa). Tal mudança só é possível em pressões menores que 0,006 atmosfera (4,6 Torr). É também nessa pressão que ocorre o ponto triplo da água, ou seja, quando os três estados físicos (sólido, líquido e gasoso) coexistem.
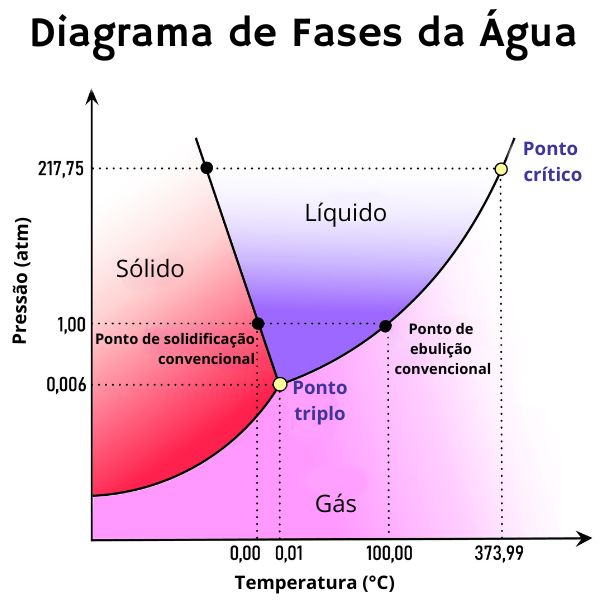
Tais valores são determinados experimentalmente e podem ser vistos no diagrama de fases da água. Esse gráfico apresenta uma leitura mais abrangente das temperaturas de mudança de estado físico da água em diferentes condições de pressão.
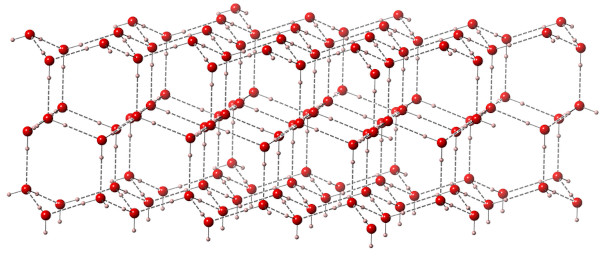
Uma curiosidade interessante é que a água apresenta, pelo menos, 10 formas de gelo diferentes, o que é consequência da forma como as moléculas da água se acomodam. Contudo, apenas uma dessas formas é estável em pressões ordinárias.
Ainda sobre o gelo, a fase sólida da água apresenta um volume maior que a fase líquida durante a fusão. A consequência é que, quanto maior for a pressão, menor será a temperatura de fusão do gelo. O que ocorre é que as ligações de hidrogênio na fase de gelo deixam as moléculas de água num arranjo hexagonal, e, ao ocorrer a fusão, parte dessas ligações de hidrogênio é rompida, permitindo uma maior aproximação das moléculas de água.
Exercícios resolvidos sobre estados físicos da água
Questão 1 (Cesmac Medicina/2020-2) A liofilização é um método muito utilizado na indústria alimentícia para desidratar alimentos, o qual submete o alimento à baixa temperatura (-197 °C) e pressão, para que a água presente no estado sólido, passe diretamente para o estado gasoso.
A passagem da água diretamente do estado sólido para o gasoso é considerada um processo de:
(A) vaporização
(B) sublimação
(C) liquefação
(D) solidificação
(E) fusão
Resposta: Letra B
Como a questão informa, durante a liofilização, baixas temperatura e pressão são aplicadas ao alimento para que a água passe do estado sólido para o estado gasoso. Tal mudança configura uma sublimação.
Questão 2 (Cesmac Medicina/2020-1) As temperaturas alcançadas no planeta Terra permitem a ocorrência da água em seus três estados físicos principais: sólido, líquido e gasoso. O diagrama de fases da água está descrito abaixo:
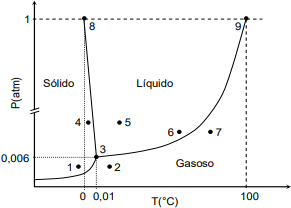
Acerca do diagrama de fases da água, sabendo que ao nível do mar a pressão atmosférica é 1 atm, é incorreto afirmar:
(A) A transição de fase do ponto 1 para 2 corresponde à sublimação.
(B) O ponto 3 corresponde ao ponto triplo da água.
(C) A transição de fase do ponto 4 para 5 corresponde à liquefação.
(D) A transição de fase do ponto 7 para 6 corresponde à condensação.
(E) Os pontos 8 e 9 correspondem aos pontos de fusão e ebulição à pressão atmosférica, respectivamente.
Resposta: Letra C
Em (4) a água se apresenta no estado sólido e em (5) a água se apresenta no estado líquido. Assim sendo, a transição de (4) para (5) é uma passagem de sólido para líquido, ou seja, uma fusão, e não uma liquefação.
Fontes:
DO CANTO, E. L.; LEITE, L. L. C.; CANTO, L. C. Química – na abordagem do cotidiano. 1. ed. São Paulo: Moderna, 2021.
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: Questionando a vida e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.




