A destilação fracionada é uma técnica específica de destilação que permite uma separação mais efetiva ou um fracionamento da mistura inicial em diversos produtos. Como toda destilação, é aplicada em uma mistura homogênea líquida e se baseia nas diferenças dos pontos de ebulição dos componentes da mistura. A destilação fracionada apresenta uma performance melhor que a destilação simples.
A destilação fracionada apresenta uma coluna de fracionamento, que aumenta o caminho percorrido pelo vapor originado a partir do aquecimento da mistura inicial, garantindo uma melhor separação dos componentes. Tal técnica é muito empregada na indústria, principalmente no refino do petróleo e na separação dos gases da atmosfera.
Leia também: Quais são os métodos de separação de misturas?
Tópicos deste artigo
- 1 - Resumo sobre a destilação fracionada
- 2 - O que é destilação fracionada?
- 3 - Como funciona a destilação fracionada?
- 4 - Para que serve a destilação fracionada?
- 5 - Exemplos de destilação fracionada
- 6 - Quais as diferenças entre destilação fracionada e destilação simples?
- 7 - Exercícios resolvidos sobre destilação fracionada
Resumo sobre a destilação fracionada
- A destilação fracionada é uma modalidade de destilação que permite uma separação mais efetiva ou um fracionamento da mistura inicial em diversos produtos.
- Como toda destilação, baseia-se na diferença das temperaturas de ebulição dos componentes da mistura homogênea líquida.
- A destilação fracionada apresenta uma separação mais efetiva do que a destilação simples.
- A destilação fracionada conta com uma coluna de fracionamento, que garante que o vapor percorra um caminho maior e, assim, apresente uma melhor separação dos componentes.
- A destilação fracionada é amplamente empregada na indústria, principalmente no refino do petróleo ou na obtenção de gases presentes na atmosfera.
O que é destilação fracionada?
A destilação fracionada é uma técnica específica de destilação e é aplicada para separar os componentes de uma mistura homogênea por meio de suas diferenças de pontos de ebulição.
No caso específico da destilação fracionada, tal técnica é mais rebuscada, uma vez que permite uma separação mais efetiva dos componentes da mistura, bem como a obtenção de diversos destilados com composições químicas distintas, ou seja, permite o devido fracionamento da mistura em diversos derivados.
Como funciona a destilação fracionada?
O sucesso da destilação fracionada depende do estabelecimento de um efeito conhecido como retificação, muitas vezes descrito como um "efeito cascata". Porém, embora os pressupostos teóricos da destilação fracionada sejam universais, a sua aplicação muda consideravelmente quando comparamos a escala laboratorial e a industrial.
No caso dos laboratórios, utiliza-se uma coluna de fracionamento, cuja dimensão deve ser suficiente para a criação de um gradiente de temperatura adequado para a separação. Para ilustrar o fenômeno, considere uma mistura binária composta por uma substância A (mais volátil/menor ponto de ebulição) e uma substância B (menos volátil/maior ponto de ebulição).
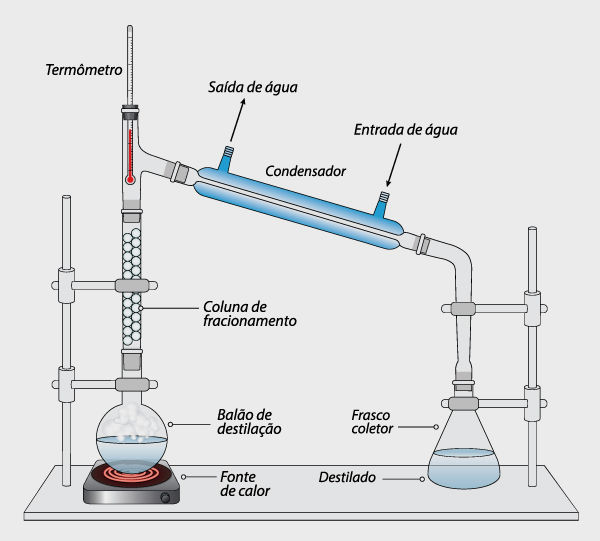
Ao aquecer a mistura, o vapor gerado é composto majoritariamente pelo componente A, embora ainda carregue frações de B. Ao atingir o topo da coluna, onde o ambiente é mais frio (por conta do gradiente de temperatura), ocorre uma condensação parcial. Esse condensado inicia um fluxo descendente pela coluna de fracionamento, criando uma contracorrente líquida.
O líquido descendente é rico no componente B. À medida que desce pela coluna, ele interage com o vapor ascendente. Esse encontro promove uma troca de massa: o vapor ascendente retira possíveis moléculas do componente A que está no líquido, enquanto o líquido descendente absorve moléculas do componente B presentes no vapor. Esse ciclo de evaporação e de condensação sucessivas enriquece o vapor no componente mais volátil (A), que finalmente alcança o topo da coluna de fracionamento. Com o tempo, a concentração de A na mistura original diminui drasticamente, até que o volume de destilado obtido se reduz ao ponto de encerrar o processo.
Na indústria, a lógica de separação é análoga, porém adaptada para grandes volumes. A coluna é substituída por torres de destilação que podem atingir dezenas de metros, e a alimentação da mistura ocorre geralmente em uma seção intermediária da torre, a qual é calculada de acordo com o projeto.
No interior dessas torres, o contato entre as fases ocorre em pratos perfurados ou em bandejas, dispostos em diferentes alturas, para que possuam níveis de temperatura diferentes. O vapor sobe através das perfurações desses pratos, enquanto o líquido descende por vertedouros laterais em um movimento de zigue-zague. A pressão do vapor ascendente impede que o líquido caia pelos furos, forçando uma mistura íntima entre as fases em cada estágio (prato), o que garante uma separação de alta eficiência em larga escala.
Para que serve a destilação fracionada?
A destilação fracionada funciona como uma técnica para separação de componentes de misturas homogêneas por conta da diferença dos pontos de ebulição. Assim sendo, é útil na recuperação e na purificação de solventes, na produção de bebidas alcoólicas e na extração de óleos essenciais, por exemplo.
O maior uso da destilação fracionada está no refino de petróleo, em que o petróleo é vaporizado e inserido em uma coluna de destilação. Cada prato da coluna de destilação apresentará derivados diferentes, como a gasolina, o diesel, o querosene de aviação e os lubrificantes. Os rejeitos da destilação fracionada do petróleo também são aproveitados, utilizados, por exemplo, para a produção de asfalto.

Outro uso muito comum da destilação fracionada na indústria é na separação dos componentes do ar atmosférico (majoritariamente N2, O2 e Ar). No caso, os gases lá presentes são resfriados e pressurizados até sua condensação. Uma vez liquefeitos, são destilados, com a obtenção dos componentes em frações distintas.
Exemplos de destilação fracionada

- Refino de petróleo: a destilação fracionada é o ponto de partida em uma refinaria de petróleo. Basicamente, todas as refinarias de petróleo exigem a etapa de destilação fracionada. No caso, o petróleo é completamente vaporizado e inserido em uma coluna de destilação. Lá, em cada prato (ou bandeja), são obtidos destilados de composições químicas diferentes (frações), de acordo com a temperatura de ebulição dos componentes. Dessa forma, tem-se o pontapé inicial para a produção de diversos combustíveis, como gasolina, diesel e querosene de aviação, além de lubrificantes, de óleos e de asfalto.
- Separação dos componentes do ar: a separação dos gases nitrogênio (N2), oxigênio (O2) e argônio (Ar) presentes no ar atmosférico é feita em larga escala por meio de uma destilação fracionada. Por meio de pressurização e de queda brusca de temperatura, esses componentes são liquefeitos e, posteriormente, são destilados.
Quais as diferenças entre destilação fracionada e destilação simples?
→ Destilação simples
A destilação simples é caracterizada por um arranjo experimental mais direto, projetado para separar uma mistura em duas frações principais. O processo, claro, também se baseia no aquecimento da fase líquida para gerar um vapor progressivamente enriquecido no componente mais volátil (aquele que possui menor ponto de ebulição e, consequentemente, maior pressão de vapor). Esse vapor é direcionado ao condensador, mas sem passar por uma coluna de fracionamento, onde retorna ao estado líquido e é coletado como destilado. O material remanescente no balão de aquecimento, concentrado no componente de menor volatilidade, é também denominado resíduo.
Porém, na destilação simples, a separação completa é raramente atingida. O que se obtém, na verdade, são duas frações que ainda contêm os componentes originais, embora em proporções distintas das iniciais. Por essa limitação, costuma-se indicar a destilação simples apenas para misturas cujos componentes apresentem uma diferença de temperatura de ebulição superior a 50 °C. Caso a diferença de temperaturas de ebulição dos componentes seja muito próxima, tanto o resíduo quanto o destilado apresentarão uma composição parecida, mostrando que a separação foi ineficiente.
→ Destilação fracionada
Para superar as lacunas da destilação simples, recorre-se à destilação fracionada. A lógica por trás deste método consiste em promover uma sucessão de destilações simples em um único ciclo, criando o já citado fenômeno de cascata.
Diferentemente da destilação simples, na destilação fracionada, o destilado percorre um caminho maior até o condensador, por meio da coluna de fracionamento. Lá, uma parcela do destilado retorna ao sistema na forma de fluxo líquido descendente, estabelecendo um contato íntimo com o vapor que sobe. É essa interação contínua em contracorrente que garante uma separação mais efetiva, pois o contato entre o vapor ascendente e o líquido descendente permite um enriquecimento dessas partes.
Confira também: Destilação simples e destilação fracionada — mais detalhes sobre essas duas técnicas de separação de misturas
Exercícios resolvidos sobre destilação fracionada
Questão 1
(UnirG) Análise feita pela Marinha e pela Petrobrás na massa de coloração escura que poluiu as praias do Nordeste apontou que se trata da substância de hidrocarboneto, conhecida como piche, que é um dos produtos da destilação do petróleo.
Além do piche, outro produto não volátil também resultante da destilação fracionada do petróleo é o
A) querosene.
B) asfalto.
C) diesel
D) óleo lubrificante.
Resolução:
Alternativa B.
Ao realizar a destilação fracionada do petróleo, os produtos não voláteis são tratados como rejeitos. São componentes de alto volume molecular e alta massa molecular. Nesse caso, além do piche, também se destaca como resíduo o asfalto.
Questão 2
(UNIFIPMoc) Um aluno misturou água e acetona indevidamente. Para separar os componentes da mistura, realizou uma destilação fracionada, retirando amostras do resíduo e do destilado durante o processo de separação, representada de acordo com esquema a seguir.

Dados:
T.E.água = 100 °C
T.E.acetona = 56 °C
Nesse processo de separação, a:
A) temperatura de ebulição do destilado é maior que a do resíduo ao final da destilação.
B) pressão de vapor das amostras do resíduo torna-se maior no término da destilação.
C) temperatura de ebulição das amostras do destilado permanece constante.
D) temperatura de ebulição do destilado se iguala à do resíduo no início da operação.
E) pressão de vapor do resíduo é menor que a do destilado nas amostras recolhidas.
Resolução:
Alternativa E.
O resíduo é o componente menos volátil e, dessa forma, possui maior ponto de ebulição e, consequentemente, menor pressão de vapor. Já o destilado é o componente mais volátil e, dessa forma, possui o menor ponto de ebulição e, consequentemente, a maior pressão de vapor.
Fontes
PETLYUK, F. B. Distillation Theory and Its Application to Optimal Design of Separation Units. 1a ed. Cambridge, Reino Unido: Cambridge University Press, 2004.
VOGELPOHL, A. Distillation – The Theory. 4a ed. Berlim, Alemanha: de Gruyter, 2015.
SMITH, R.; JOBSON, M. Distillation. In: Encyclopedia of Separation Science. 1a ed. p. 1117-1134. Estados Unidos: Academic Press, 2000.
SPEIGHT, J. G. The Chemistry and Technology of Petroleum. 5ª ed. Flórida, EUA: CRC Press, 2014.
MICHELL INSTRUMENTS. Air separation process: application note. Ely, UK: Michell Instruments, . 1 arquivo (2 p.). Disponível em: http://www.michell.com/downloads/appnotes/Air-Separation-Process-App-Note.pdf.
ROYAL SOCIETY OF CHEMISTRY. Everything you need to teach fractional distillation. London: RSC, 2022. Infográfico. Disponível em: https://edu.rsc.org/infographics/everything-you-need-to-teach-fractional-distillation/4016691.article.
CHEMICALS.CO.UK. What is fractional distillation? [S. l.]: Chemicals.co.uk, 2024. Disponível em: https://www.chemicals.co.uk/blog/what-is-fractional-distillation.