A capacidade que as ligações possuem de atrair cargas elétricas se define como Polaridade, esta assume caráter diferente dependendo da ligação onde se faz presente.
Em relação à ligação iônica e covalente, esta última faz com que a molécula seja apolar. A molécula onde a ligação iônica é responsável por manter átomos unidos apresenta polaridade.
A ligação predominante entre os compostos orgânicos é a covalente, portanto se tornam na maioria compostos apolares. As longas cadeias carbônicas presentes em substâncias orgânicas não lhes permitem outro caráter senão o apolar.
A explicação vem do fato de que a ligação ocorre entre elementos iguais (C-C), portanto possuem mesma escala de eletronegatividade. Veja um exemplo:
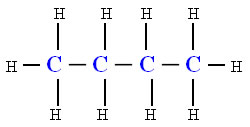
Molécula apolar
O butano representado pela estrutura acima é um gás, repare que os átomos ligantes são iguais (4 carbonos ligados entre si).
Mas não significa que todo composto orgânico seja apolar, a presença de outros átomos entre carbonos dá à molécula caráter polar. Confira o exemplo:
.jpg)
Molécula polar
A presença da Hidroxila OH (Oxigênio ligado a hidrogênio) fez com que a molécula do composto orgânico Etanol passasse a exibir polaridade.
O Butano é usado como gás de isqueiros e o Etanol é o chamado álcool comum.
Por Líria Alves
Graduada em Química
Equipe Brasil Escola
Veja mais!
Propriedades dos compostos orgânicos
Polaridade – Saiba por que a eletronegatividade influi na polaridade de uma ligação.
Polaridade das ligações iônica e covalente
Química Orgânica - Química - Brasil Escola


