As reações de adição são importantes ações no que se diz respeito às sínteses orgânicas, pois através delas um número interessante de substâncias orgânicas podem ser desenvolvidas.
Para que ocorra a reação de adição é necessária a criação de dois sítios de ligação na cadeia carbônica, o que ocorre de forma simples quando a cadeia é insaturada (presença de ligação pi). Dessa forma, ao ser rompida a ligação pi, os sítios surgem na cadeia.
Um grupo de substâncias que podem ser utilizadas nas sínteses de adição são cicloalcanos ou ciclanos, grupo de hidrocarbonetos de cadeias cíclicas e saturadas. Eles fogem à regra geral da adição por não possuírem ligação pi, porém dependendo de algumas condições (calor, metal catalisador, meio ácido) eles podem sofrer uma quebra na cadeia, entre dois átomos de carbono, fazendo com que surjam dois sítios de ligação para que a adição seja efetivada. Porém, existe um fato que restringe a utilização destes compostos. O fato é a chamada teoria das tensões dos anéis, proposta por Adolf V. Bayer em 1885.
Para que a ligação sigma entre os carbonos seja rompida é necessário que haja uma certa instabilidade entre os carbonos. Essa instabilidade está relacionada ao ângulo das ligações entre os carbonos. De acordo com Bayer, o ângulo que fornece uma grande estabilidade para a ligação sigma é o de 109,47O. Assim, as cadeias que tiverem um ângulo entre os carbonos menor que 109,47O tendem a ter instabilidade nas ligações sigma entre os carbonos que formam as cadeias, o que favorece a sua ruptura aliado a uma condição externa ideal.
Os únicos cicloalcanos que apresentam ângulo menor que 109,47O entre seus carbonos são ciclopropano (60O), ciclobutano (90O) e ciclopentano (108O). O ciclopentano por ter uma angulação muito próxima de 109,47O apresenta ligações sigma bastante estáveis, por conta disso ele não pode sofrer qualquer reação de adição. Abaixo temos as estruturas desses três cicloalcanos:

Fórmula estrutural do ciclopropano, ciclobutano e ciclopentano, respectivamente
Observação: Qualquer cicloalcano que apresentar mais de 5 carbonos na cadeia irá realizar reação de substituição por exemplo, e jamais uma adição pelo fato de as ligações sigma entre seus átomos de carbono serem extremamente estáveis.
As reações de adição que podem acontecer com cicloalcanos são basicamente todas, porém com o ciclopentano as únicas que ele pode sofrer são hidrogenação e halogenação. Segue abaixo exemplos das adições com os cicloalcanos e suas condições de ocorrência:
a) Hidrogenação
Reação do cicloalcano com a molécula de hidrogênio com presença do catalisador metálico em pó (zinco, níquel ou platina) em presença de aquecimento (em torno de 180OC). Nessa reação o cicloalcano dará origem a um alcano. Nessa reação, após a quebra do ciclo temos a adição de um átomo de hidrogênio em cada um dos carbonos da ligação sigma que foi quebrada.
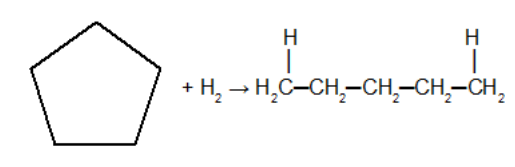
Reação de adição no ciclobutano utilizando hidrogênio
b) Halogenação
Reação do cicloalcano com a molécula de halogênio (cloro, bromo, iodo, por exemplo) com presença do catalisador cloreto de ferro III (FeCl3). Nessa reação o cicloalcano dará origem a um haleto orgânico com dois átomos de halogênio na cadeia. Após a quebra do ciclo temos a adição de um átomo de halogênio em cada um dos carbonos da ligação sigma que foi quebrada.
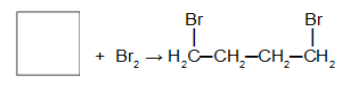
Reação de adição no ciclobutano utilizando bromo
c) Reação com Halogenidretos (haletos de ácido)
Reação do cicloalcano com a molécula de hidrácido inorgânico contendo halogênio (HCl. HBr, HI). Como é utilizado um ácido como reagente não se utiliza um catalisador. Nessa reação o cicloalcano dará origem a um haleto orgânico com apenas um átomo de halogênio na cadeia. Após a quebra do ciclo temos a adição de um átomo de hidrogênio em um dos carbonos da ligação sigma que foi quebrada e um halogênio no outro carbono. Obedecendo à regra de Markovnikov (H no carbono mais hidrogenado e halogênio no carbono menos hidrogenado).
Observação: Ela só ocorre com ciclopropano e ciclobutano.
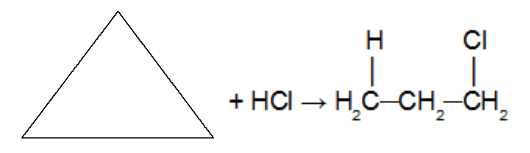
Reação de adição no ciclopropano utilizando ácido clorídrico
Observação: Ela só ocorre com ciclopropano e ciclobutano.
d) Hidratação
Reação do cicloalcano com uma molécula de água em presença de ácido sulfúrico e aquecimento. Nessa reação o cicloalcano dará origem a um mono álcool (álcool com apenas um grupo OH na cadeia). Após a quebra do ciclo temos a adição de um átomo de hidrogênio em um dos carbonos da ligação sigma que foi quebrada e uma hidroxila (OH) no outro carbono. Obedecendo à regra de Markovnikov (H no carbono mais hidrogenado e hidroxila no carbono menos hidrogenado).
Observação: Ela só ocorre com ciclopropano e ciclobutano.
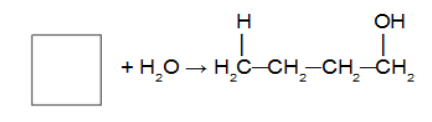
Reação de adição no ciclopropano utilizando ácido clorídrico
Por Me. Diogo Lopes Dias