A Química quântica estuda conceitos relacionados aos elétrons presentes na eletrosfera de um átomo. Essa ciência tem como base os princípios da mecânica quântica, foram eles que inspiraram o pesquisador Werner Heisenberg (1901-1976) a propor um modelo quântico para o átomo.
Antes de introduzir o conceito de Heisenberg, observe a eletrosfera de um átomo:
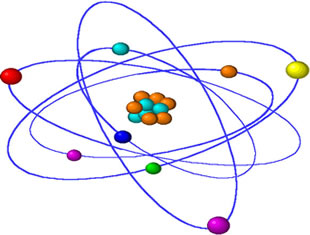
Com base na imagem acima podemos afirmar que:
- A eletrosfera, onde estão localizados os átomos, circula todo o núcleo atômico (composto por prótons e nêutrons);
- Os elétrons estão em movimento constante demonstrado pelas órbitas (anéis azuis).
Daria para saber onde exatamente um elétron se posiciona na eletrosfera? É claro que não, uma vez que estão sempre em movimento de rotação ao redor do núcleo.
Foi baseado neste questionamento que Heisenberg criou o "Princípio da Incerteza" onde, como o próprio nome sugere, não se pode afirmar que exista uma órbita definida para o elétron. No mesmo parâmetro introduziu o conceito de Orbitais: local onde existe a maior probabilidade de se encontrar um elétron.
Orbitais são considerados como nuvens onde se localizam os elétrons. Como a eletrosfera se localiza ao redor do núcleo, imagine os orbitais como sendo nuvens eletrônicas que circulam a parte central do átomo. Para um melhor entendimento, considere a ilustração:

No desenho acima, os orbitais são representados pelas formas ovais roxas e azuis. Repare que o núcleo do átomo é caracterizado pela presença das esferas amarela e rosa (prótons e nêutrons).
Por Líria Alves
Graduada em Química
Equipe Brasil Escola
Veja mais!



