As oses ou monossacarídeos são compostos que pertencem à classe dos glicídios, também chamados de carboidratos. Essa classe é caracterizada por conter funções mistas em sua estrutura, sendo que vários compostos são do grupo dos álcoois e um grupo é uma cetona ou um aldeído.
O que difere as oses dos demais glicídios é o fato de elas não hidrolisarem.
Como elas possuem vários carbonos assimétricos, as oses possuem vários isômeros ópticos. Lembre-se que isomeria é um fenômeno que ocorre quando dois ou mais compostos diferentes apresentam a mesma fórmula molecular, porém diferentes fórmulas estruturais.
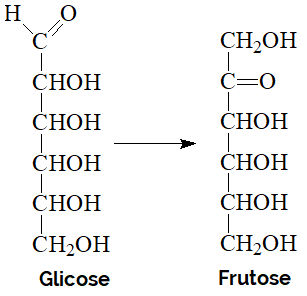
Por exemplo, a glicose e a frutose são oses que possuem a mesma fórmula molecular: C6H12O6. A diferença entre esses dois grupos é que os grupos funcionais dessas duas substâncias são diferentes. Conforme é possível visualizar abaixo, a glicose é do grupo dos aldeídos, portanto ela é considerada uma aldose; já a frutose é do grupo das cetonas, sendo designada como uma cetose.
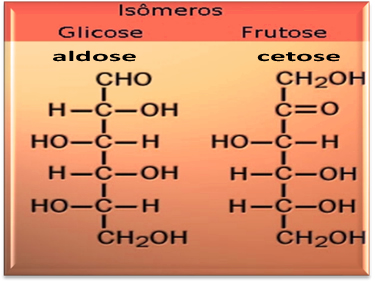
A glicose e a frutose são compostos isômeros.
A isomeria óptica denomina como dextrogiro (D) o isômero que desvia a luz polarizada para a direita; e como levogiro (L), o isômero que desvia a luz polarizada para o plano da esquerda.
Aplicando esse conceito para os isômeros das oses, considera-se que as oses sejam derivadas do aldeído glicérico. Esse composto possui dois isômeros ópticos ativos, pois ele possui um carbono assimétrico:
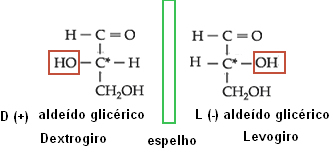
Isomeria do aldeído glicérico.
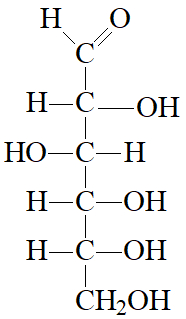
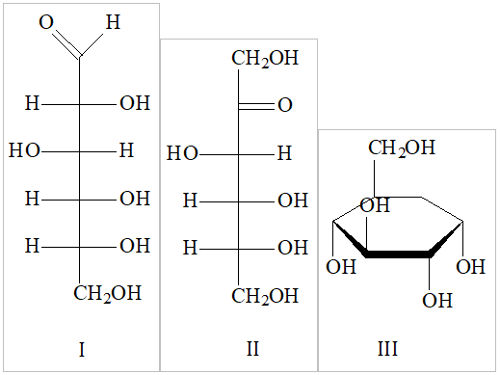
Assim, para todas as oses que possuem o grupo OH do lado direito do segundo carbono, contando de baixo para cima, o composto é considerado da série D. Porém, se o grupo OH estiver do lado esquerdo, ele será da série L. Os sinais positivo e negativo servem para indicar se o composto é dextrogiro ou levogiro, respectivamente. Abaixo temos alguns exemplos:
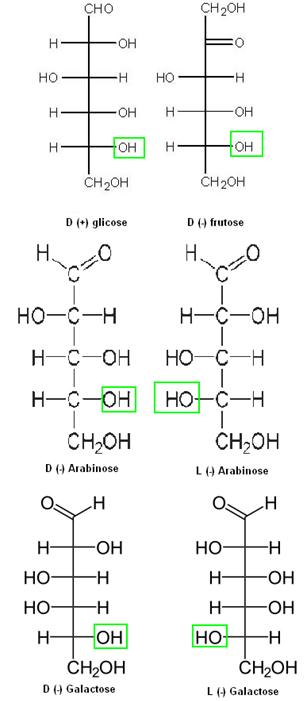
Exemplos de séries dextrogiras e levogiras do grupo das oses.
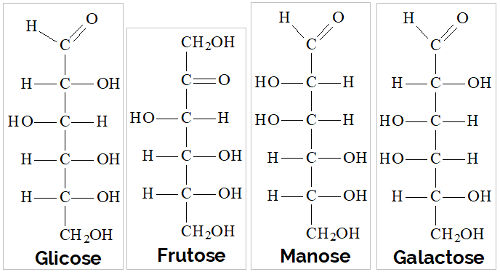
Observe que a D (+) glicose, a D (-) frutose e a D (-) arabinose se diferem apenas nos carbonos 1 e 2 (no sentido de cima para baixo). Quando isso ocorre, dizemos que esses compostos são epímeros.
Por Jennifer Fogaça
Graduada em Química