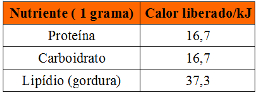
Para realizar as tarefas do cotidiano e manter as funções vitais de seu corpo, você precisa ter energia. Essa energia é derivada e reposta através do consumo de alimentos. Ao serem queimados em nosso organismo, os alimentos liberam uma quantidade de energia que depende da composição de cada um.
Essa quantidade de energia fornecida é denominada “caloria”, cujo símbolo é o cal. Podemos definir de maneira mais exata o que representa a caloria em termos de energia, da seguinte forma:

Por exemplo, se 1,0 g de açúcar elevar a temperatura de 1000 g de água em 4°C, isso significa que 1 g de água absorve 4 cal de energia. Mas, visto que a massa considerada é de 1000 g, a energia total absorvida é de 4000 cal ou 4 kcal.
Visto que os valores de calorias dos alimentos costumam ser muito grandes, a unidade cal quase não é utilizada. Utiliza-se mais o kcal (1 kcal = 103 cal ou 1 kcal = 1000 cal).
Em muitas embalagens de alimentos aparece o símbolo Cal (note a letra maiúscula), para representar os valores energéticos dos alimentos em “calorias nutricionais”, que na realidade quer dizer kcal.

Essa unidade (Cal) é utilizada somente por algumas pessoas do campo da saúde, mas deve ser evitada, pois não faz parte do SI. Essa situação gera muita confusão não só na questão dos alimentos, mas também quando se indica a quantidade de energia que será queimada pelo organismo através dos exercícios físicos. Observe que na tabela abaixo, que indica o conteúdo calórico de alguns alimentos, usam-se (de modo não recomendado, conforme já explicado) os termos Caloria e quilocaloria (kcal), como sinônimos:
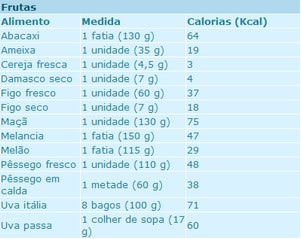
Apesar de essas unidades serem muito utilizadas, a unidade recomendada pelo SI (Sistema Internacional de Unidades) é o joule (1 cal = 4,18 J) ou o quilojoule (1 kcal = 4,18 kJ).

Na realidade, não são só os alimentos que liberam energia quando queimados. Um carvão, por exemplo, também libera energia quando queimado na forma de calor e luz. Outro exemplo é a queima da gasolina, em que 1 L libera 7 750 000 calorias. Assim, o termo “calorias” se aplica a qualquer fenômeno envolvendo trocas de calor.
Por Jennifer Fogaça
Graduada em Química