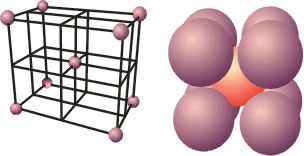
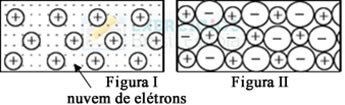
Se fosse possível visualizar a estrutura de um metal de forma bem nítida, veríamos como na imagem acima. A estrutura atômica dos metais é a Cristalina, que se constitui por cátions do metal envolvidos por elétrons.
Os retículos cristalinos presentes nos metais podem ser representados desta forma:
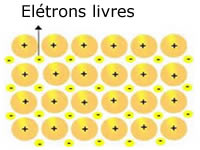
Representação do sódio (Na) metálico
Os retículos cristalinos dos metais são formados por um grupamento de cátions fixos.
Cada cátion Na+ está envolto por elétrons, mas estes se encontram deslocalizados, ou seja, não se sentem atraídos por nenhum núcleo.
Como não há atração entre cargas negativas (elétron) com o núcleo positivo (cátion), os elétrons livres acabam por ocupar todo o retículo cristalino do metal. A liberdade que os elétrons têm de se movimentar faz com que formem uma nuvem eletrônica.
A capacidade dos metais na condução de eletricidade se explica pela presença dessa nuvem. A corrente elétrica é resultante do contato de elétrons livres com outros metais.
Na composição de qualquer átomo, inclusive de metais como Sódio (Na), Ouro Au, Cobre (Cu), existe a camada de valência. Os elétrons se movimentam livremente por essa camada mantendo a atração eletromagnética pelos cátions. Essa propriedade estrutural permite a formação das moléculas metálicas e, consequentemente, dos próprios metais.
Por Líria Alves
Graduada em Química