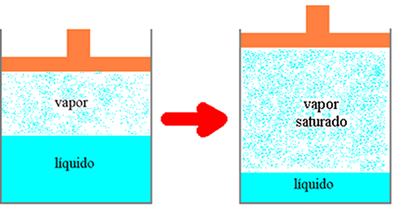
O que é pressão máxima de vapor?
Denominamos pressão máxima de vapor aquele tipo de pressão em que as fases gasosa e líquida coexistem em equilíbrio.

Escrito por: Domiciano Correa Marques da Silva
Escritor oficial Brasil Escola
Deseja fazer uma citação?
SILVA, Domiciano Correa Marques da.
"O que é pressão máxima de vapor?"; Brasil Escola.
Disponível em: https://brasilescola.uol.com.br/fisica/o-que-pressao-maxima-vapor.htm. Acesso em 04 de junho
de 2026.
Copiar
Videoaulas

📽 Reproduzindo
Artigos Relacionados
Pressão de vapor
Descubra o que é pressão de vapor e a sua relação com temperatura, ebulição e volatilidade. Entenda como esses conceitos impactam diversas substâncias.
Vaporização e condensação
Clique aqui e saiba mais sobre os fenômenos que envolvem a vaporização e a condensação, mudanças de estado físico que ocorrem com líquidos e gases.


