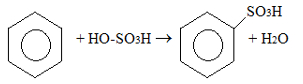
Reações de substituição, em geral, são aquelas em que há troca de pelo menos um átomo de hidrogênio da molécula de um hidrocarboneto por um grupo substituinte.
1- Nitração: Reação entre ácido nítrico (HNO3) e um composto orgânico.
Exemplo: Reação entre Benzeno e ácido nítrico.
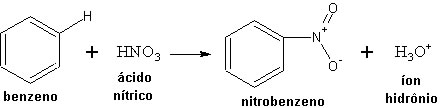
O benzeno também pode reagir com ácido nítrico em presença de ácido sulfúrico (H2SO4) que, sendo um ácido mais forte que o HNO3, faz com que este se comporte como base de Lewis, recebendo um próton do H2SO4. Veja a equação que representa o processo:
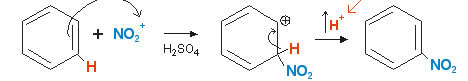
Nesta reação de Nitração ocorre um equilíbrio ácido-base.
2- Sulfonação: esta reação tem como reagente ácido sulfúrico (H2SO4).
Exemplo: Sulfonação do anel benzênico.
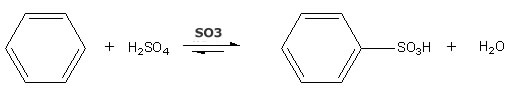
Observe que a reação ocorre na presença de um catalisador - trióxido de enxofre (SO3), e é realizada sob aquecimento. Os produtos da reação são Ácido benzenossulfônico e água.
3- Halogenação: Até pelo nome já se deduz, na Halogenação ocorre a substituição do átomo de hidrogênio por átomos de halogênio (F, Cl, Br, I). As mais comuns são a cloração e a bromação.
Exemplo: Monobromação do Propano
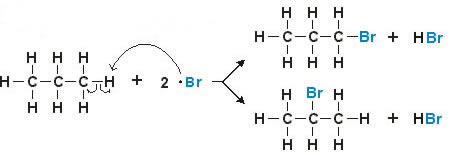
O ligante H da molécula de propano é substituído pelo ligante Br, originando o 1 -Bromo propano ou 2 - Bromo propano.
Observação: As duas setas indicam que o halogênio (Bromo) pode substituir qualquer hidrogênio da estrutura.
Exemplo: Cloração do benzeno.
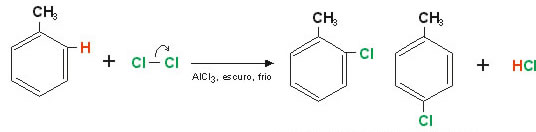
Repare que um dos átomos de hidrogênio presentes no anel benzeno foi substituído por um átomo de Cloro, este pode ocupar tanto a posição orto como a para, daí os produtos: o-clorobenzeno ou p-clorobenzeno.
Por Líria Alves
Graduada em Química
Equipe Brasil Escola
Veja mais!
Ramificações de hidrocarbonetos