Quando o anel benzênico já possui um substituinte, este radical influenciará todas as outras substituições de H no anel. Este substituinte pode ser orto e para-dirigente ou meta-dirigente. Mas surgem as questões:
| O que faz com que o grupo ligado ao anel benzênico influa na direção e na reatividade da reação de substituição? |
| O que faz com que determinados grupos sejam orientadores meta (desativantes) e outros orto-para (ativantes)? |
Essas duas perguntas são respondidas ao se entender os chamados efeitos eletrônicos que esses grupos exercem no anel. Esse efeito ocorre em razão da diferença de eletronegatividade entre os elementos, pois o substituinte irá polarizar as ligações do núcleo aromático, induzindo alternadamente um caráter positivo a alguns carbonos do anel, enquanto outros ficam com caráter negativo.
| Uma nova substituição ocorrerá nos átomos de carbono que tiverem caráter negativo. |
Vejamos como ocorrem esses efeitos eletrônicos no anel aromático, tendo em mente a ordem de eletronegatividade dos elementos: F > O > N > Cl > Br > S > C > I > H.
1º caso: Radical ativante ou orto-para-dirigente:
Por exemplo, no caso abaixo da molécula do benzol (fenol), o oxigênio é o elemento mais eletronegativo, por isso ele atrai os elétrons para si, fazendo com que o carbono fique com uma carga parcialmente positiva, o que induz a polarização alternada do anel. As posições que ficam negativas são exatamente as posições orto e para. Por isso o grupo –OH é um radical ativante ou orto-para-dirigentes. Isso pode ser visto na reação de nitração do fenol abaixo, originando como produtos o o-nitrofenol e o p-nitrofenol:
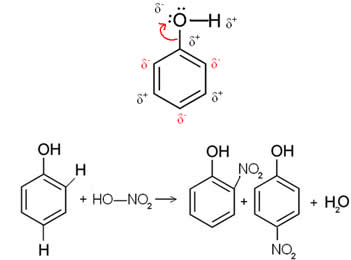
2º caso: Radical desativante ou meta-dirigente:
Considere agora o caso do nitrobenzeno:
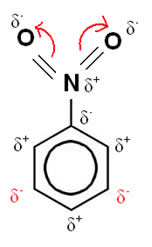
Nesse exemplo, o oxigênio continua sendo o elemento mais eletronegativo, por isso ele atrai para si as ligações feitas com o nitrogênio, que fica com carga parcialmente positiva, induzindo o átomo de carbono ligado a ele a ficar polarizado negativamente e assim sucessivamente. Desse modo, a posição que fica negativa e mais suscetível a uma substituição é a posição meta, sendo ele, portanto, um desativante.
Veja agora mais detalhadamente esse efeito eletrônico, que é denominado efeito ressonante.
| Efeito ressonante é a atração ou repulsão dos elétrons em ligações π (pi) das ligações duplas ou triplas, quando elas entram em ressonância com o próprio anel benzênico. |
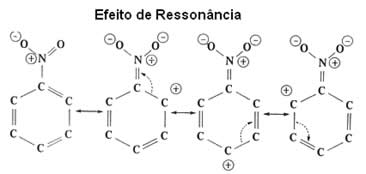
Como visto, o grupo NO2 está desativando o anel, pois está retirando elétrons dele e diminuindo sua densidade eletrônica. Assim, o grupo que irá atacar e fazer a substituição (eletrófilo) é positivo, então ele irá atacar preferencialmente a posição meta que ficou com carga negativa.
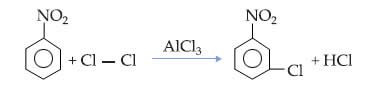
Esse fato pode ser constatado na reação de monocloração do nitrobenzeno, em que a substituição ocorre apenas na posição meta:
Por Jennifer Fogaça
Graduada em Química
Equipe Brasil Escola